
科目: 来源:广东省东莞市2018届中考模拟(一)化学试卷 题型:计算题
阿司匹林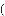
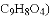 是一种常用解热镇痛药,用于治疗感冒、发烧、头痛等疾病
是一种常用解热镇痛药,用于治疗感冒、发烧、头痛等疾病



查看答案和解析>>
科目: 来源:广东省东莞市2018届中考模拟(一)化学试卷 题型:填空题
(7分)金属在生产、生活中有广泛的用途。
(1)下列金属制品中,分别利用了金属的导热性、 和延展性。

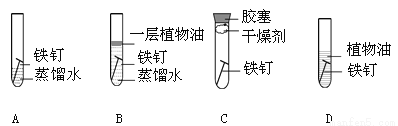
下列四个实验中,铁钉最易生锈的是(填字母) ,B、D中放植物油的目的是 。
(3)工业常用赤铁矿(主要成分为氧化铁)和一氧化碳在高温条件下炼铁,该反应的化学方程式为 。
(4)为验证铁、铜、铝三种金属的活动性顺序,可选用的一组物质是(填字母) 。
A.FeSO4溶液、Cu、AlCl3溶液 B.AlCl3溶液、Fe、Cu
C.CuSO4溶液、Fe、Al D.CuSO4溶液、Fe、AlCl3溶液
(1)导电性 (2)A 隔绝空气或氧气 (3)Fe2O3 + 3CO高温2Fe + 3CO2 (4)D 【解析】 试题分析:(1)铁锅是利用金属的导热性,铜导线是利用铜的导电性,铝箔是利用铝的延展性 (2)铁生锈的条件:与空气、水接触,故四个实验中,铁钉最易生锈的是A,B、D中放植物油的目的是:隔绝空气或氧气 (3)工业常用赤铁矿(主要成分为氧化铁)和一氧化碳在高温条件下炼...查看答案和解析>>
科目: 来源:广东省东莞市2018届中考模拟(一)化学试卷 题型:填空题
A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素.其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分.它们之间的部分转化关系如图所示(图中反应条件及部分反应物、生成物已省略).

回答下列问题:
(1)写出下列物质的化学式:A__;D__.
(2)写出由物质C转化为物质B的化学方程式__.
(3)写出物质C与过氧化钠(Na2O2)反应生成碳酸钠和物质A的化学方程式__.
(1)O2CaCO3 (2) CO2+ C高温 2CO (3) 2CO2+ 2Na2O2= 2Na2CO3+ O2 【解析】试题分析:B为氧化物,且B为有毒气体,说明B是一氧化碳,D是大理石的主要成分,说明D是碳酸钙,C也是氧化物,C和B能够互相转化,说明C是二氧化碳,A是一种气体单质,说明A是氧气。带入后符合题意。查看答案和解析>>
科目: 来源:广东省东莞市2018届中考模拟(一)化学试卷 题型:填空题
某同学在实验室用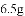
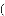

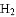 。
。


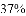
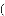
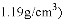 的体积为______
的体积为______

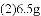
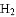 的质量为
的质量为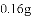

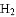 ,装置如图所示。
,装置如图所示。
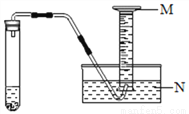
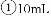
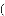


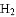 体积V______
体积V______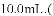



查看答案和解析>>
科目: 来源:广东省东莞市2018届中考模拟(一)化学试卷 题型:实验题
化学是一门以实验为基础的学科,正确认识和使用实验装置进行实验是我们学习的一项重要内容。
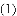


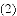
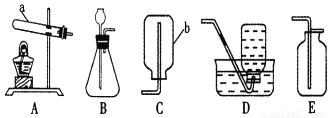

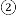
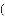

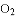 外,还可以制取的一种气体是______
外,还可以制取的一种气体是______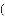

查看答案和解析>>
科目: 来源:广东省东莞市2018届中考模拟(一)化学试卷 题型:综合题
硝酸铜是制备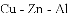

该小组同学查阅资料发现有三种设计方案可供选用:
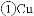
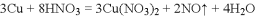
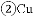
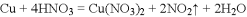
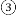
甲同学认为三种方案的反应都可以在铁制容器中进行,乙同学认为______




硝酸铜为蓝色固体,溶于水可得蓝色溶液
【提出问题】硝酸铜在加热条件下到底发生了怎样的反应?
【查阅资料】

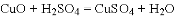
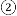
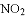 是红棕色、有刺激性气味的气体.
是红棕色、有刺激性气味的气体.
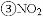 有助燃性,能使带火星的木条复燃
有助燃性,能使带火星的木条复燃
【猜想假设】
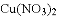 受热分解除了生成______,还可能生成了CuO和
受热分解除了生成______,还可能生成了CuO和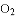 .
.
【进行实验】
实验操作 | 实验现象 | 实验结论 |
步骤I:将反应后试管中的固体加水充分溶解,过滤, ______ ,加热 | 固体全部溶解,得到蓝色溶液 | 硝酸铜分解生成了氧化铜. |
步骤II:在如图的试管和集气瓶之间连上此图所示的装置,重新进行加热硝酸铜的实验 | 集气瓶中气体为无色,______ | 硝酸铜分解生成了氧气 |
步骤II是同学们查阅了新的资料后设计完成的
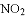 ______方面的性质信息.
______方面的性质信息.
【获得结论】根据实验结果,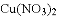 受热分解的化学方程式为______.
受热分解的化学方程式为______.
该小组同学取10g的硝酸铜加热一段时间后,测得剩余固体的质量为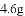


【反思与评价】
已知相同状况下,气体的体积比等于其分子个数比
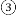
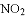 可能具有助燃性
可能具有助燃性
查看答案和解析>>
科目: 来源:广东省东莞市2018届中考模拟(一)化学试卷 题型:填空题
氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
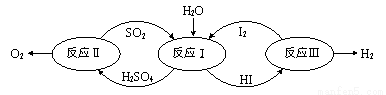
(1)反应I中,发生反应的化学方程式为 。
(2)反应Ⅲ中,反应前后化合价发生改变的元素是 ,发生反应的基本类型为 反应。。
(3)在整个反应过程中,可循环使用的物质有 ,制得H2中氢元素最初来源于 (填化学式)。
⑴ SO2+2H2O+I2=== H2SO4 +2HI ⑵ H、I;分解 ⑶SO2、I2 、H2SO4、HI ;H2O 【解析】 试题分析:反应I中,发生反应的化学方程式为SO2+2H2O+I2=== H2SO4 +2HI。反应Ⅲ中,反应前后化合价发生改变的元素是 H、I,发生反应的基本类型为分解反应,碘和氢元素都从化合物变为单质,在整个反应过程中,可循环使用的物质有SO2、I2 、H...查看答案和解析>>
科目: 来源:广东省东莞市2018届中考模拟(一)化学试卷 题型:计算题
BaCl2是一种重金属盐,其水溶液具有很强的毒性。若误服了BaCl2溶液可立即服用MgSO4溶液解毒。为测定某BaCl2溶液的溶质质量分数,现取100克BaCl2溶液,不断加入MgSO4溶液,反应过程中溶液总质量与加入MgSO4溶液的质量关系如图所示,请回答:
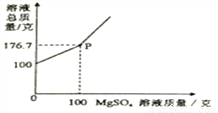
(1)P点时溶液中的溶质名称是_________________;
(2)反应生成沉淀的最大质量为_________________克;
(3)试计算原溶液中BaCl2溶液的溶质质量分数为_________________。
MgCl2 23.3g 20.8% 【解析】(1)当硫酸镁溶液的质量加到100g时,溶液总质量出现拐点,此后随着硫酸镁溶液的增加,溶液总质量增加,不再产生新的变化。故P点时硫酸镁溶液与氯化钡溶液恰好完全反应生成硫酸钡沉淀和氯化镁。因此P点时溶液中的溶质名称是氯化镁; (2)由图可知,反应生成沉淀的最大质量为100g+100g-176.7g=23.3g; (3)设原BaCl2溶液的...查看答案和解析>>
科目: 来源:山西省晋中市2018届中考考前适应性训练理综化学试卷 题型:单选题
下列生活中的变化属于化学变化的是
A. 酒精燃烧 B. 瓷碗破碎 C. 干冰升华 D. 灯泡发光
A 【解析】A、酒精燃烧后生成水和二氧化碳,有新物质的生成,是化学变化,正确; B、瓷碗破碎是瓷碗的形态发生了变化,没有新物质的生成,是物理变化,错误; C、干冰是固态的二氧化碳,干冰易升华,吸热,变为气态的二氧化碳,该过程中没有新物质的生成,是物理变化,错误; D、灯泡发光没有新物质生成,是物理变化,错误。故选A。查看答案和解析>>
科目: 来源:山西省晋中市2018届中考考前适应性训练理综化学试卷 题型:单选题
随着生活水平的提高,餐桌上的饮料种类越来越丰富。下列饮品中属于溶液的是
A. 牛奶 B. 豆浆 C. 冰水 D. 雪碧
D 【解析】A、牛奶是乳浊液,不是溶液,错误; B、豆浆不具有稳定性,不是溶液,错误; C、冰水是纯净物,不是溶液,错误; D、雪碧是碳酸的水溶液,是溶液,正确。故选D。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com