
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:单选题
甲乙丙有如图所示的转化关系(“→”表示反应一步实现,部分反应物和反应条件略去),下列各组物质按照甲乙丙的顺序不符合要求的是
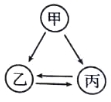
A.C、CO2、CO
B.H2O2、O2、H2O
C.CuO、Cu、Cu(NO3)2
D.NaOH、NaCl、NaNO3
D 【解析】A、碳不完全燃烧生成一氧化碳,一氧化碳燃烧生成二氧化碳,二氧化碳和碳高温下反应生成一氧化碳;碳完全燃烧生成二氧化碳。B过氧化氢分解生成水和氧气,氧气和氢气反应生成水,水分解生成氧气;C氧化铜和氢气反应生成铜和水,氧化铜和硝酸反应生成硝酸铜;铜和硝酸银反应生成铜和硝酸银,硝酸铜和铁反应生成硝酸亚铁和铜;D、氢氧化钠和盐酸反应生成氯化钠和水,氯化钠和硝酸银反应生成氯化银和硝酸钠,硝酸...查看答案和解析>>
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:填空题
钛(Ti)具有硬度大,密度小,熔点高,抗腐蚀性能好等优良性能,被誉为“未来金属”。现有5种含钛元素的物质:Ti、TiO2、Ti2O3、TiCl4、K2TiO3。回答下列问题:
(1)Ti2O3读作_____________。
(2)上述5种物质中钛元素的化合价一共有______种。
(3)从物质分类的角度看,K2TiO3属于_______。(填选项)
A.盐 B.氧化物 C.碱
(4)已知Ti2(SO4)3溶于水溶液呈紫色。Ti2O3(紫黑色固体)在加热条件下可溶于硫酸,生成Ti2(SO4)3 。可观察的现象是_________________。
三氧化二钛 3 A 紫黑色固体消失,溶液由无色变为紫色 【解析】(1)根据氧化物的命名方法来分析;(2)根据单质的化合价为0,化合物中各元素正负化合价的代数和为0来分析;(3)根据物质的分类来分析;(4)根据化学反应的原理以及实验现象来分析。(1)由氧化物的命名方法可知,Ti2O3读作三氧化二钛;(2)Ti属于单质,化合价为0;TiO2中氧元素显-2价,则钛元素显+4价;Ti2O3中氧元素显...查看答案和解析>>
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:填空题
下图中,①是钠元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。
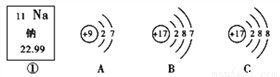
试回答下列问題:
(1)钠元素的原子序数为______________;
(2)A、B、C中属于同种元素的粒子是________________(写字母编号);
(3)A和B两种粒子的_____________相同,所以它们有相似的化学性质;在化学反应中它们容易______________(填“得到”或“失去”)电子;
(4)C所表示的粒子是_____________________(填“原子”或“离子”)。
11 BC 最外层电子数 得到 离子 【解析】根据所学知识和题中信息知,(1)钠元素的原子序数为11;(2)A、B、C中属于同种元素的粒子是B C;质子数决定元素种类。(3)A和B两种粒子的最外层电子数相同,所以它们有相似的化学性质;最外层电子数决定元素的化学性质。在化学反应中它们容易得到电子;(4)C所表示的粒子是离子,核外电子数不等于核内质子数。查看答案和解析>>
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:综合题
现实验室要把20%的硫酸配制成5%的稀硫酸,小洪同学看了室内温度计上的示数为25℃。查了书本中不同温度下各浓度的硫酸密度(g/ml),部分数据如下:
H2SO4浓度% | 15℃时密度 | 20℃时密度 | 25℃时密度 | 30℃时密度 |
15 | 1.1045 | 1.1020 | 1.0994 | 1.0968 |
20 | 1.1424 | 1.1394 | 1.1365 | 1.1335 |
25 | 1.1816 | 1.1783 | 1.1750 | 1.1718 |
(1)从表中数据分析,可以得出不同质量分数硫酸的密度与温度的关系为: ________。
(2)25℃时要配制20g质量分数为5%的稀硫酸,需要质量分数为20%的硫酸的体积为____________ml(保留小数点后一位小数),需要量取水_________ml。
(3)将质量分数为98%的浓硫酸稀释为质量分数为20%的稀硫酸溶液时,下列操作正确的是___________(填序号)。
①将浓硫酸沿烧杯壁缓慢地注入盛有水的烧杯里
②倾倒时,试剂瓶口要紧挨着烧杯壁
③震荡,使烧杯内的溶液混合均匀
温度越高,硫酸密度越小 4.4 15 ①② 【解析】(1)由图中数据分析解答;(2)根据溶液配制前后溶质质量不变分析解答;(3)根据浓硫酸的稀释步骤解答。(1)从表中数据分析,可以得出不同质量分数硫酸的密度与温度的关系为温度越高,硫酸密度越小;(2)设需要20%的硫酸的体积为x。 20g×5%=x×1.1365g/ml×20% x=4.4 mL 4.4 mL×1.13...查看答案和解析>>
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:流程题
生产金属镁后的废渣可以综合利用制备光卤石(MgCl2·6H2O)和金属镁,其工业流程如下图所示:
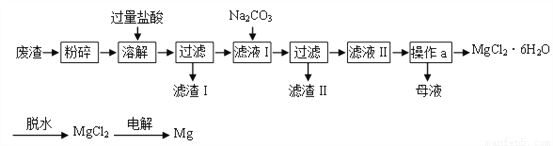
已知:①废渣的主要成份:MgCl2、KCl、MgO、BaCl2、CaCl2、粉尘等杂质。
②MgCO3微溶于水,本题中视为可溶。
回答下列问题:
(1)将废渣粉碎的作用是_______________________。
(2)流程中往滤液I中加入Na2CO3时发生了多个化学反应,请写出其中能够产生气体的那个化学方程式______________________。
(3)滤渣Ⅱ的主要成分____和____;母液的主要成分有3种,分别是MgCl2、____和____。
(4)操作a包含多个操作,分别为______________________过滤,洗涤,干燥。
增大接触面积,加快溶解过程反应速率 Na2CO3+2HCl= 2NaCl+H2O+CO2↑ CaCO3 BaCO3 KCl NaCl 蒸发浓缩,冷却结晶 【解析】(1)根据增大接触面积,加快溶解过程反应速率解答;(2)根据盐酸与碳酸钠反应生成氯化钠、水和二氧化碳解答;(3)根据碳酸钠与氯化钡和氯化钙反应生成碳酸钡和碳酸钙的沉淀及废渣粉碎溶解后的溶液中含有氯化镁、氯化钾及过量盐酸与碳酸钠反应生...查看答案和解析>>
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:简答题
NaCl在生产和生活中具有广泛的用途,是一种重要的资源。通过晾晒海水可以得到粗盐和母液(又叫苦卤)。下图为母液中最主要的四种盐(NaCl、KCl、MgCl2、MgSO4)的溶解度曲线图。回答下列问题:
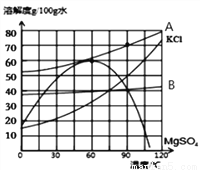
(1)①90℃时,四种盐中MgCl2的溶解度最大,则表示 MgCl2溶解度曲线的是_________。(填“A”或“B”)此时饱和MgCl2溶液的质量分数为_______(请写出计算表达式即可)
②四种盐中溶解度受温度变化的影响最小的 是___________。(填化学式)
(2)60℃时,若母液中的NaCl、KCl、MgCl2、MgSO4都已达到饱和,为了获得较纯净的MgSO4晶体,可采用的方法是_____________。
(3)工业上常通过加入碱溶液与母液中的Mg2+反应来制取Mg(OH)2沉淀。为了探究获得较高Mg2+沉淀率的反应条件,进行下列对比实验(每组实验取250mL母液):
实验序号 | 反应温度/℃ | 反应时间/min | 反应pH值 | Mg2+的沉淀率/% |
a | 40 | 60 | 10 | 90.1 |
b | 40 | 60 | 12 | 92.7 |
c | 40 | 90 | 12 | 93.6 |
d | 50 | 60 | 12 | 96.4 |
e | 50 | 90 | 12 | x |
①反应过程中需测定溶液的pH,则测定溶液pH的操作是:先在玻璃片上放一小片pH试纸,然后用_____________,再将试纸显示的颜色与标准比色卡比较,读取溶液的pH。
②实验a和b对比,可得到的结论是___________________。
③表格中X的数值可能为__________(填编号)。
A.95.8 B.92.1 C.97.2 D.93.1
A 7/17 NaCl 升高温度 用玻璃棒蘸取(或胶头滴管吸取)溶液滴到pH试纸上 在反应温度和反应时间相同时,反应pH值越大,Mg2+的沉淀率越大 C 【解析】(1)根据溶解度曲线解答;(2)根据氯化镁的溶解度曲线分析解答;(3)根据测定溶液pH的方法及对比实验分析解答。(1)①由溶解度曲线可知,90℃时,A的溶解度最大,故表示 MgCl2溶解度曲线的是A;此时饱和MgCl2溶液的质量分数...查看答案和解析>>
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:综合题
利用下列仪器进行气体的制取实验。请根据要求填空。

(1)实验室为制取一瓶较纯净的氧气,选取了加热氯酸钾与二氧化锰的方法,应选取的装置组合是_______________(填字母,下同),如果改用过氧化氢溶液制取氧气,制取1.6g氧气,需要5%的过氧化氢溶液的质量为:______g。
(2)实验室用硫化亚铁(FeS)固体与稀硫酸混合制硫化氢气体,该反应的化学方程式是_______,选用的发生装置是_________;
(3)某同学用大理石与浓盐酸反应制取二氧化碳时,发现收集到的二氧化碳气体中混入大量氯化氢气体和水蒸气,于是使用了下边装置进行处理,得到纯净、干燥的二氧化碳。那么混合气体应先进入装置_______再进入装置________。
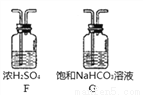
查看答案和解析>>
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:填空题
下图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。
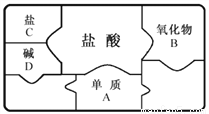
(1)A不可能是______(填标号)。
a.Mg b.Fe c.Ag d.Zn
(2)若B为铁锈的主要成分Fe2O3,B与盐酸反应的化学方程式为_________________。
(3)若C为碳酸钠
①C与D的反应属于______(填基本反应类型)。
②D与盐酸反应的化学方程式为______(写一个)。
③将二氧化碳通入C溶液,可化合生成碳酸氢钠( NaHCO3),该反应的反应物有______种。
c Fe2O3+6HCl= 2FeCl3+3H2O 复分解反应 2HCl+Ca(OH)2= CaCl2+2H2O(或“2HCl+Ba(OH)2= BaCl2+2H2O”) 3 【解析】(1)根据金属活动性顺序的应用:位于氢前面的金属能与酸反应生成氢气,银位于氢的后面,故不能与稀盐酸反应,故选c;(2)氧化铁与稀盐酸反应生成氯化铁和水,反应的化学方程式表示为Fe2O3+6HCl= 2FeCl3...查看答案和解析>>
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:实验题
CO2在高温下能与木炭反应生成CO。为验证该反应,某课外兴趣小组设计了一套实验装置,装置图如下:
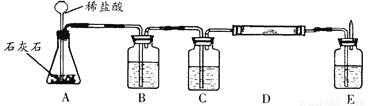
(1)根据装置图,填写下表:
仪器标号 | 仪器中所加物质 | 作用 |
A | 石灰石,稀盐酸 | 石灰石与盐酸作用产生CO2 |
B | 饱和碳酸氢钠溶液(与CO2不反应) | 除去CO2中的HCl气体 |
C | _____________________ | ____________ |
D | __________________ | ________________ |
E | ______________ | ________________ |
(2)D处要增加的仪器的名称是___________________________。
浓硫酸 除去CO2中的水蒸气 木炭粉 与CO2在高温下反应 NaOH溶液(或澄清石灰水) 吸收(除去)CO2 酒精灯或酒精喷灯 【解析】(1)C中装有浓硫酸,浓硫酸有吸水性,故其作用是吸水作干燥剂;D中装有木炭,作用是在高温下和二氧化碳反应生成一氧化碳;E中装有NaOH溶液,作用是吸收未反应的CO2; (2)根据碳与二氧化碳反应需要高温分析解答。(1)C中装有浓硫酸,浓硫酸有吸水性,故其作...查看答案和解析>>
科目: 来源:广东省广州市番禺区2018届九年级中考一模测试化学试卷 题型:科学探究题
某草木灰(主要成分为K2CO3,杂质不溶于水)样品,可能还添加了K2SO4、KCl。某化学兴趣小组进行了如下实验:
(1)样品的预处理:

①操作a的名称为__________________,其目的是____________________
②溶液A中主要的阴离子,除CO32-外,可能还含有_______________(填离子符号)
(2)样品成分的确定:设计实验方案,完成下述表格;限选试剂:稀盐酸、稀硝酸、稀硫酸、氯化钡溶液、硝酸钡溶液、硝酸银溶液
实验操作 | 预期现象和必要结论 |
步骤1:取溶液A少量于试管中,加入足量 _______________,充分振荡,静置,过滤。 |
|
步骤2:取少量步骤1所得的滤液于试管中,____________ | ______,说明样品中未添加KCl |
步骤3:取少量步骤1所得的滤渣于试管中,__________________ | ______,说明样品中添加了K2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com