
科目: 来源:江苏省苏州市2017~2018学年初三化学第二次模拟测试卷(1) 题型:简答题
“人工固氮”的新方法的反应过程示意图如下:

(1)依据反应的微观示意图写出化学方程式____________。
(2)氨气进入大气后与雨水作用,可能形成“碱雨”。写出碱雨中的碱的化学式,并标出其中氮元素的化合价________________。
(3)氨是氮肥工业的重要原料。某化肥厂生产铵态氮肥(NH4)2SO4的工艺流程如下:

① 加入的X 应为________________(填字母序号)。
A.H2SO4 B.CaSO4 C.SO2
②生产流程中能被循环利用的物质是_________________。
6H2O + 2N2 =4NH3 + 3O2 H3.H2O B CO2 【解析】(1)由微观示意图可知,反应物是水和氮气,生成物是氨气和氧气,故反应方程式为6H2O + 2N2 = 4NH3 + 3O2 (2)氨气与水反应生成氨水,生成的氨水的化学式为NH3·H2O;氨水中氢元素的化合价为+1价,根据化合价的代数和为0可求得氮元素的化合价为-3价,化合物中元素的化合价标在该元素的正上方...查看答案和解析>>
科目: 来源:江苏省苏州市2017~2018学年初三化学第二次模拟测试卷(1) 题型:实验题
完成下列基础学生实验。根据下列装置图,回答有关问题。
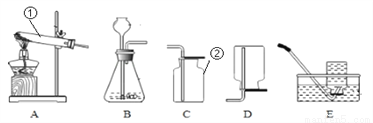
(1)写出图中标号仪器的名称:① ______________ ②_______________。
(2)用大理石与稀盐酸反应制取CO2,化学方程式为 __________,应该选用的发生和收集装置分别是_______。检验二氧化碳收集满的方法是____________。
(3)如果选择KClO3与MnO2的混合物作为制备O2的药品时,则反应过程中,MnO2的质量将___(填“增加”、“减小”或“不变”等)。
(4)下图装置可用于气体的收集、检验、除杂和体积的测量等,用该装置不能完成的实验是______(填序号)。
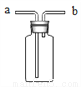
A.气体从b端通入,收集二氧化碳。
B.瓶内装有澄清石灰水,气体从a端通入,检验氧气中是否混有二氧化碳。
C.瓶内装有氢氧化钠溶液,气体从a端通入,除去一氧化碳中混有的二氧化碳。
D.瓶内装满水,在b端接量筒,气体从a端通入,测量气体的体积。
II.对含有固体不溶物的粗盐进行初步提纯并计算纯度。
(1)实验主要步骤:称量一定质量的粗盐、__________、称量剩余粗盐、过滤、蒸发、称量精盐。蒸发操作时,待蒸发皿中出现____________时停止加热,利用余热将滤液蒸干。
(2)下列因素会导致获得的精盐质量偏小的是_____________(填序号)
A.粗盐中加入过量的水 B.过滤时,滤纸破损
C.过滤后,滤纸上的泥沙未用水洗涤 D.蒸发时,液滴溅出
试管 集气瓶 CaCO3 + 2HCl=CaCl2+ H2O + CO2↑ BC 将燃着的小木条放在集气瓶口处,木条熄灭,证明已经集满二氧化碳。 不变 AD 溶解 较多固体 CD 【解析】(1)仪器①的名称是试管,仪器②的名称是集气瓶; (2)大理石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,反应方程式为CaCO3 + 2HCl=CaCl2+ H2O + CO2↑;...查看答案和解析>>
科目: 来源:江苏省苏州市2017~2018学年初三化学第二次模拟测试卷(1) 题型:填空题
某科研小组设计利用稀H2SO4浸取某废弃的氧化铜锌矿(主要成分为CuO和ZnO,其余成分既不与酸反应,也不溶解于水)的方案,实现废物综合利用。部分实验流程如下:
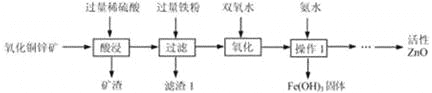
请根据上述实验流程回答下列问题:
(1)操作1的名称是 。
(2)在氧化铜锌矿中加入过量稀硫酸,主要成分发生反应的化学方程式为 , 。
(3)加过量铁粉后,发生反应的基本反应类型是 ,得到滤渣1的成分为 (填化学式)。
(4)在实验过程中,双氧水会与Fe2+反应生成Fe3+和水,以便在后续的操作中将溶液中铁元素除去。高锰酸钾溶液也能将Fe2+氧化成Fe3+,选用双氧水的优点是 。
(1)过滤 (2)ZnO+H2SO4═ZnSO4+H2O CuO+H2SO4=CuSO4+H2O (3)置换反应 Fe、Cu (4)不引入较难除去的杂质 【解析】(1) 操作1的名称是过滤,过滤能把沉淀和滤液分开;(2)在氧化铜锌矿中加入过量稀硫酸,稀硫酸和氧化铜反应生成硫酸铜和水,和氧化锌反应生成硫酸锌和水,反应的化学方程式为:CuO+H2SO4═CuSO4+H2O或Zn...查看答案和解析>>
科目: 来源:江苏省苏州市2017~2018学年初三化学第二次模拟测试卷(1) 题型:简答题
溶液在生产、生活和实验中起着十分重要的作用。请回答下列问题:
(1)井水中通常含有较多的 ______________, 属于硬水。取等量的井水和蒸馏水,向其中加入______________充分振 荡,可以检验出井水和蒸馏水。
(2)t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛 100g 水的两个烧杯中,充分搅拌后现象如图 1 所示, 硝酸钾和氯化钾的溶解度曲线如图 2 所示。
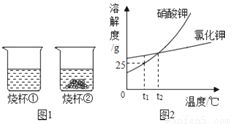
I.烧杯①的溶质是 ______________(填名称);将图 1 中两烧杯内的物质温度升高到 t2℃(不考虑水的蒸发),充分搅拌 后两烧杯内所得溶液中溶质的质量分数______________(选填:相等、不相等、无法确定)。
II.要除去 KNO3 固体中混有的少量 KCl 的实验操作是:加适量水溶解→加热得到热饱和溶液___________→过滤→ 洗涤→干燥。
(3)水是一种常用的溶剂,下列各组固体物质能用水鉴别的是______________(填字母)。
A.氢氧化钠和硝酸铵 B.碘和高锰酸钾
C.碳酸钙和氯化钙 D.氯化钠和硫酸钠
(4)用浓硫酸配制 10%稀硫酸时,不需要用到的仪器 ______________(填字母)。
A.托盘天平 B.胶头滴管 C.漏斗 D.量筒
可溶性钙镁化合物; 肥皂水; 氯化钾; 相等; 降温结晶; ABC; AC 【解析】(1)硬水中含有较多的钙、镁离子,由于硬水遇肥皂水产生的泡沫少,软水遇肥皂水产生的泡沫多,所以,我们可以用肥皂水来检验井水是软水还是硬水。 (2)I.t1℃时,烧杯①中溶质全部溶解,因为在该温度下,氯化钾的溶解度大于硝酸钾,溶质是氯化钾;t2℃时两种物质的溶解度相等,升温到t2时,两种物质都完全溶解形成...查看答案和解析>>
科目: 来源:江苏省苏州市2017~2018学年初三化学第二次模拟测试卷(1) 题型:科学探究题
馒头、面包等发面食品在制作时都需使用发酵粉,发酵粉的主要成分最常见的是碳酸钠、碳酸氢钠等。某兴趣小组的同学对制作馒头用的发酵粉(白色粉末)进行探究。
【提出问题】白色粉末成分是什么?
【进行猜想】 猜想Ⅰ:碳酸钠 ; 猜想Ⅱ:碳酸氢钠; 猜想Ⅲ:__________________。
【初步探究】取少量白色粉末于试管中,加适量水,测得溶液的 pH=10.5,说明溶液呈________性。
【查阅资料】
(1)碳酸氢钠受热易分解,该反应可表示为2NaHCO3  Na2CO3+CO2↑+H2O;而碳酸钠很稳定,受热不易分解。
Na2CO3+CO2↑+H2O;而碳酸钠很稳定,受热不易分解。
(2)参照实验:
NaHCO3稀溶液 | Na2CO3稀溶液 | |
加入稀盐酸 | 产生气泡 | 产生气泡 |
加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 |
【实验探究】:
甲、乙、丙三位同学分别设计三种不同实验方案进行探究。
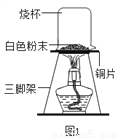
甲同学方案:如图1,取适量发酵粉在铜片上加热,加热一段时间后,观察到烧杯内壁有液滴出现,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到_____________。甲得出结论: 猜想Ⅱ正确。
乙同学方案:
实验步骤 | 实验现象 | 实验结论 |
①取少量发酵粉于加足量水后形成的无色稀溶液,再加入过量CaCl2溶液,静置。 | 有白色沉淀产生 | 化学方程式 __________。 |
②再取步骤①的上层清液,加入稀盐酸 | 有气泡冒出 | 该清液中含 ____________。 |
乙得出结论: 猜想Ⅲ正确。
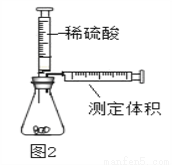
丙同学方案:用如图2所示,锥形瓶中分别盛有等质量的碳酸钠、碳酸氢钠和发酵粉,再注入等体积、等浓度的足量的稀硫酸,准确测量生成气体的体积。
记录如表:
实验 编号 | 锥形瓶内物质 | 最终得到 CO2 体积/mL | |
名称 | 质量/g | ||
① | 碳酸钠 | a | V1 |
② | 碳酸氢钠 | a | V2 |
③ | 发酵粉 | a | V3 |
【实验结论】经同学们讨论,最终确认:该发酵粉是碳酸钠和碳酸氢钠的混合物。
【反思应用】
(1)同学们讨论时认为:甲同学方案不严密的原因是_____________________________。
(2)乙同学方案中,实验①中加入CaCl2溶液要过量的目的是____________________。
(3)丙同学方案也能得到正确结论应满足的条件是_____________________________。
(4)制作馒头、面包时,将面粉发酵(产生有机酸),再加入适量的碳酸氢钠,可以使馒头、面包松软。原因是________________。
(5)将12.0g该白色粉末加热至完全反应,剩余固体的质量为8.9g,计算该白色粉末中Na2CO3的质量分数为 _________________。(写出计算过程)
碳酸钠和碳酸氢钠 碱 澄清石灰水变浑浊 CaCl2 + Na2CO3 CaCO3↓+ 2 NaCl; 碳酸氢钠(NaHCO3) 猜想Ⅲ也会产生相同的现象 (其它表达合理时,也可) 除净碳酸钠 V1<V3<V2 碳酸氢钠与有机酸(在水溶液中)反应生成二氧化碳气体,(气体在面团中形成许多小气室 ,使馒头、面包疏松多孔) 30% 【解析】【进行猜想】发酵粉主要是碳酸钠或碳酸氢钠与有机酸反应,故猜想...查看答案和解析>>
科目: 来源:湖北省随州市2018届九年级中考模拟(3)化学试卷 题型:单选题
下列过程中发生化学变化的是( )
A. 食物腐败变质 B. 分离液态空气制氧气
C. 活性炭吸附冰箱中的异味 D. 海水晒盐
A 【解析】有新物质生成的变化是化学变化,无新物质生成的变化是物理变化。A. 食物腐败变质,有新物质生成,属于化学变化,符合题意;B. 分离液态空气制氧气,无新物质生成,属于物理变化,不符合题意;C. 活性炭吸附冰箱中的异味,无新物质生成,属于物理变化,不符合题意;D. 海水晒盐,无新物质生成,属于物理变化,不符合题意。故选A。查看答案和解析>>
科目: 来源:湖北省随州市2018届九年级中考模拟(3)化学试卷 题型:单选题
下列实验操作正确的是( )
A.  过滤 B.
过滤 B. 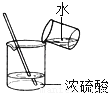 稀释浓硫酸
稀释浓硫酸
C.  闻气味 D.
闻气味 D. 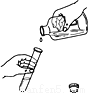 倾倒液体
倾倒液体
查看答案和解析>>
科目: 来源:湖北省随州市2018届九年级中考模拟(3)化学试卷 题型:单选题
喝酒不开车,开车不喝酒。酒后驾驶是一种违法行为。酒精的化学式为C2H5OH。下列有关酒精的说法正确的是
A.酒精中氢元素的质量分数最大
B.酒精中碳、氢元素的质量比为1:3
C.酒精属于有机物
D.酒精是由2个碳原子、6个氢原子和1个氧原子构成的
C 【解析】A、C2H5OH中个元素的质量分数:氢元素:6 46 ×100%,碳元素:24 46 ×100%,氧元素:16 24 ×100%;显然碳元素的质量分数最大,故A错误; B、已知C2H5OH,酒精中碳、氢元素的质量比为24:6=4:1,故B错误; C、酒精属于有机物,因为含有碳元素,具有有机物的特征,故C正确; D、“一个”酒精分子是由2个碳原子、6个氢原子和1个...查看答案和解析>>
科目: 来源:湖北省随州市2018届九年级中考模拟(3)化学试卷 题型:单选题
按下表提供的信息,以下判断正确的是

A.第三周期元素的原子核外电子层数从左到右依次增多
B.第二周期的Li、Be和B均为金属元素
C.Mg2+、H+最外层电子数分别为2和0
D.Na+和Al3+ 的核外电子数相同
D 【解析】 试题分析:A、同周期元素的原子核外电子层数相同,第三周期元素的原子核外电子层数都为三层,错误;B、第二周期的Li、Be为金属元素,B为非金属元素,错误;C、Mg2+的最外层电子数为8,H+最外层电子数为0,错误;D、Na+和Al3+ 的核外电子数相同,都为10,达到相对稳定结构。查看答案和解析>>
科目: 来源:湖北省随州市2018届九年级中考模拟(3)化学试卷 题型:单选题
小明为探究金属与盐的反应,将一定质量的某种金属M的粉末放入AgNO3与Cu(NO3)2的混合溶液中,充分反应后发现,溶液呈现无色,溶液底部有少量固体粉末;过滤后在滤渣和滤液中分别加入适量稀盐酸,滤渣中有无色气体产生,滤液中无沉淀产生.结合实际现象判断,小明得出的以下结论错误的是( )
A. 滤液中一定没有银离子 B. 滤渣中一定含有金属单质M
C. 滤渣中一定含有单质铜 D. 加入的金属M可能是单质铁
D 【解析】将金属M放入AgNO3与Cu(NO3)2的混合溶液中,充分反应后溶液呈现无色,说明Cu(NO3)2已经完全反应,则AgNO3一定也完全反应,则置换出的金属是Ag和Cu,由于这两种金属与稀盐酸都不反应,根据“滤渣中加入适量稀盐酸,有无色气体产生”可知,滤渣中一定有剩余的金属M,且M与稀盐酸反应生成了氢气.根据“滤液中加入适量稀盐酸,无沉淀产生”进一步确定,滤液中没有银离子.由于Fe...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com