
科目: 来源:江苏省徐州市2018届九年级下学期第二次模拟考试化学试卷 题型:单选题
NaCl和KNO3的溶解度曲线如图所示。下列说法正确的是

A. KNO3、NaCl都是“微溶于水”的物质
B. 常用冷却热饱和溶液的方法使NaCl结晶
C. 20℃的KNO3饱和溶液升温至60℃,溶液的浓度变大
D. 40℃时将32g KNO3放入50g水中,所得溶液的溶质质量分数约为39%
D 【解析】A、据图可知,KNO3、NaCl20℃的溶解度都大于10g,易溶于水,故选项错误;B、NaCl的溶解度受温度影响较小,常用蒸发溶剂的方法使NaCl结晶,故选项错误;C、20℃的KNO3饱和溶液升温至60℃,溶解度增大,变成不饱和溶液,溶液的浓度不变,故选项错误; D、40℃时,KNO3的溶解度为63.9克,将32g KNO3放入50g水中形成该温度下的饱和溶液,所得溶液的溶...查看答案和解析>>
科目: 来源:江苏省徐州市2018届九年级下学期第二次模拟考试化学试卷 题型:单选题
下列实验操作,很难达到预期目的是
A. 通过点燃,除去CO2中混有的少量CO
B. 通过测量导电性,区分蒸馏水与食盐水
C. 采用溶解、过滤、蒸发的方法,提纯粗盐
D. 采用燃烧闻气味的方法,鉴别羊毛线和涤纶线
A 【解析】A、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项实验操作不能达到预期目的;B、蒸馏水中没有自由移动的离子,不能导电,食盐水中有自由移动的钠离子、氯离子,能导电,通过测量导电性能区分,故选项实验操作能达到预期目的;C、粗盐中的氯化钠溶于水,其它杂质不溶,可按溶解、过滤、蒸发的方法,提纯粗盐,故选项实验...查看答案和解析>>
科目: 来源:江苏省徐州市2018届九年级下学期第二次模拟考试化学试卷 题型:单选题
选用稀H2SO4和NaOH溶液探究中和反应,并借助pH传感器测得烧杯中溶液酸碱度的变化(见图)。下列说法正确的是
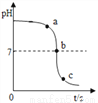
A. 该实验是将NaOH溶液滴到盛有稀H2SO4的烧杯中
B. a点所示溶液中,含有的溶质是Na2SO4和H2SO4
C. c点所示溶液中含有大量的OH-
D. b点到c点的变化过程中,没有发生化学反应
D 【解析】A、由图象可知,pH值是开始时大于7逐渐的减小到7然后小于7,可知原溶液显碱性,然后不断的加入酸性溶液,使pH减小,说明是把稀硫酸滴加到氢氧化钠溶液中,故错误;B、a点的pH大于7,溶液显碱性,溶液中的溶质是硫酸钠和氢氧化钠,故错误;C、c点的pH小于7,溶液显酸性,故错误;D、b点到c点的pH变化,是由于酸过量而产生的,反应已停止,故正确。故选D。查看答案和解析>>
科目: 来源:江苏省徐州市2018届九年级下学期第二次模拟考试化学试卷 题型:填空题
某矿泉水的水质成分(mg/L)如下表所示,请根据表中信息回答:
硅酸(H2SiO3):28.9~42.9 | 锶离子(Sr2+):0.01~0.32 |
碳酸氢根(HCO3--):173~205 | 钙离子:5~45 |
氯离子:1.0~8.0 | 钠离子:45~70 |
硫酸根:16.06~19.52 | 钾离子:0.5~2.0 |
镁离子:2.5~7.5 | pH:7.8 ± 0.5 |
(1)该矿泉水显弱_________性。硅酸中硅元素的化合价是_________。
(2)用化学符号表示:5个锶原子________;硫酸根_________。
(3)由标签中的阴、阳离子构成的一种化合物________(写化学式)。
(4)取该矿泉水少许注入试管,滴入肥皂水,充分振荡,若出现大量的________,则属于____(填硬水或软水)。
碱 +4 5Sr SO42- NaHCO3、Na2SO4、NaCl、CaCl2、Ca(HCO3)2、MgCl2、K2SO4 等 白色垢状物(或泡沫) 硬水(或软水) 【解析】(1)矿泉水的pH:7.8 ± 0.5pH略大于7,显弱碱性;硅酸(H2SiO3)中氢元素显+1价,氧元素显-2价,故硅元素显+4价;(2)有表中的的阴阳离子,按照化合价的规则,可构成的化合物的化学式有:NaHCO3、N...查看答案和解析>>
科目: 来源:江苏省徐州市2018届九年级下学期第二次模拟考试化学试卷 题型:简答题
早在1754年,英国化学家布莱克就发现了一种重要的气体。他曾这样记载:
①灼烧白垩后质量减轻44%,说明有气体从中放出;该气体固定在白垩中,所以它是“固定空气”。②“固定空气”能被熟石灰吸收,生成不溶于水的白垩。③蜡烛在“固定空气”中不燃烧。④麻雀在“固定空气”中会窒息而死。请回答下列问题:
(1)布莱克发现的“固定空气”是_________。
(2)白垩、石灰石、大理石与_________(填生活中的一种物质)等,主要成分相同。
(3)写出资料①、②中有关反应的化学方程式:________、_________。
(4)从资料④可知,进入久未开启的地窖、干涸的深井时,首先要_________。
CO2 鸡蛋壳、珍珠、贝壳等 CaCO3 CaO+CO2↑ Ca(OH)2+CO2=CaCO3↓+H2O 检验二氧化碳浓度(或检验二氧化碳浓度是否有害) 【解析】(1)由②“固定空气”能被熟石灰吸收,生成不溶于水的白垩、③蜡烛在“固定空气”中不燃烧、④麻雀在“固定空气”中会窒息而死,可推知布莱克发现的“固定空气”是CO2;(2)白垩、石灰石、大理石、鸡蛋壳、珍珠、贝壳等的主要成分是碳酸钙;(...查看答案和解析>>
科目: 来源:江苏省徐州市2018届九年级下学期第二次模拟考试化学试卷 题型:实验题
根据下列实验装置图,回答问题:

(1)在B装置中,由无机材料制成的仪器是_________(写一种)。
(2)实验室收集某气体只能用C装置,说明该气体具有_________、________等性质
(3)实验室也用加热氯酸钾和二氧化锰混合物的方法来制取氧气,其中二氧化锰的作用是_______________;若要得到高纯度的氧气,发生装置与收集装置的组合是__________;气体收集完毕,接下来的先后操作是_________。实验结束(氯酸钾已完全分解),从残留固体中分离出的__________(写化学式)可用作钾肥。
(4)实验室制取二氧化碳的化学方程式是_________,应选择的发生装置是________。检验二氧化碳气体是否集满的方法是________。
锥形瓶或分液漏斗 密度大于空气 易溶于水(或能溶于水) 加快反应速率(或催化) AE 先将导管移出水面再熄灭酒精灯 KCl CaCO3+2HCl=CaCl2+CO2↑+H2O B 将燃着的木条放在集气瓶口 【解析】(1)玻璃属于无机材料,据图可以知在B装置中,由无机材料制成的仪器是锥形瓶或分液漏斗;(2)C装置属于向上排空气法收集气体,故该气体应具有密度大于空气、易溶于水(或能溶于水) 的性...查看答案和解析>>
科目: 来源:江苏省徐州市2018届九年级下学期第二次模拟考试化学试卷 题型:科学探究题
某化学兴趣小组在帮助老师整理实验室时,发现一瓶久置的KOH溶液,他们对该溶液中溶质的成分进行了实验探究。
【查阅资料】
①KOH与NaOH的化学性质非常相似。
②K2CO3与Na2CO3的化学性质非常相似。
请用化学方程式解释KOH变质的原因:_________。
【猜想假设】
假设①:没有变质,溶质只含KOH。
假设②:部分变质,溶质含_________。
假设③:完全变质,溶质只含K2CO3。
【进行实验】
实验操作步骤 | 实验现象 | 实验结论 | |
(1)甲同学取样品少许,滴入足量稀盐酸 | 有气泡产生 | 假设________错误 | |
(2)乙同学取样品少许 | 滴入过量BaCl2溶液,振荡,静置 | ________ | 假设②成立 |
再向上层清液里滴加酚酞试液 | ________ |
【问题讨论】
(1)步骤(2)中加入过量BaCl2溶液的作用是________。
(2)要除去该KOH溶液中的杂质,方法是_________(用化学方程式表示)。
2KOH+CO2=K2CO3+H2O KOH、K2CO3 ① 产生白色沉淀 溶液变红 检验KOH是否变质并除尽K2CO3(或除尽K2CO3) Ca(OH)2+K2CO3=CaCO3↓+2KOH(或Ba(OH)2+K2CO3=BaCO3↓+2KOH) 【解析】【查阅资料】KOH与NaOH的化学性质非常相似,所以KOH变质的化学方程式:2KOH+CO2=K2CO3+H2O;【猜想假设】KOH部分...查看答案和解析>>
科目: 来源:江苏省徐州市2018届九年级下学期第二次模拟考试化学试卷 题型:计算题
某化工厂的废水中含有亚硫酸钠(Na2SO3),若直接排放会造成污染。化学兴趣小组对该厂的废水处理设计了下图所示的实验方案:

(提示:Na2SO3 + CaC12 = CaSO3↓ + 2NaCl;CaC12不与废水中的其它杂质反应)
(1)氯化钙的相对分子质量是_________。
(2)反应生成亚硫酸钙沉淀的质量为_________g。
(3)求废水中亚硫酸钠的质量分数为_________(写出计算过程,结果精确到0.1%)。
111 6 12.6% 【解析】(1)氯化钙的相对分子质量=40+35.52=111;(2)根据质量守恒定律可得,生成的亚硫酸钙的质量为50g+50g-94g=6g; 设亚硫酸钠的质量为x, Na2SO3+CaCl2═CaSO3↓+2NaCl 126 120 x 6g x=6.3g, 废水中亚硫酸钠的质量分数为:×100%=12.6%。查看答案和解析>>
科目: 来源:北京市2018届九年级5月月考化学试卷 题型:单选题
下列物质属于溶液的是
A.  白酒 B.
白酒 B.  豆浆 C.
豆浆 C.  酸奶 D.
酸奶 D.  蒸馏水
蒸馏水
查看答案和解析>>
科目: 来源:北京市2018届九年级5月月考化学试卷 题型:单选题
往滴有石蕊的稀盐酸溶液中逐渐滴入氢氧化钠溶液并振荡,直至氢氧化钠过量,可观察到溶液颜色的变化是
A. 红—蓝—紫 B. 红—紫—蓝 C. 蓝—紫—红 D. 蓝—红—紫
B 【解析】紫色石蕊溶液遇酸性溶液变红色,遇碱性溶液变蓝,滴有石蕊的稀盐酸溶液显红色,逐渐滴入氢氧化钠溶液并振荡,氢氧化钠与稀盐酸反应生成氯化钠和水,至恰好完全反应,溶液显中性,溶液呈紫色;至氢氧化钠过量,溶液显碱性,溶液呈蓝色,则可观察到溶液颜色的变化是红-紫-蓝。故选B。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com