
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:单选题
推理是一种重要的化学思维方法,以下推理合理的是
A. 溶液是均一稳定的,但均一稳定的物质不一定是溶液
B. 碳酸盐能与酸反应生成气体,所以能与酸反应生成气体的一定是碳酸盐
C. 单质由同种元素组成,所以由同种元素组成的物质一定是单质
D. 中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应
A 【解析】A、溶液是均一稳定的混合物,均一稳定的物质不一定是溶液,如水,正确;B、碳酸盐能与酸反应生成气体,但能与酸反应生成气体的不一定是碳酸盐,如活泼金属铁等,错误;C、单质由同种元素组成,但由同种元素组成的物质不一定是单质,如氧气与臭氧组成的物质,错误;D、中和反应一定有盐和水生成,但有盐和水生成的反应不一定是中和反应,如二氧化碳与氢氧化钙溶液反应生成碳酸钙和水,错误。故选A。查看答案和解析>>
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:单选题
利用催化剂可消除室内装修材料释放的甲醛,其反应微观示意图如下,下列说法正确的是

A. 该反应可以将无机物转化为有机物
B. 该反应中包含三种氧化物
C. 该反应中生成物的质量比为22∶9
D. 该反应中反应物三种原子个数比为1∶1∶1
C 【解析】由反应的微观示意图可知,反应的方程式是CH2O+O2CO2+H2O。A、由反应的化学方程式可知,该反应可以将有机物转化为无机物,错误;B、该反应中包含CO2、H2O两种氧化物,错误;C、由反应的化学方程式可知,该反应中生成物的质量比为44:18=22∶9,正确;D、该反应中反应物三种原子个数比为1∶2∶1,错误。故选C。查看答案和解析>>
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:多选题
用“W”型玻璃管进行微型实验。将注射器中的过氧化氢溶液推入管中与二氧化锰接触。下列说法正确的是
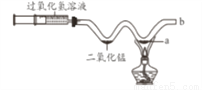
A. 过氧化氢分解能生成氧气
B. 若a处粉末是木炭粉,观察到有二氧化碳生成
C. 若a处粉末是硫粉,b处应接有尾气处理装置
D. 若a处粉末是铜粉,能看到粉末由黑色变为红色
AC 【解析】A、过氧化氢分解能生成氧气,正确;B、二氧化碳是无色气体,即使a处粉末是木炭粉,也无法观察到有二氧化碳生成,错误;C、由于二氧化硫气体有毒,逸散到空气中会造成污染,故若a处粉末是硫粉,b处应接有尾气处理装置,正确; D、若a处粉末是铜粉,红色的铜能与氧气反应生成黑色的氧化铜,故能看到粉末由红色变为黑色,错误。故选AC。查看答案和解析>>
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:单选题
下列除杂质的方法不正确的是
选项 | 物质(括号内为杂质) | 除杂方法 |
A | NaCl(Na2CO3) | 加入足量稀盐酸,蒸发结晶 |
B | KCl(MnO2) | 溶解,过滤,蒸发结晶 |
C | CO2(CO) | 在空气中点燃 |
D | Cu (Fe) | 加入足量的稀盐酸,过滤 |
查看答案和解析>>
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:单选题
按下图装置进行实验,倾斜锥形瓶使足量稀盐酸全部倒入,并与固体接触发生反应,瓶内气压的变化如坐标图所示。下列说法错误的是

A. 块状碳酸钙反应速率较快
B. a点所对应的体系中含有CaCl2和HCl
C. 1 g碳酸钙完全反应后,可获得0.44g 二氧化碳
D. 对比分析坐标图中的a、c点或b、d点,可知化学反应速率与反应物的接触面积有关
A 【解析】A、由图像可知,块状碳酸钙反应速率较慢,错误;B、由图像可知,a点压强在增加的过程中,稀盐酸与粉末状碳酸钙发生反应且稀盐酸未反应完,故a点所对应的体系中含有稀盐酸与碳酸钙反应生成的CaCl2和过量的HCl,正确;C、设1g碳酸钙完全反应后生成二氧化碳的质量为x。 CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 44 0.1g x x=0.44g...查看答案和解析>>
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:多选题
某实验室提出了一种煤制氢技术。其流程如下图所示。
资料:Ⅰ.水煤浆是由煤(主要含碳)与水混合而成,经过气化器后转化为CO2和H2。
Ⅱ.在气化器中发生了两个反应:
①C + H2O CO + H2 ② CO + H2O
CO + H2 ② CO + H2O  CO2 + H2
CO2 + H2

下列说法正确的是
A. 气化器中发生的反应均为置换反应 B. 流程中需不断加入CaO
C. 重整器的作用是分离CO2和H2 D. 100kg氢气燃烧理论上可生成水900kg
CD 【解析】A、气化器中发生的反应①为置换反应,反应②不是置换反应,错误;B、煅烧炉内煅烧碳酸钙生成的氧化钙被加入到重整器中,不需要不断加入CaO,错误;C、重整器的作用是分离CO2和H2,正确;D、设100kg氢气燃烧理论上可生成水的质量为x。 2H2+O2点燃2H2O 4 36 100kg x x=900kg,正确。故选CD。查看答案和解析>>
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:填空题
氯化铵、硫酸钾是常见的化肥,请回答下列问题:
(1)氯化铵的化学式______;
(2)铵根离子______(填写离子符号),其氮元素化合价为______;
(3)铵态氮肥不能与碱性肥料混合施用。氯化铵与氢氧化钠溶液共热反应的化学方程式为____。碳酸氢铵应避免在气温较高时使用,其受热分解的化学方程式为________。碳酸氢铵还能与盐酸反应,其化学方程式为________;
(4)下列物质属于复合肥的是____________;(填写字母)
A.氯化铵 B.硝酸钾 C.磷酸二氢铵 D.硫酸钾
(5)氮肥中的“氮”指的是____________。(填写字母)
A.单质 B.元素 C.原子 D.分子
NH4Cl NH4+ -3 NH4Cl +NaOHNaCl+ NH3↑+H2O NH4HCO3 NH3↑+ CO2↑+ H2O NH4HCO3+HCl=NH4Cl + CO2↑+ H2O BC B 【解析】(1)根据氯化铵中铵根显+1价,氯离子显-1价解答;(2)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多...查看答案和解析>>
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:填空题
(1)某学校中午的营养餐如下表所示:

①牛肉中富含的营养素主要是______;
②炒菜时使用铁强化酱油。人体中缺少铁元素,会导致________;
A.佝偻病 B.贫血 C.发育不良
③工业上利用赤铁矿炼铁的化学原理是________。(用化学方程式表示)
(2)国家能源局指出:到2020年,将在全国范围内推广使用车用乙醇汽油。利用农作物秸秆可生产乙醇(C2H6O),主要流程如下图所示:

①乙醇中含有____________种元素;
②发酵罐中,葡萄糖(C6H12O6)在酒化酶的催化作用下发生分解反应,生成乙醇和二氧化碳。其化学方程式为________;
③蒸馏塔中发生的是____________(填“物理”或“化学”)变化;
④分子筛的作用是吸附小于筛孔直径的_______(填“水分子”或 “乙醇分子”)。
蛋白质 B Fe2O3 + 3CO 高温 2Fe + 3CO2 3 C6H12O6 2C2H6O+ 2CO2↑ 物理 水分子 【解析】(1)①根据常见食品中含有的营养素分析回答;②根据缺铁会导致贫血解答;③根据一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳解答;(2)①根据乙醇的化学式分析解答;②根据葡萄糖在酒化酶的催化下分解生成乙醇和二氧化碳解答;③根据是否有新物质生成分析解答;④根据...查看答案和解析>>
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:简答题
钠是一种活泼金属,其原子的结构示意图为 。钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目:银白色有金属光泽。钠还能与水反应,生成氢氧化钠和氢气。1807年,科学家首次利用电解氢氧化钠的方法制备金属钠,同时得到氧气和水。1921年,科学家通过电解熔融氯化钠的方法制备金属钠同样获得成功。根据以上资料,回答下列问题:
。钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目:银白色有金属光泽。钠还能与水反应,生成氢氧化钠和氢气。1807年,科学家首次利用电解氢氧化钠的方法制备金属钠,同时得到氧气和水。1921年,科学家通过电解熔融氯化钠的方法制备金属钠同样获得成功。根据以上资料,回答下列问题:
(1)在钠的原子结构中,钠原子的质子数为________,最外层电子数为________;
(2)钠具有的物理性质有________(任写一点);
(3)钠与水反应的化学方程式为________;
(4)电解氢氧化钠和电解熔融氯化钠都属于基本反应类型中的________反应;
(5)实验室中的金属钠通常保存在煤油中的原因是________。(填写字母)
A.钠不与煤油反应 B.钠能与氧气反应
C.钠能与水反应 D.钠的密度比煤油的密度大
11 1; 银白色固体,有金属光泽,质软(任写一点); 2Na + 2H2O==2NaOH + H2↑ 分解 ABCD 【解析】(1)根据原子结构示意图分析解答;(2)根据题中信息分析解答;(3)根据钠与水反应,生成氢氧化钠和氢气解答;(4)根据反应特点分析解答;(5)根据钠的性质分析钠的保存方法。(1)在原子结构示意图中圆圈内的数字表示质子数,故钠原子的质子数为11,最外层电子数为1;(2...查看答案和解析>>
科目: 来源:江苏省高邮市2018届九年级第二次模拟考试化学试卷 题型:实验题
实验小组用下图装置进行实验。
已知:甲瓶中充满二氧化碳,乙中液体是水,实验前K关闭。

(1)图1装置甲中仪器a的名称____________;
(2)将装置甲中胶头滴管中的浓NaOH溶液挤入瓶中,振荡;打开装置甲中K,观察到乙中的现象是_____,原因是________;接着将装置甲仪器a中的稀盐酸注入甲中,观察到甲中有气泡产生,该反应的化学方程式为________。观察到乙中的现象是____________;
(3)为了充分证明二氧化碳与氢氧化钠能发生反应,某同学设计了图2所示的实验方案,则装置丁中X试剂含有的溶质为______和______(填化学式),装置丙的作用是______;
(4)实验过程中需配制100 g30%的NaOH溶液,需要水的质量是________ g。配制时需要用到的仪器 ____________。(填写字母)
A.托盘天平 B.胶头滴管 C.漏斗 D.量筒
分液漏斗 导管口有气泡冒出 甲中二氧化碳被消耗,导致瓶内压强减小,空气进入乙瓶中 Na2CO3+2HCl== 2NaCl + CO2↑+ H2O (或NaHCO3+HCl== NaCl + CO2↑+ H2O) 长玻璃管内液面上升 NaOH BaCl2 证明二氧化碳与氯化钡不能发生反应(或作对比) 70 ABD 【解析】(1)根据常见仪器解答;(2)根据氢氧化钠溶液与二氧化碳反应使甲内压强降...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com