
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:单选题
能正确反映我国早在西汉发现,宋初应用的湿法炼铜反应原理的是
A. 2CuO+C  2Cu+CO↑ B. Hg+CuCl2 =Cu+ HgCl2
2Cu+CO↑ B. Hg+CuCl2 =Cu+ HgCl2
C. 2Fe+3CuSO4=3Cu+Fe2(SO4)3 D. Fe+CuSO4=Cu+FeSO4
C 【解析】湿法炼铜反应原理指的是Fe+CuSO4===Cu+FeSO4,故选D。查看答案和解析>>
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:单选题
木炭在耐高温的容器中密封(内含空气)加热,下列各图中,能正确表示容器里所盛的物质总质量变化的是( )
A.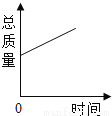 B.
B. C.
C. D.
D.
查看答案和解析>>
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:单选题
在硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,充分反应后,有少量金属析出,过滤后,向滤液中滴加稀盐酸,有白色沉淀析出,则析出的少量金属是
A. 铜 B. 银 C. 铁和铜 D. 铜和银
B 【解析】金属活动性顺序中,排在前面的金属能把排在后面的金属从其化合物的水溶液中置换出来,金属活动性差距越大,越易发生化学反应,所以首先发生的化学反应是:Fe+2AgNO3=2Ag+ Fe(NO3)2 ,当硝酸银溶液完全反应后,铁粉才与硝酸铜溶液反应,Fe+Cu(NO3)2==Fe(NO3)2+Cu。 向滤液中滴加稀盐酸,有白色沉淀析出,说明滤液中含有AgNO3溶液,则铁粉无剩余,铁...查看答案和解析>>
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:单选题
与碳酸钠、硫酸钠、硝酸镁三种溶液都能发生反应,且都有白色沉淀生成的是
A. 氯化钡溶液 B. 氢氧化钾溶液 C. 氯化钙溶液 D. 氢氧化钡溶液
D 【解析】A、氯化钡溶液不与硝酸镁溶液反应,不符合题意;B、氢氧化钾溶液不与碳酸钠溶液反应,不符合题意;C、氯化钙溶液不与硝酸镁溶液反应,不符合题意;D、氢氧化钡溶液与碳酸钠溶液反应生成碳酸钡白色沉淀、与硫酸钠溶液反应生成硫酸钡白色沉淀、与硝酸镁溶液生成氢氧化镁白色沉淀,符合题意。故选D。查看答案和解析>>
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:单选题
对物质的量的理解正确的是
A. 物质的量就是6.02?1023个微粒的集合体,单位是mol
B. 1molO3和1.5molO2含有相同数目的氧原子
C. 物质的量就是物质所含微粒的数量
D. 任何物质的摩尔质量就是它的相对原子质量或相对分子质量
B 【解析】A. 物质的量是一个物理量,它表示含有一定数目粒子的集合体,不一定是6.02?1023个微粒的集合体,表示物质所含微粒数与阿伏伽德罗常数之比,它是把微观粒子与宏观可称量物质联系起来的一种物理量,单位是mol,错误;B. 1molO3含有1mol×3=3mol氧原子,1.5molO2含有1.5mol×2=3mol氧原子,正确;C. 物质的量是一个物理量,表示物质所含微粒数与阿伏伽德...查看答案和解析>>
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:单选题
图1是甲、乙两种物质的溶解度曲线。20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到图2所示的现象。下列说法正确的是

A. 20℃时,乙溶液是饱和溶液
B. t℃后某一温度时,乙溶解度大于甲的溶解度
C. 升高温度可使两试管中甲、乙溶液的质量分数均增大
D. 从20℃降低到t℃时,甲、乙两物质的溶解度相等,溶质质量分数甲溶液比乙溶液小
B 【解析】A.20℃时,B试管中无乙物质剩余,乙溶液可能是饱和溶液,错误;B. A试管中有甲物质剩余,说明20℃时,甲的溶解度小于乙的溶解度,故b是甲,a是乙。 t℃后的某一温度时,乙的溶解度大于甲的溶解度,正确;C. 升高温度,甲、乙的溶解度增大,剩余的固体甲物质继续溶解,溶液的溶质质量分数增大,而乙物质没有固体继续溶解,升温后溶液的溶质质量分数不变,错误;D. 从20℃降低到t℃时,甲...查看答案和解析>>
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:单选题
某同学在学习酸的化学性质后,做了甲、乙二个实验,实验结束后,把甲乙试管中的废液依次缓慢倒入同一洁净的废液缸中,下列对废液缸中废液成分的分析正确的是
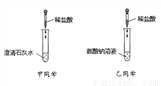
A. 废液中除氯化钠外,一定有氯化钙
B. 如果废液呈碱性,则一定有氢氧化钙
C. 如果废液呈酸性,则一定有氯化钙、氯化钠
D. 废液中一定有氯化钠,还有氢氧化钙或碳酸钠或盐酸中的一种物质
C 【解析】2HCl + Ca(OH)2 == CaCl2 + 2H2O,Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑。A. Na2CO3 + CaCl2 == CaCO3↓+ 2NaCl, Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH,废液中一定有氯化钠,不一定有氯化钙,错误;B. 澄清石灰水、碳酸钠溶液都显碱性,如果废液呈碱性,不一定有氢氧...查看答案和解析>>
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:简答题
化学与生活生产有这密切的联系,请用所学的化学知识回答下列问题。
(1)医疗上常用碘酒来消毒,其溶剂是_____;防毒面具的滤毒罐里盛放了一定量的活性炭,目的是用来除去有毒气体,这是利用活性炭的_____性。
(2)熟石灰、纯碱、天然气、硝酸钾、盐酸、硫酸 六种物质中,可用作改良土壤酸性的物质是_____;可作农作物肥料的是_____,检验该化肥可用_____反应,观察到的现象是_____。
(3)温室效应与大气中的二氧化碳含量增多有关。空气中二氧化碳增多的主要原因是_____;科学研究表明,在一定条件下可通过下述反应,将工业尾气中的CO2转化为一种重要的化工原料X:CO2+4H2 X+2H2O,则X的化学式为_____。
X+2H2O,则X的化学式为_____。
查看答案和解析>>
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:填空题
氯化钠和硫酸镁的溶解度曲线与若干温度下的溶解度表如下:
温度/℃ | 20 | 30 | 40 | 60 | 80 | 90 | 100 | |
溶解度 (g/100GH20) | NaCl | 36.0 | 36.3 | 36.6 | 37.3 | 38.4 | 39.0 | 39.8 |
MgSO4 | 33.7 | 38.9 | 44.5 | 54.6 | 55.8 | 52.9 | 50.4 |

请回答下列问题:
(1)80℃时,硫酸镁的溶解度为__________,溶解度曲线甲所代表的物质是__________。a点对应的温度t1范围是____________________。
(2)t2℃时有含有较多NaCl 的MgSO4溶液,为了得到纯净的MgSO4,可采用的方法__________
(3)40℃时把20g NaCl放入50g水中,形成的溶液中溶质质量分数为__________(精确到0.1%),要使t3℃饱和的MgSO4溶液中溶质质量分数增大,可采用的措施是__________。
55.8g 氯化钠 20°C<t1<30°C 降温结晶 过滤析出的晶体 洗涤、烘干 26.8% 适当降温并加入MgSO4固体 【解析】(1)由溶解度表可知,80℃时,硫酸镁的溶解度为55.8g,从溶解度曲线可知,甲所代表的物质溶解度随温度的升高而增大,故甲是氯化钠。a点表示在某一温度时,氯化钠与硫酸镁的溶解度相等,根据溶解度表可知,两种物质溶解度相等对应的温度范围是20°C<t1<30°C。...查看答案和解析>>
科目: 来源:上海市徐汇区2018届中考二模化学试卷 题型:科学探究题
有一包白色固体,可能含有碳酸钠、硫酸铜、硫酸钠、氯化钠等物质中的一种或几种。某化学兴趣小组为探究其成分做了以下实验:
实验步骤 | 实验现象 | 分析与结论(化学方程式) | |
1.取该固体样品溶于水 | 澄清无色溶液 | 一定不含有__________ | |
2.从步骤1中,取澄清无色溶液 | 向其中滴入氯化钡溶液 | 产生白色沉淀 | 固体中一定含有 ____________________ |
再加入足量稀硝酸 | 沉淀部分消失 | ||
3.从步骤1中,取澄清无色溶液 | 向溶液中滴加足量的硝酸钡溶液 | 产生白色沉淀 | 向溶液中滴加足量硝酸钡溶液的作用是__________。 写出滤液中滴加硝酸银后反应的化学方程式__________ |
过滤,在滤液中滴加硝酸银溶液 | 有白色沉淀产生 |
实验步骤3的目的是__________________________________________________。
CuSO4 Na2CO3和Na2SO4 将Na2CO3和Na2SO4除尽,防止对NaCl的检验造成干扰 AgNO3+NaCl→AgCl↓+NaNO3 检验原白色固体中是否含有NaCl 【解析】实验步骤:1.含Cu2+的溶液为蓝色。取该固体样品溶于水,得到澄清无色溶液,说明固体中无CuSO4。2. BaCl2 + Na2CO3 == BaCO3↓+ 2NaCl, BaCl2 + Na2S...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com