
科目: 来源:山东省2018届九年级模拟考试(二)化学试卷 题型:填空题
化学就在我们身边,根据有关信息回答下列问题。
(1)每100克巧克力中营养成分的含量如下表。
蛋白质/g | 脂肪/g | 糖类/g | 矿物质/mg | 维生素B/mg | 维生素C/mg | 总能量/千焦 | ||
钙 | 铁 | 磷 | ||||||
5 | 32 | 51 | 50 | 4 | 120 | 0.2 | ---- | 2142 |
①表中2142千焦能量全部来自糖吗?______________(填“是”或“不是”)。葡萄糖完全烧焦后得到黑色物质,说明葡萄糖含_________元素(填元素符号)。
②营养成分表中的“钙”是指 __________(填“元素”或“单质”),幼儿及青少年摄入量不足,会导致骨骼疏松,易得__________。铁、磷元素中属于人体必需微量元素的是_______。
③下列物质,富含糖类的是 ____________ (填序号)。
A.面粉 B.橄榄油 C.鸡蛋 D.白砂糖 E.牛奶
(2)汽水是常见的饮料,常用塑料瓶盛装,打开瓶盖汽水会自动喷出。
①汽水瓶的材质属于___________(填“金属”或“合成”)材料。
②打开汽水瓶盖时,汽水会自动喷出的原因是________________________________。
(3)①燃料电池是一种将化学反应产生的能源直接转化成电能的装置,下列燃料电池比较适合宇宙飞船上使用的是 ______________。(填序号)
A.O2——CH4燃料电池 B.O2——C2H5OH燃料电池
C.O2——H2燃料电池 D.O2——CO燃料电池
②煤燃烧时排放出的二氧化硫等污染物,有可能会导致降雨的酸性增强。我们把pH________5.6(填“>”“=”或“<”)的降雨称为酸雨。某电厂为防止环境污染,用石灰石浆来吸收二氧化硫,其反应的化学方程式为:2CaCO3 +2SO2+O2=2CaSO4+2X,则X的化学式为_____________。
不是 C 元素 佝偻病 铁 AD 合成 汽水中的气体的溶解度随压强减小而减小 C < CO2 【解析】(1)①糖类、油脂与蛋白质是人体的三大供能物质,所以表中2142千焦能量来自于糖类、油脂与蛋白质;葡萄糖(C6H12O6)中含有碳元素,所以完全烧焦后得到黑色物质; ②物质是由元素组成的,营养成分表中的“钙”是指钙元素;老年人缺钙易患骨质疏松症,青少年和幼儿缺钙易患佝偻病;铁属于人体所...查看答案和解析>>
科目: 来源:山东省2018届九年级模拟考试(二)化学试卷 题型:填空题
模型是联系宏观与微观的桥梁。
(1)图1是元素周期表中的一部分,图2 是溴原子的结构示意图。据图回答问题:
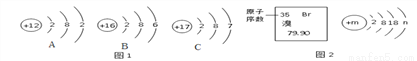
①图2中n的值为_________,溴元素与图1中_______(填字母)化学性质相似。
②写出溴和A形成化合物的化学式_________________。
(2)下图是氢分子和氧分子运动的示意图。

①在A、B、C中,能比较得出“温度越高,分子运动速率越快”是______(填标号)。
②从图中可见,影响分子运动速率的因素除温度外,还与 __________ 有关。
③举一个能说明“温度升高,分子运动速率加快”的生活事例:__________________ 。
(3)下图是某化学反应的微观示意图:已知:“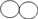 ”代表A分子,“
”代表A分子,“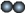 ”代表B分子,“
”代表B分子,“ ”代表C分子)
”代表C分子)

写出该反应的化学方程式_________________________ 。
7 C MgBr2 BC 分子种类 湿衣服在阳光下比在阴凉处干得快 A+3B==2C 【解析】(1)①由元素周期表的信息可知,溴的原子序数为35,即质子数为35,在原子中在,质子数=核外电子数,所以m=35,n=35-2-8-18=7;最外层电子数决定了元素的化学性质,溴原子的最外层有7个电子,C原子的最外层也为7个电子,二者化学性质相似; ②溴原子的最外层有7个电子,在化学反应中易得...查看答案和解析>>
科目: 来源:山东省2018届九年级模拟考试(二)化学试卷 题型:综合题
氮气在高温、高能量条件下可与某些物质发生反应。下图1是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题:
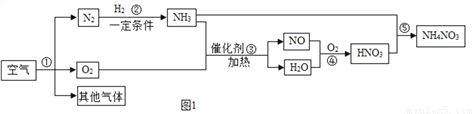
(1)步骤①中发生的是________变化(填“物理”或“化学”)。
(2)写出步骤③中发生反应的化学方程式_________________________________。
(3)在反应中有元素化合价变化的化学反应是氧化还原反应。其中元素的化合价升高的反应是氧化反应,在步骤④中,发生氧化反应的物质是 ______________________。
(4)在图1中所发生的化学反应,属于化合反应的有_______个。
(5)下图2是化肥硝酸铵包装袋上的部分说明,据图回答问题:

①硝酸铵要防潮防晒的原因____________________________。
②施用该类肥料时,要避免与碱性物质混合使用,写出硝酸铵与熟石灰反应的化学方程式____________
③图2标签所标注的“含氮量≥40%”是否合理_________(选填“是”或“否”)。
物理 4NH3+5O2 4NO+6H2O NO 3 硝酸铵易溶于水(或硝酸铵受热易分解) 2NH4NO3 +Ca(OH)2 === Ca (NO3)2 +2NH3↑+2H2O 否 【解析】(1)从空气中分离出原有的氮气和氧气是利用二者的沸点不同,没有产生新的物质,发生的是物理变化; (2)由题意可知,步骤③是氨气和氧气在催化剂加热的条件下生成一氧化氮和水,化学方程式为:4NH3+5O2...查看答案和解析>>
科目: 来源:山东省2018届九年级模拟考试(二)化学试卷 题型:科学探究题
某研究小组为探究“影响铁制品锈蚀快慢的因素”,取同浓度的稀氨水和稀醋酸用下图1装置完成表中实验,回答下列问题。
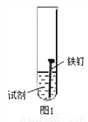
实验序号 | ① | ② | ③ | ④ |
实验温度/℃ | 25 | 25 | 70 | 70 |
试剂 | 稀氨水 | 稀醋酸 | 稀氨水 | 稀醋酸 |
出现铁锈 所需时间 | 1天未见锈蚀 | 5分钟 | 1天未见锈蚀 | 1分钟 |
(1)铁锈的主要成分是__________(填化学式)。
(2)实验②和④可探究_________ 因素对铁制品锈蚀快慢的因素;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是________(填实验序号)。
(3)根据表中实验现象得出的结论是 _____________(写出1 点即可)。
(4)影响铁制品锈蚀快慢除上述因素外,还有__________(写出1 点即可),请设计实验方案__________。
氧化铁( Fe2O3) 温度 ①②或③④ 相同的条件下,酸性试剂使铁制品容易生锈(相同的条件下,温度越高铁制品越容易生锈) 酸的浓度 相同条件下, 取两份不同浓度的醋酸分别在 25 摄氏度下观察铁钉的生锈时间 【解析】(1)铁锈的主要成分是氧化铁,氧化铁表示为Fe2O3;(2)实验②和④温度不同,其他条件完全相同,故探究的是温度对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,...查看答案和解析>>
科目: 来源:山东省2018届九年级模拟考试(二)化学试卷 题型:科学探究题
小英、小明在学完酸的化学性质后,做了如下图1的①--⑤个实验,
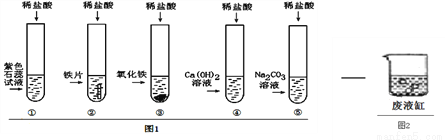
据图1回答下列问题:
(1)反应后试管②③中一定含有的阳离子分别是_______、_______(填离子符号)。
(2)实验④在反应时没有明显的实验现象。如何才能确定实验④反应的发生_______。
(3)写出实验⑤发生反应的化学方程式__________。从粒子的角度分析,此化学反应能发生的原因 _________。实验结束后,小英依次将试管④⑤的废液缓缓倒入同一洁净的废液缸中(如上图2),观察到废液缸先有气泡产生,后有白色沉淀生成。通过废液缸中出现现象,经过讨论确定,试管④⑤中废液含有的溶质分别是:试管④ ___________ 、试管⑤________________。
(4)小英将废液缸中物质进行过滤,得到白色沉淀和无色滤液。欲探究无色滤液中溶质的成分。小英分析得出无色滤液中一定不含HCl,理由是 _____________________。
(提出问题)过滤出的无色滤液中含有什么溶质?
(作出猜想) ①NaCl; ②NaCl和CaCl2; ③NaCl 、CaCl2和Na2CO3; ④NaCl和Na2CO3。小明认为猜想_________一定不正确。
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
小英取少量滤液于试管中,滴加少量碳酸钠溶液 | 无明显现象 | 猜想2不成立 |
小英取少量滤液于试管中,滴加少量_____溶液 | 有沉淀生成 | 猜想______ 成立 |
(表达与交流)两位同学确认了最终废液中溶质的成分。你认为处理该废液的方法是________。
Fe2+ Fe3+ 先向Ca(OH)2溶液中滴加几滴酚酞,溶液变红,再滴加稀盐酸 Na2CO3+2HCl =2 NaCl+ H2O+CO2↑ H+、CO32-结合生成水和CO2 CaCl2 HCl NaCl Na2CO3 因为白色沉淀是碳酸钙,如果有盐酸,它们会起反应 ③ 氯化钙 ④ 向最终废液中加入氯化钙溶液(或加入酸溶液)至中性后再倒掉废液 【解析】(1)反应后试管②中铁与盐酸反应生成氯...查看答案和解析>>
科目: 来源:山东省2018届九年级模拟考试(二)化学试卷 题型:综合题
某化学兴趣小组在做Fe和CuSO4溶液反应实验时,发现生成Cu的同时有气泡产生。为了进一步探究有气泡产生原因,做了如下实验:
①取8.5gFe粉放入一定量的CuSO4中,反应完成后,滤出固体,洗涤、干燥后称量,固体质量为9.2g。
②将该9.2g固体与一定质量分数的稀盐酸充分反应,消耗盐酸50.0g。根据实验绘制如图所示反应时间与反应产生氢气的质量关系图。

根据提供的有关数据进行下列计算和分析:
(1)根据图像可知,步骤②与稀盐酸反应的Fe的质量为_______。
(2)步骤①与CuSO4反应的Fe的质量为_______。
(3)步骤①与CuSO4反应的Fe的质量及步骤②与盐酸反应的Fe的质量之和______(选填“大于”、“小于”或“等于”)所取的Fe的质量8.5g。
(4)由上面实验的数据分析得出:Fe和CuSO4溶液反应,有气泡产生原因___________。
2.8g 5.6g < 因为少量的铁与硫酸铜溶液中的酸性物质发生了反应(硫酸铜溶液呈酸性,少量的铁与其反应 【解析】(l)【解析】 设与稀盐酸反应的Fe的质量为x,盐酸的质量为w Fe+2HCl═FeCl2+H2↑ 56 73 2 x w 0.10g 解之得:x=2.8g;w=3.65g; 答:与稀盐酸反应的Fe的质量...查看答案和解析>>
科目: 来源:山东省2018届九年级模拟考试(二)化学试卷 题型:计算题
工业上“侯氏”制碱法制得的纯碱产品中常含有少量的氯化钠。化验员对每批刚生产出的纯碱产品都要进行检测,标示出各种成分的含量后投放市场。在实验室中取22g该样品于烧杯中,加水将其溶解,然后逐滴加入溶质质量分数为10%的稀盐酸并不断振荡,首先发生的反应是:Na2CO3+HCl==NaHCO3+NaCl,然后发生的反应是:NaHCO3+HCl==NaCl+CO2↑+H2O。在上述过程中烧杯中溶液质量与加入稀盐酸质量的关系如图甲所示。
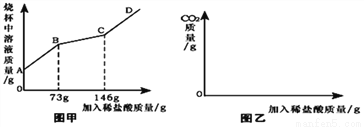
(1)请你根据图甲提供的信息,在图乙的坐标系中画出检测过程中产生CO2的质量随滴加盐酸质量的变化曲线(注意标明二氧化碳、盐酸质量的相应数值)。______________________
(2)计算出22g该样品中各成分的质量为______________。
纯碱Na2CO3 21.2g,NaCl 0.8g 【解析】(1)开始的45°夹角,说明加入的溶液的质量等于溶液质量增加量,说明过程中无气体或者沉淀产生.当加入73g稀盐酸时,开始放出气体二氧化碳;当稀盐酸的量达146g时,放出二氧化碳气体达最大值;以后再加稀盐酸,不再放出二氧化碳气体; 【解析】 设碳酸氢钠与盐酸反应得到的二氧化碳的质量为x.对应的生成二氧化碳消耗的盐酸的质量为146...查看答案和解析>>
科目: 来源:四川省广元市利州区2018届九年级中考模拟二诊化学试卷 题型:单选题
ClO2是生产饮用水的新一代消毒剂。从物质分类来看,ClO2属于( )
A. 氧化物 B. 酸 C. 碱 D. 盐
A 【解析】A、二氧化氯是由两种元素组成,其中一种是氧元素的化合物,属于氧化物,故A正确;B、二氧化氯不能电离出氢离子,不属于酸,故B错误;C、二氧化氯不能电离出氢氧根离子,不属于碱,故C错误;D、二氧化氯不能电离出金属离子和酸根离子,不属于盐,故D错误。故选A。查看答案和解析>>
科目: 来源:四川省广元市利州区2018届九年级中考模拟二诊化学试卷 题型:单选题
下列与人体健康有关的叙述正确的是( )
A. 工业用盐代替食盐烹调食物 B. 长期饮用蒸馏水不利于身体健康
C. 在饲料中掺入“瘦肉精”,可提高猪肉的瘦肉率 D. 只要胃液的pH<7人体就是健康的
B 【解析】A、工业用盐主要指亚硝酸盐,它有毒,不能烹调食物,所以错误;B、蒸馏水中无人体必需的营养素,长期饮用不利于健康,所以正确;C、在饲料中掺入“瘦肉精”,可提高猪肉的瘦肉率,人大量食用会影响健康,所以错误;D、胃液中有胃酸,它的pH应小于7,但是也不是随意数值,所以pH小于7就健康,所以错误。故选B。查看答案和解析>>
科目: 来源:四川省广元市利州区2018届九年级中考模拟二诊化学试卷 题型:单选题
六偏磷酸钠(Na6P6O18)常用于食品加工。六偏磷酸钠中磷元素的化合价为
A.-3 B.+2 C.+4 D.+5
D 【解析】根据在化合物中正负化合价代数和为零,(+1)×6+x×6+(-2)×18=0,则x=+5,故选D.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com