
科目: 来源:江苏省扬州市宝应县2018届九年级下学期中考二模考试化学试卷 题型:多选题
以钛铁矿(主要成分为 FeTiO3,同时含有少量的 Fe2O3、FeO等)为原料制 TiO2,再由 TiO2制金属 Ti 的工艺流程如下:

(查阅资料)①钛、镁在高温下与空气中的氧气、二氧化碳等反应。
②TiO2与氯气、焦炭在高温下按氯气和碳的质量比71:12参加反应。
下列说法错误的是
A. 生成硫酸铁的反应属于是置换反应
B. 操作2的名称是过滤;水解属于化学变化
C. 用金属镁和 TiCl4反应的方法制备Ti,氩气的作用是催化作用
D. TiO2与氯气、焦炭在高温下反应的化学方程式为:TiO2+2Cl2+2C TiCl4+2CO
TiCl4+2CO
查看答案和解析>>
科目: 来源:江苏省扬州市宝应县2018届九年级下学期中考二模考试化学试卷 题型:填空题
(化学语言包括符号语言、文字语言、图表语言等。
(1)用化学符号表示:
①镁元素_________; ②2个铝离子_________;
③硫酸亚铁_________; ④人体缺少_________元素会得佝偻病
(2)用下列字母符号填空
A.碳酸氢钠 B. 漂白粉 C. 生石灰 D.己烷
①_________可用作食品干燥剂 ②_________可用作焙制糕点的发酵粉
③_________可用作自来水的消毒剂 ④__________可用作提取大豆中油脂的溶剂
(3)写出下列反应的化学方程式
①铁在氧气中燃烧:___________ ;
②氯化铵与氢氧化钙混合加热:___________ ;
③碳酸钠与氢氧化钙溶液反应:___________ ;
④铁与硝酸银溶液反应:___________ 。
Mg 2Al3+ FeSO4 Ca C A B D 3Fe + 2O2 Fe3O4; 2NH4Cl+ Ca(OH)2 CaCl2+2H2O+2NH3↑; Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH; Fe+ 2AgNO3 == Fe (NO3)2 + 2Ag。 【解析】本题考查了常见化学用语的书写和常见物质的用途。书写时注意规范。 (1) ①镁元素符号是Mg;②...查看答案和解析>>
科目: 来源:江苏省扬州市宝应县2018届九年级下学期中考二模考试化学试卷 题型:简答题
化学在日常生活中有广泛应用
(1)根据如图衣服标签的部分说明回答下列问题:

①面料中的棉属于_______(填“天然”或“合成”,下同)有机高分子材料,面料中的涤纶属于________有机高分子材料,
②你知道聚酯纤维有下列哪三个优点____________(填序号)
A. 强度高、弹性好 B. 耐磨
C. 吸水性、透气性好 D. 耐化学腐蚀
(2)均衡的膳食结构可以保障身体健康。某种食品的配料标签如图所示:
该配料中富含蛋白质的物质是____________。从营养均衡的角度看,该食品中除水外,还缺少的营养素是____________。
(3)以下是我们日常生活中常用的清洗剂,其名称及有效成分如下表:
生活中的 用品 |
|
活氧彩漂 |
污渍爆炸盐 |
有效成分 | 盐酸 | 过氧化氢 | 过碳酸钠 |
①清除以下物质,可以使用洁厕灵的是____________(填字母序号)。
A. 铁锈 B. 水垢(主要成分为碳酸钙和氢氧化镁) C. 油渍
②“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(—O—O—)。据此推测,下列物质中,可用作杀菌消毒剂的是____________(填序号)。
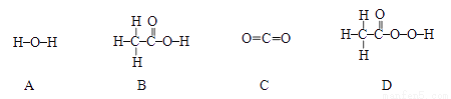
查看答案和解析>>
科目: 来源:江苏省扬州市宝应县2018届九年级下学期中考二模考试化学试卷 题型:简答题
金属元素有广泛的应用
(1) 不锈钢是生活中常用的合金,不锈钢的主要成分有铁、铬、镍。其中,铬的金属活动性与铁相近,常见化合价为+3、+6和+2,金属铬与硫酸反应生成呈蓝色的硫酸亚铬(CrSO4)溶液。回答以下与金属铬(Cr)相关的问题。
①铬+3价的氧化物化学式为____________。
②将铬片浸入稀硫酸中,充分反应,观察到的现象是____________;结合现象分析,反应前后溶液中减少的离子是____________(写离子符号);
(2) 如图是一款燃气灶的示意图:

①图示不锈钢面板属于______材料(填“金属”或“非金属”)。
②燃气灶所用燃气包括煤气、天然气、液化石油气等,天然气属于_______(填“可再生”或“不可再生”)能源,写出天然气的主要成分燃烧的化学方程式____________。
③熄灭燃气灶的方法是关闭阀门,其灭火的原理是____________。
(3) 铝合金材料在航空、航天、汽车、机械制造、船舶及化学工业中已大量应用。用铝土矿(含有Al2O3)与NaOH溶液反应可以得到NaAlO2,NaAlO2被CO2酸化生成Al(OH)3,Al(OH)3 受热分解生成Al2O3和H2O。
①铝合金材料属于____________。(填选项)
A.单质 B.化合物 C.纯净物 D.混合物
②Al2O3+2NaOH=2NaAlO2+____________。
③HAlO2读作偏铝酸,则NaAlO2读作____________。
④NaAlO2中铝元素的化合价为____________。
⑤Al(OH)3受热分解的化学方程式为____________。
⑥电解熔融的Al2O3可以制得Al和O2,其基本反应类型为____________。
Cr2O3 金属铬表面有气泡产生,溶液逐渐由无色变为蓝色 H+ 金属 不可再生, CH4+2O2CO2+2H2O 撤离可燃物 D H2O 偏铝酸钠 +3 2Al(OH)3 Al2O3+3H2O↑ 分解反应 【解析】本题主要考查了金属的化学性质,化学式的书写,甲烷的燃烧,物质的分类,质量守恒定律及其应用,有关元素化合价的计算,反应类型的判定,化学方程式的书写等。 (1)①铬的化合价为+3...查看答案和解析>>
科目: 来源:江苏省扬州市宝应县2018届九年级下学期中考二模考试化学试卷 题型:实验题
请结合下图回答问题:
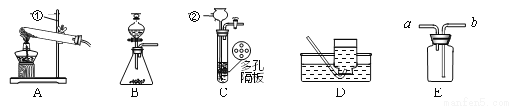
(1)仪器名称:①________,②______。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置______(选填序号)和D组合,反应的化学方程式为________,二氧化锰的作用是_______。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有__________。用E装置收集H2,气体应从________(选填“a”或“b”)端通入。
(4)有同学将实验室制得的CO2通入澄清石灰水,石灰水未变浑浊,于是作如右图探究:
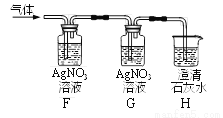
①实验室制CO2反应的化学方程式_________。
②装置F、H中溶液变浑浊,G中溶液不变浑浊,则原石灰水未变浑浊的原因是________。
铁架台 长颈漏斗 A 2KClO32KCl+3O2↑ 催化作用(催化、催化剂) 控制反应的发生和停止(或随开随用,随关随停) a CaCO3+2HCl=CaCl2+H2O+CO2↑ CO2中含有HCl(或使用了浓盐酸) 【解析】本题主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的除杂等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关...查看答案和解析>>
科目: 来源:江苏省扬州市宝应县2018届九年级下学期中考二模考试化学试卷 题型:科学探究题
某研究小组为探究“铁钉在不同溶液中腐蚀的速率”,在相同条件下取同浓度的下列不同溶液用如图装置完成实验,并用手持数据采集器进行测定。回答下列问题:

(1)铁锈的主要成分的化学式为____________
(2)在NH4Cl、(NH4)2SO4、和NH4NO3溶液中,铁钉锈蚀过程中上述溶液的酸性均变____________(填“强”或“弱”)
(3)上述实验方案是否合理?_________(填“合理”或“不合理”),你的理由是__________
(4) 该小组在不同酸碱性溶液中又进行了探究,在相同条件下其测定的实验数据如下图:

①上述实验中,氧气浓度下降先陡后缓的原因为________________
②根据甲、乙图像,可看出:铁钉在酸性溶液中比在中性溶液中生锈________(填“快”或“慢”, 下同);在开始时PH相同的情况下,甲、乙组中均为含氯离子的溶液生锈________ 。
Fe2O3 弱 不合理; 实验前溶液的PH没有保持相同 氧气浓度下降使腐蚀速率变慢。 快 快 【解析】本题主要考查了影响化学反应速率的因素探究,铁锈蚀的原理,溶液的酸碱性与pH值的关系。 (1)铁锈的主要成分是氧化铁,化学式为Fe2O3; (2)在NH4Cl、(NH4)2SO4、和NH4NO3溶液中,铁钉锈蚀过程中上述溶液的pH都在增大,酸性均变弱; (3)上述实验方案不合...查看答案和解析>>
科目: 来源:江苏省扬州市宝应县2018届九年级下学期中考二模考试化学试卷 题型:综合题
目前,全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
I、制备草酸镍(NiC2O4,其中Ni为+2价):
工业上用含镍合金废料(除镍外,还含有Fe、Cu、Ca、Mg、C等杂质)制取草酸镍。
(资料卡片1):
(1).过氧化氢(H2O2)俗称双氧水,是一种液体,受热易分解,可用于实验室制取氧气;过氧化氢能将+2价铁氧化为+3价铁。
(2).金属镍的化学性质类似于铁,与盐酸反应能生成氯化镍(NiCl2)。
根据下列工艺流程图回答问题:
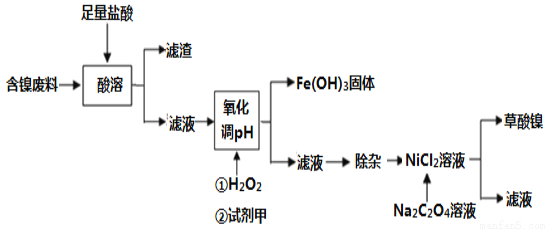
(1)酸溶之后的滤渣中含有的金属是____________(填化学式)。
(2)写出酸溶过程中Ni与盐酸反应的化学方程式____________。
(3)加H2O2时,温度不能太高,其原因是______________________,若H2O2在一开始酸溶时便与盐酸一起加入,则与原步骤酸溶过滤后的滤液相比,该滤液中会增加的金属离子是Cu2+和____________(写离子符号)。
(4)已知Na2C2O4溶液加入NiCl2溶液发生复分解反应,写出该反应的化学方程式_________。
II、镍粉制备:
工业用电解镍液(主要含NiSO4)制备碱式碳酸镍晶体xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉,过程如下:
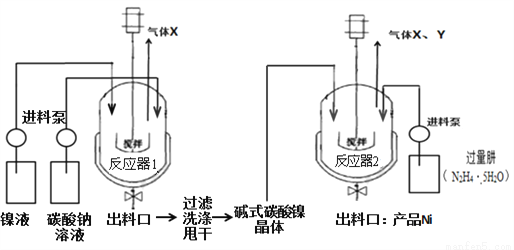
(5)反应器1中的一个重要反应为3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2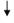 +3Na2SO4+2X,X的化学式为_______________。
+3Na2SO4+2X,X的化学式为_______________。
(6)反应器1的出料口获得的固体洗涤时,需用纯水洗涤,可以用来检验固体洗涤干净的试剂是_______________。
(7)反应器2中产生的气体Y是空气中含量最多的气体,该气体是________(填化学式)。
III、测定碱式碳酸镍晶体的组成:
测定碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)组成的实验方案及装置如下图:
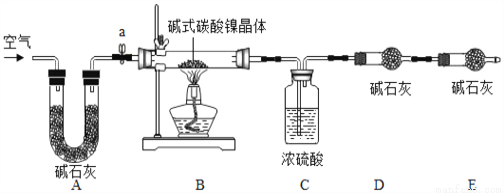
(资料卡片2):
碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(实验步骤):
①检查装置气密性;②准确称取3.77g碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)。
装置C/g | 装置D/g | 装置E/g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 201.08 | 180.44 | 180.00 |
(实验分析及数据处理):
(8)计算3.77g碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)中镍元素的质量_____g。(写出计算过程,精确到小数点后两位)
Cu Ni+2HCl=NiCl2+H2↑ 防止过氧化氢受热分解 Fe3+ Na2C2O4+ NiCl2=NiC2O4↓+ 2NaCl。 CO2 BaCl2 N2 1.77g 3.77g-1.08g-0.44g=2.25g (2.25g×59/75)×100%=1.77g 【解析】本题通过关于金属镍的探究,考查了金属活动顺序表的应用,复分解反应的应用,质量守恒定律的应用,硫酸根离子的检验,获得...查看答案和解析>>
科目: 来源:河北省二十一县(市、区)2018届九年级中考联合模拟理综化学试卷 题型:单选题
下列物质中富含蛋白质的是
A. 鸡蛋 B. 大白菜 C. 大米 D. 植物油
A 【解析】蛋白质主要存在于动物的肌肉组织中,其余存在于血液、皮肤、软组织、毛发、蹄、角中。另外,许多植物(如大豆、花生)的种子里也含富含蛋白质。大白菜富含植物纤维及维生素,大米富含糖类,植物油富含油脂,鸡蛋富含蛋白质。故选A。查看答案和解析>>
科目: 来源:河北省二十一县(市、区)2018届九年级中考联合模拟理综化学试卷 题型:单选题
下列做法正确的是
A. 用烧碱治疗胃病 B. 金刚石用来裁割玻璃
C. 用甲醛溶液浸泡海产品 D. 熟石灰可用来改良碱性土壤
B 【解析】A、烧碱是氢氧化钠,氢氧化钠具有强烈的腐蚀性,不能用用烧碱治疗胃病,错误;B、金刚石是天然存在硬度最大的物质,可以金刚石用来裁割玻璃,正确;C、甲醛会使蛋白质变质,所以不能用甲醛浸泡海产品,否则会使人中毒,错误;D、熟石灰显碱性,可用来改良酸性土壤,错误。故选B。查看答案和解析>>
科目: 来源:河北省二十一县(市、区)2018届九年级中考联合模拟理综化学试卷 题型:单选题
规范实验操作是实验成功的重要保证。如图所示化学实验操作不正确的是
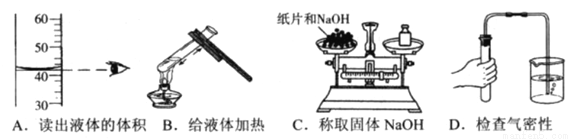
A. A B. B C. C D. D
C 【解析】A、读取液体体积,视线与液体的凹液面最低处保持水平,正确;B、给试管中的液体加热时,液体不能超过试管的 1/3 ,用外焰加热,试管夹夹在离管口 1/3 处,正确;C、氢氧化钠具有强烈的腐蚀性,为防止腐蚀托盘,不能放在纸上称量,应放在玻璃器皿中称量,错误;D、导管放入水中,用手握住试管,导管口有气泡冒出,装置气密性良好,正确。故选C。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com