
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:单选题
如图中甲—戊是初中化学常见物质。甲、戊为氧化物且甲为黑色固体,乙、丙分别是酸或碱中的一种。(图“—”表示相连的物质间可发生反应,“→”表示一种物质可转化为另一种物质,反应条件、部分反应物与生成物均已略去)。下列说法中不正确的是

A. 乙溶液能使紫色石蕊溶液变红 B. 丙溶液能与戊反应生成丁
C. 甲→戊只能通过置换反应实现 D. 不能由甲通过一步反应生成丁
C 【解析】甲、戊为氧化物且甲为黑色固体,甲能够转化为戊,因此甲可以是氧化铜,戊是二氧化碳;乙、丙分别是酸和碱中的一种,丁是大理石的主要成分,且氧化铜能够和乙反应,因此乙是酸,丁为碳酸钙,丙是碱-氢氧化钙,带入验证符合转化关系,因此:A、乙是酸,能使石蕊试液变成红色,正确;B、丙是氢氧化钙,戊是二氧化碳,氢氧化钙和二氧化碳反应产生碳酸钙沉淀和水,正确;C、氧化铜可以和碳、一氧化碳反应产生二氧...查看答案和解析>>
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:单选题
某氢氧化钠固体样品,可能含有固体氢氧化钾和不溶于酸的杂质A,取5.6g该样品与100g一定质量分数的稀盐酸反应,两者恰好完全反应,生成mg水。下列说法正确的是
A. 若样品不含任何杂质,则m < 1.8
B. 若m =1.8,则样品中一定含有杂质A,可能含有固体氢氧化钾
C. 若m =1.8,则样品中至少含有杂质A或固体氢氧化钾中的一种
D. 若样品中既含有A,也含有固体氢氧化钾,则一定m > 1.8
B 【解析】【解析】 假设5.6g全部为氢氧化钠,则设生成水的质量为x,盐酸溶质的质量为y NaOH+HCl═NaCl+H2O 40 36.5 18 5.6g y x 解得:x=2.52g y=5.11g 假设样品全部为氢氧化钾,则设生成水的质量为z KOH+HCl═KCl+H2O 56 ...查看答案和解析>>
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:填空题
化学用语是学习化学的重要工具,写出下列化学符号:
⑴ 三个亚铁离子__________;⑵ 金刚石__________;⑶ 由4个磷原子构成的磷分子_________;⑷ 碳铵_________;⑸ 地壳中含量最多的金属元素__________。
3Fe2+ C P4 NH4HCO3 Al 【解析】(1)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故三个亚铁离子可表示为:3Fe2+; (2)金刚石由碳原子直接构成,所以表示为:C; (3)表示分子中的原子个数的数字标在元素符号的右下角,故4个磷原子...查看答案和解析>>
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:填空题
化学物质在日常生活中有重要用途。请选择适当的物质填空(填字母):
A.氧气 B.干冰 C.熟石灰 D.小苏打 E.稀硫酸 F.尿素
⑴ 改良酸性土壤___________;⑵ 急救病人_________;⑶ 工业常用来除锈_________;⑷ 人工降雨_________;⑸ 焙制糕点__________。
C A E B D 【解析】(1)熟石灰显碱性,常用于改良酸性土壤; (2)氧气能供给呼吸,常用于急救病人; (3)铁锈主要成分是氧化铁,硫酸可与氧化铁反应生成硫酸铁和水,所以工业常用稀硫酸来除锈; (4)干冰即固态二氧化碳升华时会吸收周围环境的热量,可用于人工降雨; (5)小苏打即碳酸氢钠受热会分解放出二氧化碳,常用于焙制糕点。查看答案和解析>>
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:填空题
下图装置可以完成多个简单实验,具有药品用量少、实验现象明显、尾气不外逸等优点。
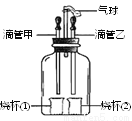
⑴ 若甲中吸有浓氨水,乙中吸有无色酚酞试液,将甲、乙中的液体同时挤出,一段时间后,观察到无色酚酞试液变红,说明分子具有的性质是_____________。
⑵ 若先将甲中的液体挤出,观察出气球明显鼓起,一段时间后恢复原状;再将乙中的液体挤出,气球又明显鼓起,过一会,略缩小,但不会恢复到原状。请将下表中的试剂补充完整。
滴管甲 | 烧杯① | 滴管乙 | 烧杯② | |
试剂 | H2O | ________ | _________ | Mg |
图示气球鼓起是因为装置内气压增大,第二次气压增大的原因是______________。
⑶ 若甲中吸有水,乙中吸有稀硫酸,烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠粉末。为了验证使石蕊变色的物质是碳酸而不是二氧化碳,应进行的实验操作是___________。
分子在不断的运动 氢氧化钠固体 稀盐酸 镁和盐酸反应生成气体且放热 先捏滴管乙,再捏滴管甲 【解析】(1)由于氨水和酚酞试液不在一个烧杯中,但酚酞试液变红了,说明氨水进入了酚酞试液中,氨水显碱性能使酚酞试液变红,所以说明了氨分子在不断运动,才运动到酚酞试液中的,所以说明分子在不断运动; (2)将甲中的液体挤出,观察到气球明显鼓起,由于甲中滴管是水,所以该物质溶于水放出热量,溶于水放热的...查看答案和解析>>
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:填空题
t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。

⑴ 烧杯②中的上层清液是否达到饱和状态?_______(填“是”“否”或“无法判断”)。
⑵ 烧杯①中溶解的溶质是________(写化学式)。
⑶ 将t1℃时硝酸钾的饱和溶液50g稀释成10%的溶液,需加水_________g。
⑷ 关于图1中烧杯内的物质,下列说法正确的是__________。
a.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
b.两烧杯同时蒸发少量的水,两烧杯中都一定有固体析出
c.将两烧杯中的溶液混合到一起,充分搅拌后,烧杯中一定还有剩余固体
d.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
是 KCl 50 ad 【解析】(1)烧杯②中有固体剩余,所以上层的清液达到饱和状态; (2)t1℃时,氯化钾的溶解度大于硝酸钾的溶解度,剩余烧杯①中溶解的溶质是氯化钾; (3)t1℃时硝酸钾的溶解度是25g,所以饱和溶液的溶质质量分数为:×100%=20%,所以将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水 -50g=50g; (4)a、等质量的固体溶解在10...查看答案和解析>>
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:综合题
下图装置常用于实验室制取常见的气体。

⑴ 仪器①的名称________。
⑵ 若用装置A和E制取氧气,写出相关的化学方程式______。验证氧气收满的方法_____。
⑶ 若实验室制取氢气,应选用的发生装置是_______(填字母,下同),该装置的特点是__________。 若用F装置收集氢气,气体应从________(填“a”或“b”)端导管导入。若用F装置除去一氧化碳气体中混有的二氧化碳气体,瓶中应盛放的试剂是________溶液(填化学式)。
⑷ 实验室常用石灰石和稀盐酸制取二氧化碳。现要制备二氧化碳8.8g,至少需要含碳酸钙80%的石灰石______克?
铁架台 2KClO3 2KCl+3O2↑ 有气泡从集气瓶口向外冒 B 控制反应的发生和停止 b NaOH 25g 【解析】(1)仪器①是铁架台; (2)若用装置A需要加热并且试管口没有棉团,适用于氯酸钾制氧气,化学方程式为2KClO3 2KCl+3O2↑;排水取气法收集时有气泡从集气瓶口向外冒说明已满; (3)制取氢气用稀硫酸和锌粒,是固体和液体不需要加热,发生装置选B.该装置的...查看答案和解析>>
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:实验题
小明利用图甲装置测定空气中氧气的体积分数,多次实验后,发现每次测得氧气的体积分数总是远小于21%,他认为误差主要是由实验装置造成,于是改用图乙装置进行实验,步骤如下:①连接装置并检查气密性,②在量筒内加入100mL水,③在集气瓶中加入少量水使瓶内空气体积为250mL,④在燃烧匙内放入过量的红磷,塞紧瓶塞,关闭止水夹,接通电源使电烙铁发热,点燃红磷后,断开电源。⑤燃烧结束,充分冷却后,打开止水夹,待量筒内水面不再下降时,记录量筒内水的体积为60mL。试回答:
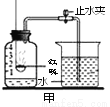
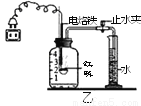
⑴ 若小明用图甲进行实验,写出检查装置气密性的方法:______________________。
⑵ 与装置甲相比,装置乙可以减小实验误差,其原因是____________。
⑶ 根据本实验数据,计算出空气中氧气的体积分数为_____________。
⑷ 小强同学按图1所示装置测定空气中氧气的含量,并用压强传感器实时地传回集气瓶内压强—时间关系图(该装置气密性良好,p0是集气瓶内初始气压,p和p’分别是反应结束后恢复到室温时集气瓶内的气压),下列说法正确的是_____________。
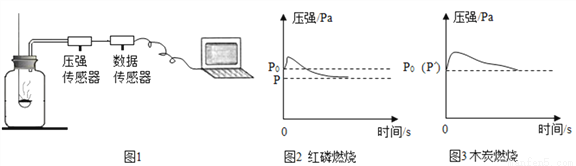
a.燃烧匙内所装红磷或木炭的多少对实验结果无影响
b.反应开始时集气瓶中压强瞬间变大是由燃烧放热造成的
c.p=0.79p0,p’= p0是因为红磷比木炭消耗的氧气多。
d.由图三可推出空气中氧气的含量
将导管一端插入水中,打开止水夹,双手紧握集气瓶外壁,导管口冒气泡,松手,导管中上升了一段液注,说明气密性好。 改进后的装置无需打开瓶塞点燃红磷,避免瓶内空气外逸造成实验误差。 16% b 【解析】(1)检验此装置的气密性时,可将导管一端插入水中,用手紧握广口瓶外壁,观察水中的导管口是否有气泡冒出,如果有气泡冒出,说明装置气密性好; (2)与装置甲相比,装置乙中使用电烙铁可以减小实验误差...查看答案和解析>>
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:流程题
某学习小组欲从高锰酸钾制氧气剩余物中回收副产物,设计了如图所示实验方案:
【资料卡片】
①KMnO4能和纤维素反应。,在中性溶液中比较稳定,加热碱性条件中的KMnO4溶液会有部分KMnO4和H2O反应,生成MnO2;
②锰酸钾溶于水为墨绿色,不稳定,在水溶液中能全部转化为KMnO4、MnO2和KOH,反应的化学方程式如下:3K2MnO4+2H2O==2KMnO4和+MnO2↓+4KOH
【实验方案】
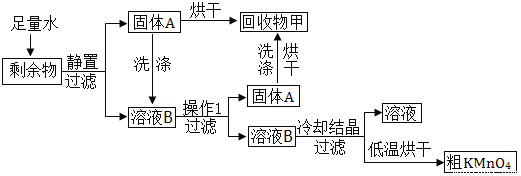
(1)将剩余物加入水中,观察到的现象是:①部分固体溶解;②有少量不溶物出现;③____________。
(2)回收物甲是____________________(填化学式)。
(3)静置后过滤时,发现滤液浑浊,在操作均正确的情况下(过滤前滤纸完好无损),原因是_______。
(4)滤液B中一定含有的溶质是KMnO4和_______________,需要加入少量硫酸进行中和,中和反应的化学方程式是____________________________________。
(5)冷却结晶后,低温烘干高锰酸钾晶体是为了防止_____________________。
(6)加热31.6gKMnO4使之完全分解,按以上实验方案可得回收物甲的质量可能是________。
A.8.7g B.11.5g C.12.8g D.28.4g
溶液由墨绿色变为紫红色 MnO2 KMnO4能和纤维素(滤纸)反应造成破损(不提反应,只写滤纸破损不给分) KOH H2SO4+2KOH=K2SO4+2H2O KMnO4受热分解 B 【解析】【资料卡片】①KMnO4能和纤维素反应。,在中性溶液中比较稳定,加热碱性条件中的KMnO4溶液会有部分KMnO4和H2O反应,生成MnO2;②锰酸钾溶于水为墨绿色,不稳定,在水溶液中能全部转化为KMnO...查看答案和解析>>
科目: 来源:江苏省常州市天宁分校2018届九年级第二次模拟考试化学试卷 题型:综合题
某食品包装袋中“双吸剂”标签如图所示:同学们对这包久置的“双吸剂”样品很感兴趣,设计下列实验进行探究。

(提出问题)久置的“双吸剂”固体的成分是什么?
(查阅资料)铁与氯化铁溶液在常温下反应生成氯化亚铁:Fe+2FeCl3=3FeCl2
(作出猜想)久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3。
(定性研究)小明取少量样品放入试管中,加入一定量的稀盐酸,发现:试管中固体质量逐渐减少,生成一种能使澄清石灰水变浑浊的气体,得到浅绿色溶液。他初步判断:样品中一定含有__________,一定不含Fe2O3。
(实验质疑)小组同学讨论认为上述实验并不能得出一定不含Fe2O3的结论,理由是 _____,_________(用化学方程式表示)。
为进一步确定这包久置的“双吸剂”固体的成分进行如下定量实验。
(定量研究)取3g样品研碎,并用磁铁充分吸收后,得到剩余固体2.6g,按照下列流程进行实验,请回答相关问题:

⑴ 操作二、操作三的名称是__________。
⑵ 固体I的成分是_________(填化学式,下同)
⑶ 写出生成固体II的化学方程式__________。
⑷ 依据定性、定量研究中现象的分析及有关数据计算判断,这包久置的“双吸剂”固体的成分中氧化钙的质量小于_____。
(实验反思)结合上面的实验,下列说法正确的是______(填字母序号)
a.对物质成分的研究有时需要定性和定量相结合
b.在原样品中加入足量盐酸有4个反应发生
c.定量研究烧杯C中的溶质为NaOH和Na2CO3
Fe和CaCO3 Fe2O3+6HCl═2FeCl3+3H2O Fe+2FeCl3=3FeCl2 过滤 CaCO3和Fe2O3 Ca(OH)2+Na2CO3═CaCO3↓+2NaOH 0.56 ac 【解析】【定性研究】由题目中可知固体成分可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3,由表中实验现象:“试管中固体逐渐减少,有大量无色气体产生,得到浅绿色溶液,澄清石灰水变浑浊。...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com