
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:单选题
钼是稀有矿产资源,主要用于航天合金材料制作。在元素周期表中钼元素的某些信息如图所示,下列有关钼的说法正确的是( )

A. 属于非金属元素 B. 元素符号为 MO
C. 相对原子质量为 95.94g D. 每个钼原子中有 138 个粒子
D 【解析】A、从汉字结构来看,钼字含有金字旁,是金属,错误; B、由两个字母组成的元素符号,第一个要大写,第二个要小写,错误; C、相对原子质量不能带g,错误; D、每个钼原子中含有42个质子,故含有42个电子,中子数=相对原子质量-质子数=54,故每个钼原子中共含有的原子数=42+42+54=138,故正确。故选D。查看答案和解析>>
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:单选题
我们国家现在已经全面禁止销售含磷洗涤剂。含磷洗涤剂中的 Na5P3O10会造成水体污染, 下列关于 Na5P3O10 叙述错误的是( )
A. Na5P3O10中钠元素、氧元素质量比为 23:32
B. Na5P3O10是由钠、磷、氧三种元素组成
C. Na5P3O10中含有 5 个氧分子
D. Na5P3O10中钠原子和氧原子的个数比为 1:2
C 【解析】A. Na5P3O10中钠元素、氧元素质量比为(23)::160=23:32,正确; B、由化学式可知,Na5P3O10是由钠、磷、氧三种元素组成,正确; C、Na5P3O10是纯净物,不含有氧分子,错误; D、由化学式可知,Na5P3O10中钠原子和氧原子的个数比为 1:2,正确。故选C。查看答案和解析>>
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:单选题
下列实验操作正确的是( )
A. 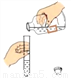 倾倒液体 B.
倾倒液体 B.  读取液体体积
读取液体体积
C.  熄灭酒精灯 D.
熄灭酒精灯 D. 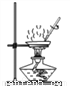 蒸发结晶
蒸发结晶
查看答案和解析>>
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:单选题
正确的是( )
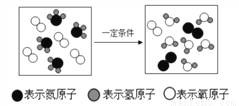
A. 反应物中包含两种化合物
B. 该反应属于化合反应
C. 该反应前后元素种类不变
D. 发生反应的分子个数比为 1:1
C 【解析】A、由微观示意图可知,反应中有两种化合物,分别是水和氨气,正确; B、该反应是由一种单质和一种化合物反应生成另一种单质和另一种化合物,故是置换反应,错误; C、任何化学反应前后元素的种类都不变,正确; D、由图可知3个氧气分子和4个氨气分子分生了反应,故分子个数比不是1:1,错误。故选C。查看答案和解析>>
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:单选题
下列关于物质的鉴别、除杂所选用的试剂或方法错误的是( )
选项 | 实验目的 | 试剂或方法 |
A | 鉴别羊毛衫的成分是羊毛还是涤纶 | 点燃闻气味 |
B | 除去 CO2 中含有的少量 CO | 点燃 |
C | 鉴别 NaOH、NH4NO3 两种固体 | 水 |
D | 除去 N2 中的少量 O2 | 将气体缓缓通过灼热的铜网 |
A. A B. B C. C D. D
B 【解析】A、羊毛是天然纤维,涤纶是合成纤维,点燃后,羊毛会出现焦羽毛味,而涤纶没有,正确; B、二氧化碳中含有少量的一氧化碳不能点燃,错误; C、氢氧化钠溶于水温度升高,硝酸铵溶于水温度降低,故可以鉴别,错误; D、氧气可以与灼热的铜网反应,而氮气不与铜网反应,故正确。故选B。查看答案和解析>>
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:单选题
下列四个图像分别与选项中的操作相对应,其中不合理的是( )
A.  向盐酸中滴加 NaOH 溶液
向盐酸中滴加 NaOH 溶液
B.  将水通电电解一段时间
将水通电电解一段时间
C.  加热 KClO3 和 MnO2 的混合物制取 O2
加热 KClO3 和 MnO2 的混合物制取 O2
D.  向一定量铁粉中加入稀盐酸
向一定量铁粉中加入稀盐酸
查看答案和解析>>
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:单选题
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )

A. 将甲、乙的饱和溶液从 t2℃分别降温 t1℃,析出晶体的质量甲一定大于乙
B. t1 时甲、乙的饱和溶液中溶质质量分数相等
C. t2 时将 60g 甲溶于 100g 水中,形成 160g 溶液
D. 将 M 点的甲溶液变成饱和溶液可以采用升高温度的方法
B 【解析】A、将甲、乙的饱和溶液从 t2℃分别降温 t1℃,析出晶体的质量与甲乙的饱和溶液的质量有关,甲不一定大于乙,当甲乙的饱和溶液的质量相等时 ,析出的甲一定大于乙,故错误; B、t1 时甲、乙两种物质的溶解度相等,故甲乙的饱和溶液中溶质质量分数相等,正确; C、由溶解度曲线可知,t2 时甲的溶解度是50g,故t2 时将 60g 甲溶于100g 水中,形成 溶液的质量为15...查看答案和解析>>
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:简答题
图是常见的干粉灭火器,请你根据所学知识回答下列问题。

(1)图中属于有机合成材料的是__________________________(写一种);
(2)除了铁表面涂油漆外,请你再提出一种防止铁制品锈蚀的方法___________________________________;
(3)在灭火器中同时使用了铁和铜两种材料,为了比较铁和铜的金属活动性,可以向硫酸 铜中加入_____,现象是_____;
(4)灭火器中使用的钢和纯铁相比优点是__________________________________________________ 。
塑料(或油漆) 使用后放在干燥的地方(合理即可) 铁丝 铁丝表面有红色固体析出,溶液由蓝色变为浅绿色 抗腐蚀性强或硬度大(合理即可) 【解析】(1)图中的塑料和油漆是有机合成材料; (2)防止铁制品锈蚀的方法有使用后放在干燥的地方、电镀等(合理即可) (3)比较铁和铜的金属活动性,可以向硫酸 铜中加入铁丝,现象是铁丝表面有红色固体析出,溶液由蓝色变为浅绿色; (4)灭火器中...查看答案和解析>>
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:实验题
下图是我们在化学学习中常见仪器和装置,请回答下列问题:
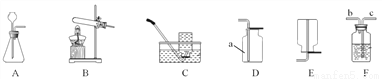
(1)D 中仪器 a 的名称是__________________;
(2)实验室用氯酸钾和二氧化锰制取氧气的化学方程式为______________________________________ ,选用 的发生装置为__________________(填装置编号,下同);若收集一瓶氧气,供铁丝在氧气中燃烧的实验使用,最好选择的收集装置为_______________________________ ;
(3)在实验室中需要收集一瓶干燥的氧气,可以将生成的气体连接 F 装置,F 装置中应该盛放的药品是_____,氧气应该从_____(填“b”或“c”)。
集气瓶 2KClO32KCl+3O2↑ B C 浓硫酸 C 【解析】(1)D 中仪器 a 的名称是集气瓶; (2)氯酸钾在二氧化锰作催化剂的条件下加热反应生成氯化钾和氧气,反应方程式为2KClO32KCl+3O2↑;该反应的反应物是固体,反应条件是加热,故选固固加热型装置B;收集氧气并做性质的验证实验时,要较纯净的氧气,故选排水法收集装置C; (3)干燥氧气用浓硫酸,为了让氧气与...查看答案和解析>>
科目: 来源:安徽省合肥市庐阳区2018届九年级质量调研检测(二)化学试卷 题型:流程题
某化学兴趣小组设计利用稀硫酸浸取某废弃的氧化铜锌矿制取活性氧化锌的方案(氧化铜锌矿主要成分为CuO和 ZnO,其余成分既不与酸反应,也不溶于水),部分实验流程如下:
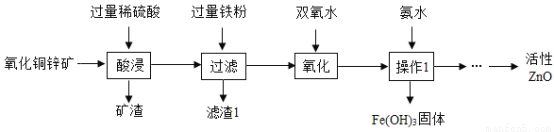
(1)将氧化铜锌矿粉碎的目的是_________,操作 1 的名称是_____,所用到的 玻璃仪器由玻璃棒、烧杯、_____;
(2)在氧化铜锌矿中加入稀硫酸要过量,其目的是_____,主要成分发生反应的化学方程式为______________________________________ (写出一个即可);
(3)得到滤渣 1 含有的金属是___________________________________________ 。
增大反应接触面积,使反应更充分 过滤 漏斗 使氧化铜、氧化锌充分反应 CuO+H2SO4=CuSO4+H2O (或 ZnO+H2SO4=ZnSO4+H2O) Fe 和 Cu 【解析】(1)在该实验操作中,将氧化铜锌矿粉碎的目的是增大反应接触面积,使反应更充分,操作 1 是固液分离的过程,故操作 1的名称是过滤,所用到的 玻璃仪器有玻璃棒、烧杯、漏斗; (2)在氧化铜锌矿中加入稀硫酸要过...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com