
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:单选题
下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是
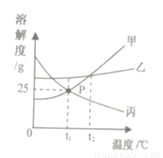
A. 甲的溶解度大于乙的溶解度
B. 降温可使接近饱和的丙溶液变为饱和溶液
C. 将t2°C甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数:乙>甲=丙
D. P点表示t1℃时甲、丙两种物质的溶解度都是25g
D 【解析】A、溶解度的大小与温度有关,错误; B、丙物质的溶解度随温度的升高而降低,故降温可以使接近饱和的丙溶液变为不饱和溶液,故错误; C、将t2°C甲、乙、丙的饱和溶液降温至t1℃,甲乙为饱和溶液,丙为不饱和溶液,故所得溶液的溶质质量分数大小关系为乙>甲>丙,故错误; D、P点表示t1℃时甲、丙两种物质的溶解度都是25g,正确。故选D。查看答案和解析>>
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:单选题
下列实验现象描述正确的是
A. 打开浓盐酸、浓硫酸的试剂瓶,瓶口都看到白雾
B. 铁丝在纯氧中燃烧,火星四射,生成黑色固体四氧化三铁
C. 实验室电解水,正负极产生的气体体积比约为2:1
D. 灼烧鸡蛋清,产生烧焦羽毛的特殊气味
D 【解析】A、浓盐酸有挥发性,而浓硫酸没有挥发性,故打开浓盐酸的瓶口有白雾现象,而浓硫酸没有,故错误; B、描述反应的现象时,不能说出生成物质的名称,故错误; C、电解水实验中正负极产生的气体体积比约为1:2,错误; D、灼烧鸡蛋清,产生烧焦羽毛的特殊气味,正确。故选D。查看答案和解析>>
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:单选题
下列选项中相关量的变化与图像不相符的是
选项 | X | Y |
|
A.向一定量饱和食盐水中加水 | 水的质量 | 溶质质量 | |
B.向一定量锌粒中加稀硫酸 | 稀硫酸质量 | 氢气质量 | |
C.向一定量CuCl2溶液中加NaOH溶液 | NaOH溶液质量 | 沉淀质量 | |
D.向一定量水中加KNO3晶体 | KNO3晶体质量 | 溶质质量分数 | |
A. A B. B C. C D. D
A 【解析】A.向一定量饱和食盐水中加水,溶质的质量不变,故错误; B、向一定量锌粒中加稀硫酸,锌与稀硫酸刚开始反应就有氢气生成,当锌反应完后,生成氢气的质量不变,正确; C、向一定量CuCl2溶液中加NaOH溶液,反应刚开始就有沉淀生成,当氯化铜反应完后沉淀的质量不再增加,正确; D、向一定量水中加KNO3晶体刚开始是纯水,故溶质的质量分数为0,随着硝酸钾的加入,溶质的质...查看答案和解析>>
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:单选题
下列实验方案设计合理的是
选项 | 实验目的 | 实验方案 |
A | 除去氢氧化钠溶液中少量碳酸钠 | 加过量的氢氧化钙溶液后过滤 |
B | 除去氧化钙中少量碳酸钙 | 加适量的稀盐酸 |
C | 鉴别硝酸钾和氯化铵固体 | 取样,分别与熟石灰混合研磨 |
D | 鉴别稀盐酸和氯化钠溶液 | 取样,分別滴加硝酸银溶液 |
A. A B. B C. C D. D
C 【解析】A、加入过量的氢氧化钙会引入氢氧化钙杂质,故错误; B、稀盐酸与氧化钙和碳酸钙都反应,故错误; C、氨态氮肥遇到碱性物质会有刺激性气味的气体生成,故可以鉴别,正确; D、稀盐酸和氯化钠中都含有氯离子,故都有白色沉淀生成,故不能鉴别,故错误。故选C。查看答案和解析>>
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:简答题
联系已学的化学知识,回答下列问题。
(1)空气中能供给呼吸的气体是_________________;
(2)熄灭酒精灯用灯帽盖灭,其灭火原理是_______________。
(3)标出水中氢元素的化合价_____________。
(4)铁制容器不能盛放硫酸铜溶液的原因_______________(用化学方程式表示)。
O2 隔绝氧气 Fe+CuSO4=Cu+FeSO4 【解析】(1)空气中能供给呼吸的气体是O2; (2)熄灭酒精灯用灯帽盖灭,其灭火原理是隔绝氧气。 (3)标出水中氢元素的化合价2O; (4)铁制容器不能盛放硫酸铜溶液的原因铁与硫酸铜反应生成铁和硫酸亚铁,反应方程式为Fe+CuSO4=Cu+FeSO4查看答案和解析>>
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:填空题
在宏观、微观和符号之间建立联系是化学学科的特点。下图是某物质发生反应的微观示意图。
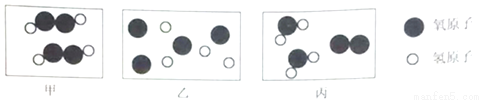
(1)丙图中所示物质都是由__________构成的(选填“分子”“ 原子”或“离子”);
(2)结合上图分析,化学变化中最小的粒子是______________;
(3)画出氧原子的结构示意图_______________;
(④)甲图所表示的意义是___________(用化学用语表示)。
分子 原子 2H2O2 【解析】(1)丙图中的分子是水分子和氧气分子,他们都是由氧气分子构成; (2)由图可知化学变化中的最小粒子是原子; (3)氧原子的结构示意图是; (4)甲图表示的是2个过氧化氢分子,表示为2H2O2;查看答案和解析>>
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:流程题
海洋是人类巨大的资源宝库,下图为从海水中提取金属镁的简易流程图。

(1)海洋中含量最多的物质是______________;
(2)实验室中进行操作1时,玻璃棒的作用是______________;
(3)生石灰转化为石灰乳的过程是___________反应(选填“吸热”或“放热”);
(4)上述流程中未涉及到的基本反应类型是____________反应。
H2O 引流 放热 置换反应 【解析】(1)海洋中含量最多的物质是水; (2)操作1是蒸发过程,该操作中玻璃棒的作用是引流; (3)氧化钙与水反应生成氢氧化钙,该反应是放热反应; (4)该过程中没有单质的生成与参加反应,故一定没有置换反应;查看答案和解析>>
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:实验题
某同学设计了如下图所示的装置,用于实验室制取CO2,并对它的部分性质进行探究,按要求回答问题。

(1)A装置用于制取CO2,反应的化学方程式为___________________。
(2)用B装置收集CO2,气体应从___________(选填“a”或“b”)端通入;
(3)若要C中的两个气球悬浮在空气中,则气体甲可能是_________(填序号);
A.氢气 B.氧气 C.空气
(4)往D试管中通入CO2,当出现__________现象,表示石灰水中的溶质恰好完全沉淀;
(5)E装置的集气瓶中充满CO2,打开分液漏斗①,滴入少量NaOH浓溶液,气球明显胀大,写出发生反应的化学方程式__________;若要气球恢复原状,应关闭分液漏斗①,打开分液漏斗②,滴入___________溶液(填化学式,忽略滴入液体体积)。
CaCO3+2HCl=CaCl2+H2O+CO2↑ a A 溶液红色刚好消失 CO2+2NaOH= Na2CO3+H2O HCl/H2SO4 【解析】(1)该装置用碳酸钙和稀盐酸制取二氧化碳,碳酸钙与稀盐酸反应生成氯化钙、二氧化碳气体和水,反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑; (2)b装置是多功能装置,此处改装为向上排空气法收集二氧化碳,故气体从a管通入; ...查看答案和解析>>
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:科学探究题
实验课上,老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种, 为确定该粉末的成分,同学们进行了如下探究,请你参与其中并回答问题。
[提出猜想]甲组:铜粉;乙组:氧化铁粉末;丙组:____________________。
[设计实验]
方案1:取少量红色粉末放入试管中,滴加足量的___________(从下列试剂中选择:氯化钠溶液、稀盐酸、氢氧化钠溶液)振荡,若甲组猜想正确,则实验现象为__________________。
方案2:取8g红色粉末放入硬质玻璃管中,先通入CO,然后用酒精喷灯加热一段时间(实验装置如图1所示),停止加热并继续通入CO至装置冷却。
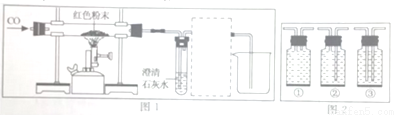
若乙组或丙组猜想正确,则硬质玻璃管内发生反应的化学方程式是____________。
实验时要先通CO再加热的目的是______________________。
[数据处理]
等装置完全冷却到室温,称量硬质玻璃管内剩余固体质量为mg。若乙组猜想正确,则m的取值范围是________________。
[实验反思]
图1虚线框内的装置是用于吸收CO2;并收集CO,请从图2(广口瓶内均为氢氧化钠溶液)中选择最合适的装置______________(填序号)。
铜粉和氧化铁粉末 稀盐酸 无明显现象 3CO+Fe2O32Fe+3CO2 排尽硬质玻璃内空气,防止爆炸 5.6≤m<8 ③ 【解析】(1)丙的猜想可能是氧化铁和铜粉; (2)铜不与酸反应,故可加入稀盐酸,如固体不溶解,则说明只有铜,猜想甲正确; (3)硬质玻璃管内是一氧化碳与氧化铁在高温的条件下反应生成铁和二氧化碳,反应方程式为3CO+Fe2O32Fe+3CO2 ;实验时要先通...查看答案和解析>>
科目: 来源:江苏省宿迁市2018年中考化学试卷 题型:计算题
某硫酸厂欲测定排放的废水中硫酸的质量分数(假设废水中只含硫酸一一种溶质),取废水样品200g,逐滴加入溶质质量分数为5%的氢氧化钠溶液,废水中硫酸的质量随加入氢氧化钠溶液质量变化如下图所示,

(1)要配制100g 5%的氢氧化钠溶液,需氢氧化钠固体质量为___________g;
(2)计算该废水中硫酸的质量分数为_____________(写出计算过程)。
5 2.45% 【解析】(1)要配制100g5%的氢氧化钠溶液,需氢氧化钠固体质量为100g5%=5g (2)设200g废水中硫酸的质量为x 2NaOH + H2SO4= 2H2O+ Na2SO4 80 98 80g x = ,解得x=4.9g 该废水中硫酸的质量分数为=2.45%查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com