
科目: 来源:湖北省武汉市2018年中考化学试卷 题型:计算题
某氯化钠样品中含有氯化镁。为测定其中氯化钠的质量分数,称量5.00g样品于烧杯中,加适量水完全溶解,然后逐滴加入氢氧化钠溶液至恰好完全反应,生成0.58g沉淀。请回答下列问题:
(1)氢氧化钠溶液可使紫色石蕊溶液变成_____色。
(2)计算该样品中氯化钠的质量分数为____________。
蓝 81% 【解析】(1)根据氢氧化钠溶液显碱性能使紫色石蕊溶液变蓝解答;(2)根据反应的化学方程式计算出氯化镁的质量,然后再计算氯化钠的质量及质量分数。(1)氢氧化钠溶液可使紫色石蕊溶液变成蓝色;(2)设样品中氯化镁的质量为x。 MgCl2+2NaOH=Mg(OH)2↓+2NaCl 95 58 x 0.58g x=0.95g 样品中氯化钠的质量为5.00g-0...查看答案和解析>>
科目: 来源:浙江省温州市2018年中考科学(化学部分)试卷 题型:单选题
“柴、米、油、盐”是厨房常备用品其主要成分属于无机物的是
A. 柴(纤维素) B. 米(淀粉) C. 油(脂肪) D. 盐(氯化钠)
D 【解析】属于无机物的是盐(氯化钠),柴(纤维素)、米(淀粉)、油(脂肪)均属于有机物。故选D。查看答案和解析>>
科目: 来源:浙江省温州市2018年中考科学(化学部分)试卷 题型:单选题
雷雨天气时,氮气可逐步转化为硝酸盐,其关键反应为:N2+O2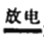 2NO。该反应属于
2NO。该反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
A 【解析】N2+O2 2NO,该反应属于化合反应,反应物是两种物质,生成物是一种物质。 点睛∶化合反应的特征是多变一。查看答案和解析>>
科目: 来源:浙江省温州市2018年中考科学(化学部分)试卷 题型:单选题
茶叶中含有茶氨酸(C7H14O3N2),茶氨酸中各元素质量分数如图所示。其中①表示的元素是

A. 碳 B. 氢 C. 氧 D. 氮
A 【解析】茶氨酸(C7H14O3N2),茶氨酸中各元素质量比为12×7∶14∶16×3∶14×2=42∶7∶24∶14,①表示的元素是碳。故选A。 点睛∶根据物质的化学式可以确定化合物中各元素的质量分数。查看答案和解析>>
科目: 来源:浙江省温州市2018年中考科学(化学部分)试卷 题型:单选题
某“天气瓶”通过樟脑在酒精溶液中的结晶情况反映气温变化。如图为该“天气瓶”在三种不同气温下的状况,则瓶内溶液一定为相应气温下樟脑饱和溶液的是
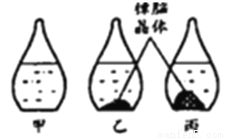
A. 甲、乙 B. 甲、丙 C. 乙、丙 D. 甲、乙、丙
C 【解析】瓶内溶液一定为相应气温下樟脑饱和溶液的是乙和丙,均有未溶解的晶体。故选C。 点睛∶判断溶液是否饱和的方法是看溶液中是否有未溶解的晶体,如果有未溶解的晶体,溶液一定是饱和溶液。查看答案和解析>>
科目: 来源:浙江省温州市2018年中考科学(化学部分)试卷 题型:单选题
根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是
A. 用铁制容器盛盐酸 B. 用铜制容器盛盐酸
C. 用铁制容器盛硝酸银溶液 D. 用铜制容器盛硝酸银溶液
B 【解析】A、用铁制容器盛盐酸,铁属于比较活泼的金属,排在氢前面,与盐酸反应; B、用铜制容器盛盐酸,铜排在氢后面,与盐酸不反应;C、用铁制容器盛硝酸银溶液,铁比银活泼,铁与硝酸银溶液反应;D、用铜制容器盛硝酸银溶液,铜比银活泼,铜与硝酸银溶液反应。 点睛∶金属活动顺序表的应用⑴排在氢前面的金属可以与稀硫酸或盐酸反应置换出氢气,排在氢后面的金属则不能⑵排在前面金属可以把排在其后面的金...查看答案和解析>>
科目: 来源:浙江省温州市2018年中考科学(化学部分)试卷 题型:填空题
我国用新技术提纯了稀有金属铼(Re),为航空航天发动机核心部件的制造提供了重要原料.
(1)铼原子的相对原子质量为186,原子核内有75个质子,则其核外电子数为_____。
(2)高铼酸钠(NaReO4)是铼的重要来源之一,高铼酸钠中铼元素的化合价为_____。
75 +7 【解析】(1)铼原子的相对原子质量为186,原子核内有75个质子,则其核外电子数为75,原子核内质子数等于核外电子数。(2)高铼酸钠(NaReO4),高铼酸钠中铼元素的化合价为∶根据化合物中正负化合价代数和为零原则,﹙+1﹚+x+﹙-2﹚×4=0,x=+7。 点睛∶原子核内质子数等于核外电子数,化合物中正负化合价代数和为零。查看答案和解析>>
科目: 来源:浙江省温州市2018年中考科学(化学部分)试卷 题型:填空题
人类发现二氧化碳经历了多个世纪,下列是其历程中的部分资料。
资料一:1630年,海尔蒙特发现在一些洞穴处,有一种能使燃着的蜡烛熄灭的气体,后来被证实是CO2.
资料二:1754年,布菜克将石灰石煅烧首次制得CO2,并完成了如下所示的物质转化研究。
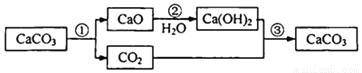
资料三:1766年,卡文迪许通过实验测得.室温下1体积水大约能溶解1体积二氧化碳气体.
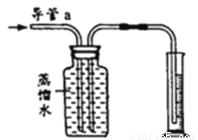
(1)根据海尔蒙特的发现,可推测二氧化碳的化学性质:_________。
(2)写出布莱克实验中反应③的化学方程式:________。
(3)如图,在室温下将容积为200毫升的广口瓶注满蒸馏水,通过导管a缓慢通入300毫升CO2。如果卡文迪许的结论是正确的,则在量简中收集到的水约为________毫升。
不燃烧也不支持燃烧, CO2 + Ca(OH)2 == CaCO3 ↓+ H2O 100 【解析】(1)根据海尔蒙特的发现,可推测二氧化碳的化学性质是不燃烧也不支持燃烧,能使燃着的蜡烛熄灭。(2)布莱克实验中反应③的化学方程式是CO2+Ca(OH)2 =CaCO3↓+H2O。(3) 在室温下将容积为200毫升的广口瓶注满蒸馏水,通过导管a缓慢通入300毫升CO2。按卡文迪许的结论,则在量简中...查看答案和解析>>
科目: 来源:浙江省温州市2018年中考科学(化学部分)试卷 题型:填空题
二氧化锰和过氧化氢酶均能催化过氧化氢分解制取氧气。为比较两者的催化能力,小明按图甲所示装置进行了如下实验。

①取1. 5毫克过氧化氢酶和8毫升蒸馏水加入容器中,搅拌后塞紧橡皮塞。
②用注射器A从容器中抽出2毫升气体,用注射器B将2毫升H2O2溶液注入容器中,采集数据.直至反应结束。
③用3.1毫克、3.6毫克过氧化氢酶及1.5毫克、5.6毫克、10. 7毫克二氧化锰重复上述实验,获取数据如图乙。
(1)步骤②将注射器B中的2mL H2O2溶液全部注入容器前,用注射器A先从容器中抽出2毫升气体,其目的是__________。
(2)小明分析相关数据,得出“过氧化氢酶对过氧化氢的催化能力比二氧化锰强”这一结论,其依据是_____________。
(3)查阅资料得知:过氧化氢分解为放热反应。小明推测:过氧化氢酶质量过大,可能导致实验过程中过氧化氢分解突然变慢。请说明其理由:___________。
使加入反应物后瓶内的初始气压与原气压相同 相等质量的催化剂使相等质量的过氧化氢达到相同气压,过氧化氢酶所需的时间更短 过氧化氢酶的质量过大,可能导致反应过快,温度过高,降低了酶的活性 【解析】根据所学知识和题中信息知,(1)步骤②将注射器B中的2mL H2O2溶液全部注入容器前,用注射器A先从容器中抽出2毫升气体,其目的是使加入反应物后瓶内的初始气压与原气压相同。(2)分析相关数据,得出“过...查看答案和解析>>
科目: 来源:浙江省温州市2018年中考科学(化学部分)试卷 题型:填空题
海螵蛸是一味中药,其主要成分是碳酸钙,某同学利用如图装置测定其中碳酸钙的含量。

①在锥形瓶中加入质量为m的海螵蛸粉末,向分液漏斗中加入稀盐酸。在烧杯中加人足量氢氧化钠溶液,并称量烧杯及氢氧化钠溶液总质量m1
②先打开止水夹,再打开分液漏斗活塞,滴加盐酸并及时关闭活塞。完全反应后,再次称量烧杯及其中液体的总质量m2.
③利用m2与m1的差值,即反应生成的二氧化碳质量,再计算海螵蛸中碳酸钙的含量。
(1)海螵蛸具有治疗胃酸过多、能为骨质发育提供重要元素的功效,其原因是___________。
(2)实验前要检查装置的气密性,方法是:用止水夹夹住橡胶管,往分液漏斗中加入适量水。打开分液漏斗的活塞.观察到_______,说明装置气密性 良好。
(3)下列情况会导致海螵蛸中碳酸钙质量分数测量值偏小的是______(可多选)。
A.海螵蛸中滴加盐酸过量
B,锥形瓶内部分水蒸气随二氧化碳逸出
C.反应结束后,锥形瓶内有二氧化碳残留
D.反应速度过快,大量气泡从氢氧化钠溶液中溢出
海螵蛸中的碳酸钙能与胃液中的盐酸反应,同时为人体提供钙元素; 分液漏斗内液面不再下降 CD 【解析】(1)海螵蛸具有治疗胃酸过多、能为骨质发育提供重要元素的功效,其原因是海螵蛸中的碳酸钙能与胃液中的盐酸反应,同时为人体提供钙元素。(2)实验前要检查装置的气密性,方法是:用止水夹夹住橡胶管,往分液漏斗中加入适量水。打开分液漏斗的活塞.观察到分液漏斗内液面不再下降,说明装置气密性良好。(3)导致...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com