
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:单选题
纳米铁粉在空气中能自燃并生成一种红色氧化物。对比铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧的事实,某同学得出的下列结论不正确的是
A. 纳米铁粉在空气中自燃的产物不是四氧化三铁
B. 相同的反应物在不同条件下生成物可能不同
C. 有些物质燃烧时温度不需要达到着火点
D. 反应物间的接触面积大小是反应能否发生的因素之一
C 【解析】 A、纳米铁粉在空气中自燃生成一种红色氧化物,四氧化三铁是黑色的固体,纳米铁粉在空气中自燃的产物不是四氧化三铁,正确;B、纳米铁粉在空气中能自燃生成氧化铁,铁在氧气中燃烧生成四氧化三铁。相同的反应物在不同条件下生成物可能不同,正确;C、物质燃烧时温度需要达到着火点,错误;D、根据“纳米铁粉在空气中能自燃并生成一种红色氧化物。对比铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧的事...查看答案和解析>>
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:单选题
常温下向一定质量的稀盐酸中逐渐加入镁条,充分反应(忽略挥发)。下列图像正确的是
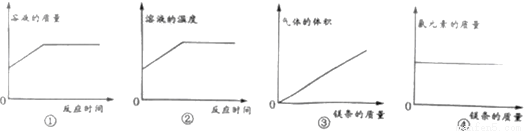
A. ①② B. ②③ C. ①④ D. ②④
C 【解析】①常温下向一定质量的稀盐酸中逐渐加入镁条,镁与盐酸反应生成氯化镁和氢气,每24份质量的镁能置换出2份质量的氢气,溶液的质量不断增加,盐酸反应结束,溶液的质量不再增大,正确;②金属与酸的反应是放热反应,溶液的温度逐渐升高,当反应结束后,温度下降,会恢复到原温度,错误;③镁与盐酸反应生成氯化镁和氢气,反应过程中气体的体积不断增加,盐酸反应结束,气体的体积不再增大,气体的体积不会一直增...查看答案和解析>>
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:简答题
江西海昏侯墓考古发掘出大量金器、竹简、玉器和青铜器。某些玉器含有Al2O3,Al2O3中铝元素显+3价,青铜器上的铜锈可用酸洗,清洗后的溶液中含有铜离子。
(1)用化学用语表示上面加点的文字为___________和___________。
(2)在下列几种物质中,属于合成材料的是___________(填序号)。
A.竹简 B.棉花 C.塑料 D.青铜
(3)黄金化学性质十分稳定,其外观与铜相似,常用灼烧的方法来鉴别它们,鉴别过程的化学反应方程式为________________。
Cu2+ C 2Cu+O22CuO 【解析】本题考查了常见化学用语的写法、材料的分类以及化学方程式的书写。书写时注意规范。 (1)元素化合价的表示方法是确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,氧化铝中铝元素显+3价,可表示为;离子的表示方法是在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后...查看答案和解析>>
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:简答题
新能源汽车的研发和使用是时代发展的需要。
(1)下列能源不属于新能源的是___________(填序号)。
A.氢能 B.核能 C.石油 D.风能
(2)锂电池可为新能源汽车提供动力,下列结构示意图表示的粒子与锂原子的化学性质最为相似的是___________(填序号)。

(3)锂(Li)的金属活泼性强于铝,它与稀硫酸反应的化学方程式为______________,新能源汽车除了节约化石能源外,其主要优点是__________________。
C B 2Li+H2SO4=Li2SO4+H2↑ 无污染 【解析】本题考查了资源综合利用和新能源开发,金属的化学性质,核外电子在化学反应中的作用,化学方程式的书写等。 (1)人们正在利用和开发的新能源有氢能、太阳能、核能、风能、地热能、潮汐能、生物质能等,石油属于化石燃料,不属于新能源。故选C; (2)元素的性质,特别是元素的化学性质是由该原子最外层电子数决定的。锂原子的最外层有...查看答案和解析>>
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:简答题
将80g M物质加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如右图所示,按要求填空。
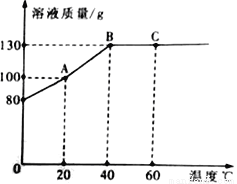
(1)A点时,该溶液的溶质质量分数为_______________________。
(2)A、B、C三点所对应的溶液,属于不饱和溶液的是__________________(填字母)。
(3)在40℃时,M物质的溶解度为___________g,若保持溶剂的质量不变,从C点对应的溶液获得M的晶体,可以采用的方法是_______________________。
50% C 160 降温结晶 【解析】本题考查了固体溶解度,结晶的方法,饱和溶液与不饱和溶液的判定,溶质的质量分数计算等。 (1)根据溶液的质量随温度的变化曲线可知,A点时,该溶液的质量为100g,溶液中的M质量为(100 g-50g)=50g,该溶液的溶质质量分数=×100%=50%; (2)A点对应的溶液随温度的升高溶液的质量不断增大,A点对应的溶液中存在未溶解的M,A点对应...查看答案和解析>>
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:推断题
某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如下图所示。

(1)固体A与某酸反应的化学方程式为____________。操作②时,当__________即可停止加热。
(2)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为__________。
(3)溶液a除了可能含有NaOH外,还一定含有的溶质是_____________(填化学式)。
Mg(OH)2+H2SO4=MgSO4+2H2O 少量水(或析出大量晶体) H2O NaCl、Na2SO4 【解析】本题考查了酸、碱、盐的化学性质,混合物的分离等。根据物质的性质以及物质间的反应,结合化学方程式的书写的知识进行分析解答。 工业废水加入氢氧化钠溶液,会与硫酸镁反应生成氢氧化镁沉淀和硫酸钠,与氯化铁反应生成氢氧化铁沉淀和氯化钠,A中加入某酸后得到硫酸镁,则加入的酸是硫酸,固...查看答案和解析>>
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:简答题
2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。根据所学知识填空。
(1)建造航母用到了钛合金,构成金属钛的粒子是________(填“原子”“分子”或“离子”),工业制钛有一种反应为:TiF4+2H2SO4 4HF+2X+TiO2,X 的化学式为_______。
4HF+2X+TiO2,X 的化学式为_______。
(2)航母外壳用涂料覆盖,是为了防止钢铁材料与_______________接触而锈蚀。
(3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是________________(填序号)。
A.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
C.ZnCl2溶液中加入足量铜粉后,再加入铁粉
原子 SO3 水和氧气 AB 【解析】本题主要考查了质量守恒定律,金属锈蚀的原理,探究金属的活动性顺序等。难度不大,根据已有的知识进行分析解答。 (1)金属是由原子直接构成,构成金属钛的粒子是原子;根据TiF4+2H2SO44HF+2X+TiO2可知,反应物中有1个钛原子,4个氟原子,4个氢原子,2个硫原子,8个氧原子,生成物中有4个氢原子,4个氟原子,1个钛原子,2个氧原子和2X;根...查看答案和解析>>
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:实验题
规范使用仪器是实验成功的保障,结合下图所示玻璃仪器,回答问题。

(1)可用作热源的是_____________(填序号),若往仪器E中加入块状固体,则应先将该仪器________(填“平”“立”或“斜”)放。
(2)若用仪器A和D稀释浓硫酸,则D的作用是________________,若用仪器A和D进行过滤操作,还必须用到上述的一种仪器是____________(填名称)。
(3)若某气体只能用F装置收集,则该气体的密度比空气小,且____________。
C 平 搅拌,加速散热 漏斗 易溶于水 【解析】本题考查了常用仪器的名称和选用,固体药品的取用,浓硫酸的稀释;过滤的原理、方法及其应用,常用气体的收集方法等。 (1)酒精灯可用作为热源,故选C;往试管中加入块状固体时,将试管平放,用镊子把药品送到试管口,再把试管慢慢竖起; (2)浓硫酸溶于水会放出大量的热,稀释浓硫酸时,要用玻璃棒不断地搅拌,使产生的热量加速散失。稀释浓硫酸时玻璃...查看答案和解析>>
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:科学探究题
(1)不同实验对反应速率有不同要求。某同学探究CO2制取实验,按要求答题。
限选控制反应速率的方法:①反应物的浓度 ②反应物的状态
限选试剂:A.稀盐酸 B.浓盐酸 C.块状石灰石 D.碳酸钠溶液 E.粉末状石灰石
填写下表并回答相关问题。
实验名称 | 控制速率的方法 | 所选用的最佳试剂 |
灭火器反应原理 | ① | ______和D |
CO2的实验室制法 | _____________ | A和C |
写出灭火器反应原理的化学方程式______________。
(2)已知:CO2和SO2既有相似性,又有差异性。

实验一:水槽中滴入紫色石蕊,将收集满两种气体的试管同时倒立于其中,片刻后实验现象如右图所示,说明相同条件下的溶解性:SO2_____ (填“>”或“<”)CO2,试管内溶液变成______色。
实验二:已知镁条在CO2中剧烈燃烧的化学方程式为:2Mg+CO2 2MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧,_______________________________。
2MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧,_______________________________。
查看答案和解析>>
科目: 来源:重庆市2018年中考化学试卷(A卷) 题型:计算题
化学反应在防治环境污染中扮演了重要角色。某工厂废气中的SO2,可用以下方式处理。方式一:2SO2+O2+2CaO=2CaSO4 方式二:2SO2+O2+4NaOH=2Na2SO4+2H2O 试计算: (已知:CaSO4的价格为700元/吨,相对分子质量为CaSO4 136 Na2SO4 142)。
(1)CaSO4中有两种元素的质量分数呈整数倍关系,这两种元素是硫元素和_________。
(2)若用方式一处理9.6tSO2,所得产品价值___________元?
(3)若用方式二处理9.61t SO2,刚好用去50t一定浓度的NaOH溶液,求所得溶液的溶质质量分数________(最终结果精确到0.1%)。
氧元素 14280 34.4% 【解析】本题考查了根据化学式计算和根据化学方程式计算。 (1)在CaSO4中,硫元素与氧元素的质量比=32:(16×4)=1:2,所以硫元素和氧元素质量分数呈整数倍关系; (2)方式一:设:生成的硫酸钙的质量为x 2SO2+O2+2CaO=2CaSO4 128 272 9.6t x x=20.4t 所得产品价值700元...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com