
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:单选题
下图所示是气体粒子示意图,图中 和
和 分别表示两种不同的原子,那么其中表示混合物的是( )
分别表示两种不同的原子,那么其中表示混合物的是( )

A. A B. B C. C D. D
C 【解析】A、该物质由一种分子构成,属于纯净物,错误; B、该物质由一种分子构成,属于纯净物,错误; C、该物质由一种分子构成,属于混合物,正确; D、该物质由两种分子构成,属于纯净物,错误。故选C。查看答案和解析>>
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:单选题
某元素的原子有三个电子层,已知第三层电子数等于第二层与第一层电子数之差,则该元素是( )
A. 铝 B. 镁 C. 硫 D. 磷
C 【解析】该原子有三个电子层,说明第一层和第二层已经排满电子,即第一层2个,第二层8个,第二层与第一层电子数之差为6,已知第三层电子数等于第二层与第一层电子数之差,则第三层上有6个电子,即原子核外的电子数为2+8+6=16,核内有16个质子,即硫元素。故选C。查看答案和解析>>
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:单选题
某原子R的质子数为m,相对原子质量为y,则粒子Rn+的核外电子数为 ( )
A. m + n B. m - n C. y - n D. y + (m-n)
B 【解析】因为在原子中核内质子数=核外电子数,所以R原子的核外电子数为m,粒子Rn+是R原子失去n个电子变成的,故Rn+的核外电子数为m-n。故选B。查看答案和解析>>
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:填空题
请认真回忆物质与其构成粒子之间的关系,回答下列问题:
(1)金属铁是由______构成的,氯化钠是由________构成的,二氧化碳是由_____构成的.
(2)若“ ”表示一个氮原子,则“
”表示一个氮原子,则“ ”表示______________.
”表示______________.
(3)在氧化汞受热分解过程中,能保持反应物化学性质的是___________;在反应前后保持不变的是___________________________.
(4)原子得到或失去电子后形成离子.某粒子的结构示意图如图
①a=__________时,该粒子是_____原子.
②当a=8时,该粒子是_________(填离子符号).
③若该粒子符号为AI3+,则该粒子的核电荷数为_______________。
铁原子 钠离子、氯离子 二氧化碳分子 一个氮分子 氧化汞分子 汞原子和氧原子 10 氖 O2- 13 【解析】原子,分子和离子都是构成物质的一种基本粒子。(1)金属铁是由铁原子构成的,氯化钠是由钠离子、氯离子构成的,二氧化碳是由二氧化碳分子构成的。(2)若“”表示一个氮原子,则“”表示一个氮分子。(3)在氧化汞受热分解过程中,能保持反应物化学性质的是氧化汞分子,分子是保持物质化学性质的最小微...查看答案和解析>>
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:填空题
下图中的①、②分别是氟元素、钙元素在元素周期表中的信息,A、B、C、D分别是四种粒子的结构示意图。根据题中信息回答:
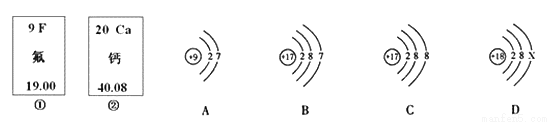
(1)钙原子的核电荷数为______________,氟元素的相对原子质量为_______________;
(2)X=______________;A、B、C、D中属于同种元素的粒子是_____________(填序号);
(3)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似_____________(填序号);
(4)17号元素在元素周期表中的位置是_______________________________________。
20 19.00 8 B、C B 第三周期第七主族 【解析】由元素周期表内元素信息表格,左上角数字表示原子序数,原子结构中,原子序数=核电荷数=质子数=核外电子数,下方数字表示该元素原子的相对原子质量;元素的种类由质子数决定,质子数相同则两种元素种类相同,而元素的化学性质由原子最外层电子数决定,以此为据解答本题。 (1)由钙元素和氟元素的元素信息表格,钙元素原子序数为20,故钙原子的核...查看答案和解析>>
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:填空题
写出下列化学符号或符号的意义:
化学符号 | H | ________ | O2 | ________ | CO2 |
意义 | ________ | 2个铁原子 | _______ | 3个水分子 | ________ |
查看答案和解析>>
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:填空题
在宏观、微观和符号之间建立联系是化学学科特点.
(1)在水、铜、氯化钠3种物质中,由原子构成的是_______.
(2)A、B、C、D表示4种物质,部分物质的微观示意图见表.A和B在不同条件下反应生成C或D.
物质 | B | C | D |
|
微观示意图 |
|
|
|
请回答以下问题:
①B、C、D三种物质都是由(填“分子”、“原子”或“离子”)_______构成的.
②B、C、D中属于化合物的是(填序号)_______.
③一个D分子由_____个原子构成.
④C、D都由碳、氧元素组成,但它们每个分子的构成________(填“相同”或“不同”),其性质有很大的差异。
铜/Cu 分子 C 、D 2 不同。 【解析】宏观角度是指物质和元素的角度、微观角度是指原子、分子、离子等的角度。(1)水是由水分子构成的;铜是由铜原子构成的;氯化钠是由钠离子和氯离子构成的;(2)通过微观示意图可得B是氧气、C是二氧化碳、D一氧化碳,而A和B在不同条件下生成的D为一氧化碳,故A是碳,C是二氧化碳。①氧气、二氧化碳、一氧化碳都是由分子构成的;②氧气是单质,二氧化碳和一氧化碳是...查看答案和解析>>
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:填空题
完成下列表格
原子种类 | 质子数 | 中子数 | 电子数 | 相对原子质量 |
钠 | 11 | _____ | _____ | 23 |
铁 | _____ | 30 | 26 | _____ |
查看答案和解析>>
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:填空题
在分子、原子、原子核、质子、中子、电子等粒子中,找出符合下列条件的粒子填在相应的横线上:
(1)能直接构成纯净物的有_______;
(2)化学反应中种类一定变化的是_______;
(3)一定能保持物质化学性质的粒子是________;
(4)化学变化中的最小粒子是________;
(5)带正电荷的粒子是________;
(6)不显电性的粒子是________;
(7)质量最小的粒子是________;
(8)在同一原子中数目相等的粒子是________;
(9)决定原子质量大小的粒子主要是________。
分子、原子 分子 分子 原子 原子核、质子 分子、原子、中子 电子 质子和电子 质子和中子 【解析】 根据分子是保持物质化学性质的最小微粒;原子是化学变化中最小微粒,原子是由原子核和核外电子组成,原子核由质子和中子组成(质子带正电,中子不带电)。原子核带正电,电子(电子质量很小)带负电,两者的带电量相同,一正一负,所以整个原子显示的是电中性;在原子中,原子序数=质子数=核电荷数=核外电...查看答案和解析>>
科目: 来源:山东省新泰市2018届九年级12月月考化学试卷 题型:填空题
通过探究物质构成的奥秘,我们知道物质是由原子等粒子构成的。请在下图的方框中填写粒子名称,表示各种粒子是怎样构成物质的。

________、________、________、________、________
质子 中子 电子 分子 离子 【解析】 从右向左考虑,最右边是构成物质的基本离子:分子、原子、离子.原子又是由原子核和核外电子构成,原子核又分为质子和中子.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com