
科目: 来源:广西百色市2018年中考化学试卷 题型:科学探究题
某化学兴趣小组的同学在进行“活泼金属与酸的反应”实验时,对铝和铝的化合物的性质进行了探究。
(查阅资料)铝是一种活泼金属,在空气中表现出良好的抗腐蚀性,是由于铝与氧气作用形成一层致密的氧化膜覆盖在铝的表面。
(性质探究)(1)金属的活动性
甲同学将用砂纸打磨过的铝片放入氯化镁溶液中,看到的现象是_________________,说明铝的金属活动性排在镁的_________。
(2)金属与酸的反应
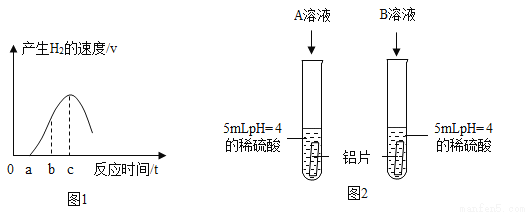
①铝片与稀硫酸反应产生氢气的速度与时间的关系如图1所示,单质铝与稀硫酸反应的化学方程式为___________。图中从a点到c点曲线上升的原因可能是____________________。
②将铝片与pH相同的足量稀硫酸、稀盐酸反应,结果是生成氢气的速度前者比后者慢很多。甲同学认为,可能是两片铝片的大小、质地等不一致的原因,于是将某铝片从中间切成两等份,再分别放入pH相同的稀硫酸和稀盐酸中,观察反应现象,结果仍是生成氢气的速度前者比后者慢得多。此实验方法是____。乙同学提出,可能是与稀硫酸反应的铝片表面有氧化膜的原因,大家一致表示反对,因为__________。丙同学对比盐酸和硫酸的化学式之后,认为可能是盐酸中的氯离子对反应产生促进作用,你认为还存在另一种可能是_____________________________。
(验证猜想)为了验证是“盐酸中的氯离子对反应产生促进作用”的猜想,大家一起设计了如图2所示的实验如果该实验能证明猜想,则加入的两种溶液的溶质化学式分别为A_______,B_________。
无明显现象后面2Al+3H2SO4===Al2(SO4)3+3H2↑随着反应的进行,温度升高,加快了反应速度控制变量法与稀盐酸反应的铝片表面也有氧化膜硫酸根离子对反应有抑制作用NaClNa2SO4(合理即可) 【解析】 根据已有的金属的性质、影响化学反应速率的因素、实验设计要注意控制变量等知识进行分析解答即可。 【解析】 【性质探究】(1)甲同学将用砂纸打磨过的铝片放入氯化镁溶...查看答案和解析>>
科目: 来源:广西百色市2018年中考化学试卷 题型:填空题
薰衣草精油的主要成分为芳樟醇、枷罗木醇等物质。其中芳樟醇的化学式为C10H18O。请回答:
(1)一个芳樟醇分子共有______个原子。
(2)芳樟醇中碳、氢、氧元素的质量比为______________。
2960:9:8 【解析】 (1)芳樟醇的化学式为(C10H18O)可知,一个芳樟醇分子是由10个碳原子18个氢原子1个氧原子构成的,共29个原子;(2)芳樟醇中碳、氢、氧元素的质量比为(12×10):(1×18):16=60:9:8。查看答案和解析>>
科目: 来源:广西百色市2018年中考化学试卷 题型:计算题
取50克一定溶质质量分数的碳酸钠溶液于烧杯中,逐滴滴入足量的氯化钡溶液,充分反应后将沉淀过滤,洗涤烘干,共得到9.85克固体物质。计算碳酸钠溶液中溶质的质量分数。
10.6%。 【解析】 【解析】 设碳酸钠溶液中溶质的质量为x, Na2CO3+BaCl2=BaCO3↓+2NaCl 106 197 x 9.85g x=5.3g 碳酸钠溶液中溶质的质量分数是:×100%=10.6%; 答:碳酸钠溶液中溶质的质量分数是10.6%。查看答案和解析>>
科目: 来源:人教版九年级化学上册:4.4“化学式与化合价 ”练习题 题型:单选题
在食盐中加入KIO3有益于防治地方性甲状腺肿大。检验食盐中是否含有碘酸钾,可利用化学反应:5X+KIO3+3H2SO4=3K2SO4+3I2+3H2O,其中X的化学式为
A. HI B. KI C. I2O5 D. HIO3
B 【解析】 根据反应的化学方程式5X+KlO3+3H2SO4=3K2SO4+3I2+3H2O,反应后K、S、O、I、H元素的原子个数分别为6、3、15、6、6,而反应前除5个X分子外K、S、O、I、H元素的原子个数分别为1、3、15、1、6;根据反应前后原子个数不变,可判断5个X分子中应含有5个K原子和5个I原子,则每个X分子由1个K原子、1个I原子所构成;故物质X的化学式为KI; ...查看答案和解析>>
科目: 来源:人教版九年级化学上册:4.4“化学式与化合价 ”练习题 题型:单选题
(题文)某种有机化合物R完全燃烧的化学方程式为:2R+3O2 4H2O+2CO2根据质量守恒定律,R的化学式是( )
4H2O+2CO2根据质量守恒定律,R的化学式是( )
A. CH3COOH B. C2H5OH C. CH3OH D. CH4
C 【解析】 根据质量守恒定律,化学反应前后各原子的种类和数目不变,反应前各原子的数目之和等于反应后各原子的数目之和,据此可推断X的化学式。 生成物中为共含有2个碳原子、8个氧原子、8个氢原子,根据质量守恒定律,化学反应前后各原子的种类和数目不变,反应前物质中也应含有2个碳原子、8个氧原子、8个氢原子,则R中含有1个碳原子、4个氢原子、1个氧原子,其化学式为:CH3OH。故选C ...查看答案和解析>>
科目: 来源:人教版九年级化学上册:4.4“化学式与化合价 ”练习题 题型:单选题
下列物质的化学式书写正确的是( )
A. 过氧化氢:H2O2 B. 纯碱:NaOH C. 硫酸铝:AlSO4 D. 氯化铁:FeCl2
A 【解析】 试题A选项是正确的书写;B选项纯碱的化学式为Na2CO3 C选项硫酸铝的化学式为Al2(SO4)3 D选项氯化铁的化学式为FeCl3 故答案选择A查看答案和解析>>
科目: 来源:人教版九年级化学上册:4.4“化学式与化合价 ”练习题 题型:单选题
高铁酸钾(K2FeO4)是一种具有氧化、吸附、凝聚、杀菌等功能的新型、高效水处理剂。它与水反应的化学方程式为4K2FeO4+10H2O==4Fe(OH)3↓+8X+3O2↑,则X的化学式为( )
A. K2O B. KOH C. K D. KH
B 【解析】 试题由反应的化学方程式4K2FeO4+10H2O=4Fe(OH)3↓+8X+3O2↑,可知反应中各原子在反应前后的个数为: 反应前 反应后 K原子 8 0 Fe原子 4 4 O原子 26 18 H原子 20 12 根据化学变化前后原子的种类、数目不变,可判断生成物X的8个分子中含8个K原子、8个O原子和8个H原子,则每个X分子由1个K原子、1...查看答案和解析>>
科目: 来源:人教版九年级化学上册:4.4“化学式与化合价 ”练习题 题型:单选题
金属锰与氯化亚铁溶液可发生如下反应:Mn+FeCl2=MnCl2+ Fe,下列说法错误的是( )
A. 该反应属于置换反应
B. 锰的金属活动性比铁强
C. 锰能置换出盐酸中的氢
D. 反应前后元素化合价都不变
D 【解析】 A、该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,正确;B、锰能与氯化亚铁反应置换出铁,故锰的金属活动性比铁强,正确;C、锰能与氯化亚铁反应置换出铁,故锰的金属活动性比铁强,因此锰是氢前的金属,能与稀盐酸反应,正确;D、氯化亚铁中铁元素为+2价,铁单质中铁为0价,错误。故选D。查看答案和解析>>
科目: 来源:人教版九年级化学上册:4.4“化学式与化合价 ”练习题 题型:单选题
以科学原理和实验事实为依据进行推理是学习化学的一种重要方法。下列推理得出的相关结论合理的是 ( )
A. 原子和分子都能构成物质,在化学变化中原子不能再分,所以分子也不能再分
B. 化合物是由不同种元素组成的纯净物,所以只含一种元素的物质一定不是化合物
C. 分解反应生成了多种物质,所以生成了多种物质的反应一定是分解反应
D. 水和过氧化氢都是由氢元素和氧元素组成的单质,所以它们的性质完全相同
B 【解析】 根据在化学变化中分子可分,原子不可分;化合物的定义,分解反应的概念,构成物质的微粒不同,物质的性质不同进行解答。 A、原子和分子都是构成物质的微观粒子,原子在化学变化中不能再分,分子在化学变化中能再分,错误;B、化合物是由有两种或两种以上元素组成的纯净物,所以只含一种元素组成的物质一定不是化合物,正确;C、分解反应是由一种反应物生成两种或两种以上其他物质的反应,但生...查看答案和解析>>
科目: 来源:人教版九年级化学上册:4.4“化学式与化合价 ”练习题 题型:单选题
下列关于维生素C(C6H8O6)的说法不正确的是( )
A. 1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成
B. 维生素C的相对分子质量为176
C. 维生素C中C、H、O三种元素的质量比为3﹕4﹕3
D. 维生素C中氢元素的质量分数约为4.5%
C 【解析】 A.1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成,正确;B.维生素C的相对分子质量为12×6+1×8+16×6=176,正确;C.维生素C中C、H、O三种元素的原子个数比为3﹕4﹕3,故说法错误;D.维生素C中氢元素的质量分数约为=4.5%。故选C。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com