
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:单选题
欲除去氯化钙溶液中含有的少量的盐酸,在不用酸碱指示剂的条件下,应加入的试剂是( )
A. 石灰石粉末 B. 生石灰 C. 石灰水 D. 纯碱
A 【解析】 例题A、石灰石的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水、二氧化碳,可把稀盐酸除去,化学反应的现象是有气体生成,并且没引进新的杂质,正确;B、生石灰虽然能把稀盐酸除去,但无现象出现,无法判断是否为恰好反应,错误;C、石灰水与稀盐酸反应无现象,错误;D、纯碱与稀盐酸反应会引入新的杂质氯化钠,错误。故选A。查看答案和解析>>
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:单选题
下列实验操作能达到预期目的是( )
①用托盘天平称取5.6克氧化铜粉末
②用10毫升水和10毫升酒精配制成20毫升酒精溶液
③用排水集气法收集到较纯净的氧气
④用pH试纸测得正常雨水的pH值为6.7
⑤用10毫升量筒量取8.2毫升氢氧化钠溶液
A. ①③⑤ B. ①②③⑤ C. ①②③④ D. ①③④⑤
A 【解析】 托盘天平的精确度为0.1g,所以能用托盘天平称取5.6克氧化铜粉末,故①能达到预期目的;由于分子之间有间隔,用10毫升水和10毫升酒精混合得到的酒精溶液的体积小于20毫升,故②不能达到预期目的;收集氧气的方法有排水法和向上排空气法,由于氧气的密度与空气的密度相差不大,所以用排空气法收集到的氧气纯度没有排水法收集到的氧气纯度高,故③能达到预期目的;用 pH试纸测得的数值只能...查看答案和解析>>
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:填空题
用化学符号填空
(1)3个钠离子_____;(2)氧化铝_____.
3Na+Al2O3 【解析】 (1)在书写离子符号时,在元素符号右上角标出该离子所带的电荷数,数字在前,正负符号在后,数字为“1”时省略不写。若表示多个该离子,就在其离子符号前加上相应的数字。由此可知3个钠离子的化学符号为3Na+。(2)氧化铝中铝元素显+3价,氧元素显﹣2价,根据正负化合价的代数和为零,并将金属元素写在前面,非金属元素写在后面,得到氧化铝的化学式为Al2O3。 ...查看答案和解析>>
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:填空题
(4分)请回答下列有关“走近低碳”的问题:
(1)以下属于“不可回收垃圾”的是________(填序号):
①废作业本 ②矿泉水瓶 ③霉变面包 ④破旧铁桶
(2)下列符合“低碳”理念的最清洁燃料是________:
①煤 ②汽油 ③天然气 ④氢气
(3)某“组合转化”技术是将CO2和H2在催化剂和加热条件下转化为化工原料乙烯(C2H4),请把该反应的化学方程式补充完整:
查看答案和解析>>
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:填空题
请完成下面填空:
(1)性质决定用途。以下连线正确的是_____(填字母)
性质 用途
a 金属的导电性 a 铜可用作电极材料
b金属的延展性 b 铁锅、铝锅是常用的烹饪用具
c 金属的导热性 c 28g纯金可拉成65km长金线
(2)用Fe粉制成的食品保鲜剂使用一段时间后,会逐渐变为_____色的氧化铁。
(3)铁制品易发生锈蚀,请写出一种防止铁生锈的方法_____。
(4)用氯化物_____(填化学式)溶液可以一次性验证Fe、Cu、Ag三种金属的活动性顺序。
a红刷漆CuCl2 【解析】 试题分析:(1)铜可用作电极材料,是利用铜的导电性、纯金可拉成金线是利用金的延展性、铁锅和铝锅作烹饪工具是利用金属的导热性。故选C。(2)铁粉作食品保鲜剂是利用铁粉与水、氧气的共同作用,铁锈的主要成分是氧化铁,它是一种红色固体。 (3)铁生锈是铁与氧气、水同时作用的结果,保持铁制品表面干燥、洁净可防止铁制品生锈。(4)铁、铜、银的金属活动性顺序是:F...查看答案和解析>>
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:填空题
下图是A、B两种物质的溶解度曲线,根据图示回答下列问题:

(1)t1℃时,A、B两种物质的溶解度是A_____B(填“>”、“<”或“=”,下同)。
(2)将t3℃的A、B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是A____B。
(3)t2℃时,100g水中溶解50gA刚好饱和,那么50g水中溶解_______gB也刚好达饱和,此时溶液的质量分数是__________(精确到0.1%)。
(1)< (2)> (3)25 33.3% 【解析】 试题(1)根据溶解度曲线可知t1oC时两种物质的溶解度是A<B,(2)因为A的溶解度受温度影响比B大,所以等质量的饱和溶液由高温降到较低温度时A析出的晶体较多。(3)t2oC时,A、B两种物质的溶解度相等,100g水中溶解50gA刚好饱和,那么50g水中最多溶解A的质量为: 50g÷2=25g.,同理50g水中最多溶解B的质量...查看答案和解析>>
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:填空题
请回答下列生活中的有关问题:
(1)区别棉纤维、羊毛纤维和合成纤维的最简单方法是做_____实验.
(2)鸡蛋中主要的营养素是_____(填“糖类”或“蛋白质”);能补充维生素C的食物是_____.
(3)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于实验操作中的_____.
灼烧闻气味蛋白质蔬菜、水果过滤 【解析】 试题(1)棉纤维燃烧时有一种烧纸的气味,羊毛纤维燃烧时有烧焦羽毛味,合成纤维燃烧时有一种特殊的气味,燃烧后的固体是硬渣,故用燃烧的方法可以区别。(2)鸡蛋中蛋白质含量较高,蔬菜和水果富含维生素。(3)通过过滤可以将难溶性的固体与液体进行分离。查看答案和解析>>
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:填空题
有五种化合物,它们两两之间发生的某些转化关系如图箭头所示。请回答:
(1)Na2SO4→NaCl的转化属于_____________反应(填基本反应类型);这一类型的反应能发生必须具备的条件之一是_______________________________(填一种)。
(2)写出下列反应的化学方程式:
NaOH→Na2SO4_______________________________;
NaCl→NaNO3_______________________________。
(3)在图中的物质间转化关系中有的可以逆向转化。他们分别是:_____________→_____________;_____________→_____________(填化学式)。

查看答案和解析>>
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:填空题
(1)酒精灯可用于_____;
(2)吸取和滴加少量液体用_____.
加热胶头滴管 【解析】 (1)酒精灯可用于给物质加热;(2)吸取和滴加少量液体用胶头滴管。查看答案和解析>>
科目: 来源:黑龙江省伊春市2018届九年级下学期期中化学试卷 题型:填空题
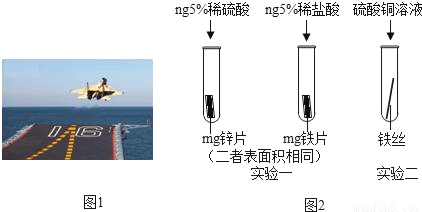
金属材料在国防建设中起着重要的作用,图1为歼﹣15飞机在辽宁舰上起飞。
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是_____、_____。
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的_____共同作用的结果。工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为_____。
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是_____。
②实验二中,若出现_____现象,可证明铁的活动性强于铜,该反应的化学方程式为_____。
(4)辽宁舰的建造耗费了大量的钢材。某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称重赤铁矿样品的质量为wg)。

①装置A中生成铁的化学方程式为_____,装置B中发生反应的化学方程式为_____。
②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是_____或_____。
强度大质量轻氧气、水Fe2O3+6HCl═2FeCl3+3H2O选取的酸的种类不同铁丝表面出现红色物质Fe+CuSO4═FeSO4+CuFe2O3+3CO 2Fe+3CO22NaOH+CO2═Na2CO3+H2O反应后装置A中药品的质量测出反应前后装置B增加的质量 【解析】 试题(1)铝合金材质的主要优点是质轻、强度和硬度好。(2)钢铁锈蚀的条件是与水和氧气同时接触。稀盐酸能与铁锈反应...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com