
科目: 来源:广西贺州市2018年中考化学试卷 题型:填空题
用化学用语填空。
(1)氦气_____________
(2)3个乙醇分子_________
(3)铝离子_________
(4)高锰酸钾中锰元素的化合价____________
He3C2H5OHAl3+ 【解析】 (1)氦气的化学式为He; (2)3个乙醇分子就是在乙醇化学式的前面加上数字3,故化学符号为:3C2H5OH; (3)铝离子带有3个单位的正电荷,故化学符号为:Al3+; (4)高锰酸钾中锰元素的化合价为+7,故化学符号为:。查看答案和解析>>
科目: 来源:广西贺州市2018年中考化学试卷 题型:填空题
化学就在我们身边,生活中蕴藏着丰富的化学知识。现有①硫酸 ②维生素 ③氢氧化钠 ④石墨 ⑤镁粉 ⑥肥皂水,请选择适当物质填空(填序号)
(1)蔬菜,水果富含______;
(2)能用来区分软水和硬水的是_____;
(3)能与油脂发生反应的是____;
(4)汽车用铅酸蓄电池中含有____;
(5)用于制作烟花和照明弹的是__________;
(6)常作于电池电极的是_____。
② ⑥③①⑤④ 【解析】 (1)蔬菜、水果中富含维生素; (2)区分硬水和软水用肥皂水,泡沫多的是软水,泡沫少的是硬水; (3)氢氧化钠能与油脂发生反应,可以用于去除油污; (4)汽车用铅酸蓄电池中含有的酸是硫酸; (5)镁在燃烧时发出耀眼的白光,可用于制作烟花和照明弹; (6)石墨具有导电性,常用作电池电极。查看答案和解析>>
科目: 来源:广西贺州市2018年中考化学试卷 题型:简答题
贺州市是个美丽的地方。
(1)在姑婆山国家森林公园里,你可以租用“共享单车”,骑行在森林与山水之间,如图所示自行车中的材料属于有机合成材料的是______(用图中序号填空);

(2)在富川县“潇贺古道”岔山村,你可以品尝到由当地种植的糯米做成的“梭子粑”,糯米富含的基本营养素是_____;
(3)初夏,在钟山县十里画廊,你可以闻到荷花的清香,从分子的角度来解释,能闻到花香的原因是_____;
(4)在邵平县黄姚古镇,你可以品当地的绿茶,茶叶中含有茶氨酸(C7H14O3N2),茶氨酸属于_______________(填“有机物”或“无机物”);
(5)平桂区的紫云洞,形态各异的钟乳石、石笋令人惊叹,这是因为溶解在水中的碳酸氢钙Ca(HCO3)2分解生成碳酸钙、二氧化碳、水的缘故,请写出该反应的化学方程式___。
②④糖类分子在不断的运动有机物Ca(HCO3)2CaCO3↓+H2O+CO2↑ 【解析】 (1)三大有机合成材料包括:塑料、合成纤维、合成橡胶,所以橡胶轮胎和手柄套属于有机合成材料;(2)糯米富含的基本营养素是糖类;(3)初夏,在钟山县十里画廊,你可以闻到荷花的清香,能间到花香的原因是分子在不断的运动;(4)茶叶中含有茶氨酸(C7H14O3N2),茶氨酸中含有碳元素,属于有机物;(5)...查看答案和解析>>
科目: 来源:广西贺州市2018年中考化学试卷 题型:简答题
甲乙丙三种物质的溶解度曲线如图所示。回答下列问题:

(1)在t1℃,甲乙丙三种物质的溶解度由大到小顺序为:_____;
(2)t2℃时乙物质的溶解度为____(没写单位“g”或“克”不给分);
(3)若甲中含有少量的乙,则采用_____方法提纯甲;
(4)将t2℃时90g甲的饱和溶液降温到t1℃,析出晶体的质量为______g。
乙>甲=丙80g降温结晶27.5 【解析】 (1)通过分析溶解度曲线可知,在t1℃,甲、乙、丙三种物质的溶解度由大到小顺序为:乙>甲=丙;(2)t2℃时,乙物质的溶解度为80g;(3)甲物质的溶解度受温度变化影响较大,所以若甲中含有少量的乙,则采用 降温结晶方法提纯甲;(4)t2℃时,甲物质的溶解度是80g,所以90g甲的饱和溶液中含有溶质40g,溶剂50g,将t2℃时90g甲的饱和溶...查看答案和解析>>
科目: 来源:广西贺州市2018年中考化学试卷 题型:填空题
学习化学后,我们学会了从微观角度认识事物,根据下列几种几种示意图,回答问题:

(1)由图A可知Si元素的相对原子质量为_____;
(2)B图微粒易_____(填“失去”或“得到”)电子后就变成阳离子;
(3)若D是离子结构示意图,则x=____;
(4)元素E处于第____周期;
(5)由B、C两种元素组成的化合物的化学式为____,该化合物属于____(填“酸”“碱”“盐”或“氧化物”)。
28.09失去84Na2O氧化物 【解析】 (1)根据元素周期表的意义可知:Si元素的相对原子质量为28.09; (2)B图微粒,最外层电子数为2,小于4,个,反应中容易失去电子就变成阳离子; (3)若D是离子结构示意图,则x=8;(4)电子层数决定周期数,元素E核外有4个电子层,E处于第4周期; (5)B是钠元素,在化合物中的化合价为+1价,C是氧元素,氧元素化合价...查看答案和解析>>
科目: 来源:广西贺州市2018年中考化学试卷 题型:简答题
下表表示汽车的行驶速度与所产生的大气污染物的质量之间的关系。
污染物 | 速率(km/h) | ||
50 | 80 | 120 | |
一氧化碳/g | 8.7 | 5.4 | 9.6 |
氮的氧化物/g | 1.0 | 1.2 | 3.8 |
碳氢化合物/g | 0.7 | 0.6 | 0.8 |
问:
(1)从上表中你认为,要使污染程度最小,汽车的速度应保持在____。
(2)汽车尾气产生的CO气体,能与血液中的______结合会导致人体中毒;CO燃烧时产生的______气体,大量排放到空气中会加剧温室效应。
(3)随着工业的发展,排放到空气中的有害气体和____对空气造成了污染;请你写出两条减少大气污染的措施:____、______(其他合理答案均可)。
80km/h血红蛋白二氧化碳烟尘减少化石燃料的使用开发利用新能源 【解析】 (1)速度为50km/h时,排放污染物总质量为:8.7g+1.0g+0.7g=10.4g;速度为80km/h时,排放污染物总质量为:5.4g+1.2g+0.6g=7.2g;速度为120km/h时,排放污染物总质量为:9.6g+3.8g+0.8g=14.2g;根据分析可知,速度为80km/h时产生污染物的总质量最...查看答案和解析>>
科目: 来源:广西贺州市2018年中考化学试卷 题型:推断题
A﹣G是初中常见的物质,其中A、C是组成元素相同的氧化物,B、D、G是气体且G有刺激性气味,Y是一种碳酸盐,E常用来改良酸性土壤,其相互反应情况如图所示(短线“﹣”表示相连的物质间能反应,箭头“→”表示能生成)请回答下列问题:

(1)A的化学式____,E的化学式_____(填名称不得分)
(2)写出物质D的一种用途_____(其他合理答案均可)。
(3)写出E溶液与Y溶液反应的化学方程式______,该反应的基本类型是____。
H2O2Ca(OH)2灭火Ca(OH)2+(NH4)2CO3=CaCO3↓+2H2O+2NH3↑复分解反应 【解析】 G有刺激性气味,则G是氨气,E常用来改良酸性土壤,则E是氢氧化钙,E和Y加热能产生氨气,故Y是铵态氮肥,A、C是组成元素相同的氧化物,且A能生成B和C,故A可能是过氧化氢,C是水,B是氧气,水能与X反应生成氢氧化钙,故X是氧化钙,氧气生成的D能与氢氧化钙反应,故D是二氧...查看答案和解析>>
科目: 来源:广西贺州市2018年中考化学试卷 题型:实验题
根据下列实验装置回答下列问题
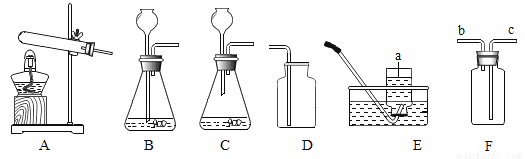
(1)写出图中仪器a的名称:____
(2)实验室制取CO2的化学方程式为____,采用的发生装置和收集装置是____(填字母序号)
(3)实验室常用亚硫酸钠和硫酸反应制取SO2,SO2是一种密度比空气大、易溶于水的有毒气体,若选择图F装置收集SO2,气体应从导管口____(填“b”或“c“)端进入,理由是_____,尾气必须要进行处理,其目的是______。
集气瓶CaCO3+2HCl═CaCl2+H2O+CO2↑BDc二氧化硫密度比空气大,二氧化硫有毒,会污染空气 【解析】 (1)通过分析题中所指仪器的名称和作用可知,a是集气瓶; (2)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳密度比空气大,溶于水,所以...查看答案和解析>>
科目: 来源:广西贺州市2018年中考化学试卷 题型:科学探究题
现有一包黑色固体粉,可能含有炭粉、CuO、Fe3O4中的两种或者三种,某化学兴趣小组通过实验探究其成分。
(1)提出问题:该黑色固体粉末成分是什么?
(2)作出猜想:
猜想一:混合固体是炭粉、CuO
猜想二:混合固体是炭粉、Fe3O4
猜想三:混合固体是______(两种物质写不全不给分)
猜想四:混合固体是炭粉、CuO、Fe3O4
(3)查阅资料:Fe3O4为黑色粉末,能与盐酸反应,含有Fe3+的盐溶液遇到KSCN(硫氰化钾)溶液时变成红色,Fe(OH)2是一种白色沉淀。
(4)实验探究:取一定量的固体于试管中,加足量的盐酸,充分反应后有部分固体溶解,过滤,得到滤液A,并对滤液A的成分进行如下探究:
实验操作 | 实验现象 | 实验结论 |
步骤一:取一定量滤液A于试管中,加入足量的铁粉 | 无红色固体析出 | 该固体物质一定没有____ |
步骤二:又取一定量的滤液A于试管中,加入少量的KSCN(硫氰化钾)溶液 | 溶液变成红色 | 滤液A中还一定含有的物质是___ |
步骤三:再取一定量的滤液A于试管中,加入足量的NaOH溶液 | 有红褐色沉淀生成,同时还有少量的白色沉淀生成,白色沉淀迅速变成灰绿色,最后面变成红褐色 | 滤液A中还一定含有的物质是____ |
(5)讨论交流:
①通过以上实验,猜想______成立。
②写出Fe3O4与盐酸反应的化学方程式_____。
③Fe3O4与盐酸反应时元素的化合价没有改变,请大家推断Fe3O4中铁元素的化合价为___(写两种价态才得分)。
(6)拓展:请写出同种元素显不同化合价的一种盐_____(其它合理答案也得分)(写化学式)。
CuO、Fe3O4氧化铜氯化铁氯化亚铁二Fe3O4+8HCl═2FeCl3+FeCl2+4H2O+2、+3NH4NO3 【解析】 稀盐酸不能和碳反应,能和四氧化三铁反应生成氯化亚铁、氯化铁和水;氢氧化钠和氯化铁反应生成红褐色沉淀氢氧化铁和氯化钠,和氯化亚铁反应生成氢氧化亚铁沉淀和氯化钠,氢氧化亚铁在空气中能被氧化成氢氧化铁。 (2)黑色固体粉末,可能含有炭粉、CuO、Fe3O4中...查看答案和解析>>
科目: 来源:广西贺州市2018年中考化学试卷 题型:计算题
某纯碱样品中含有少量的氯化钠。取该样品13.9g完全溶于206.1g水中,加入90g CaCl2溶液,恰好完全反应
后生成沉淀的质量为10g。求:
(1)生成的沉淀物的化学式为:_____;
(2)样品中碳酸钠的质量为:______g;
(3)反应后溶液中溶质质量分数为___________。(要求写出计算过程)
CaCO310.6g 5% 【解析】 根据生成的沉淀碳酸钙的质量和对应的化学方程式求算碳酸钠的质量和生成的氯化钠的质量,进而求算对应的质量分数。 【解析】 碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,所以沉淀的化学式为CaCO3;设碳酸钠的质量为x,生成的氯化钠的质量为y, Na2CO3+CaCl2=CaCO3+2NaCl 106 100 117 x...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com