
科目: 来源:重庆市2018届九年级下学期期中化学试卷 题型:填空题
选择下列物质回答问题(用字母填空):
A.钛合金 B.盐酸 C.氢氧化钠 D.活性炭
(1)炉具清洁剂中含有的可去油污的物质是_____;
(2)_____与人体具有很好的“相容性”,因此可用来制造人造骨;
(3)_____是胃液中的主要成分,可以帮助消化;
(4)制糖工业中利用_____来脱色以制白糖。
CABD 【解析】 物质的性质决定物质的用途,根据常见化学物质的性质和用途进行分析解答即可。 (1)氢氧化钠能与油脂反应,炉具清洁剂中含有的可去油污的物质是氢氧化钠; (2)钛合金与人体具有很好的“相容性”,因此可用来制造人造骨; (3)盐酸是胃液中的主要成分,可以帮助消化; (4)活性炭具有吸附性,能吸附异味和色素,可用于制糖工业中脱色以制白糖。查看答案和解析>>
科目: 来源:重庆市2018届九年级下学期期中化学试卷 题型:简答题
2018年1月26日早上7点左右,重庆一公寓发生燃气爆炸,初步调查事故原因为天然气泄漏所致。
(1)天然气属于_____(选填“可再生”或“不可再生”)能源。
(2)请写出天然气燃烧的化学方程式_____。
(3)为安全起见,可在厨房安装天然气泄漏报警器。报警器安装的正确位置应选择如图中的_____(选填“A”或“B”)。
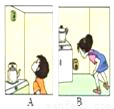
如果报警器显示漏气,下列应急措施可行的有_____(填序号)。
①关闭气源阀门 ②马上开门窗通风 ③立即打开抽油烟机 ④继续点火做饭
不可再生CH4+2O2 CO2+2H2OA ①② 【解析】 根据能源的分类,反应的原理,气体的性质以及急救措施来分析。 (1)天然气是一种化石燃料,属于不可再生能源; (2)天然气的主要成分是甲烷,甲烷与氧气在点燃的条件下反应生成二氧化碳和水,反应的化学方程式是:CH4+2O2 CO2+2H2O; (3)天然气的密度比空气小,应该安装在高处。故选A;天然气泄漏时,应该...查看答案和解析>>
科目: 来源:重庆市2018届九年级下学期期中化学试卷 题型:填空题
(1)在“南海一号”打捞出来的文物中,“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜锈;铁器则锈迹斑斑,残存很少,这说明金、铜、铁这三种金属的活动顺序由强到弱的顺序是_____;
(2)生铁和钢是世界上用量最大的_____(填“金属材料”或“合成材料”);炼铁的原理是利用一氧化碳与氧化铁反应,反应的化学方程式为_____,写出防止铁生锈的一种方法是_____。
铁>铜>金金属材料Fe2O3+3CO2Fe+3CO2在铁制品表面涂油刷漆等 【解析】 试题根据物质与氧气的反应的难易程度可以确定三者的活动性为铁大于铜大于金;生铁和钢是合金材料;炼铁的原理是利用一氧化碳与氧化铁反应,反应的化学方程式为Fe2O3+3CO高温2Fe+3CO2;防止铁生锈的一种方法隔绝同氧气接触等措施。查看答案和解析>>
科目: 来源:重庆市2018届九年级下学期期中化学试卷 题型:填空题
如图是a、b、c三种固体物质(均不含结晶水)的溶解度曲线。
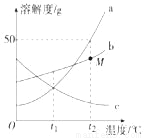
(1)t1℃时,a、b、c三种固体物质的溶解度的大小关系是_____。
(2)t2℃时,将30g物质a加入到50g水中,形成溶液的质为_____g。
(3)t2℃时,将a、b、c三种物质的饱和溶液降温到t1℃,仍为饱和溶液的是_____。
(4)在t2℃时,M点的a、b两种溶液的溶质质量分数大小关系为a_____b(填“>”或“<”或“=”)。
(5)当a中混有少量的b时,采取的提纯方法是_____。
b>a=c; 75 a、b = 降温结晶 【解析】 试题(1)根据溶解度曲线,t1℃时,a、b、c三种固体物质的溶解度的大小关系是b>a=c (2)根据溶解度曲线,t2℃时,a物质的溶解度为50g,即在t2℃时,100g水中最多只能溶解50g物质a,将30g物质a加入到50g水中,形成溶液的质量=50g+25g=75g (3)根据溶解度曲线,物质a、b的溶解度随温度的升高而...查看答案和解析>>
科目: 来源:重庆市2018届九年级下学期期中化学试卷 题型:填空题
根据下图所示, 回答有关问题:

(1)写出图中标有字母的仪器名称:a __________。
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是 ________ (填字母),实验时该装置试管口应放一团棉花,其目的是 _______________ ;反应的化学方程式为__________________________________________ 。
(3)实验室制取二氧化碳气体,若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,装置 中的液体是 ______________________ (填写试剂名称)。如果用E装置收集该气体,则气体应从 ____________ 端进入(填b或c)。通常用澄清石灰水来检验二氧化碳,反应的化学方程式 为 __________________________________ 。
(4)下图是以锌粒和稀硫酸反应制备H2,并用排水法收集.请把图补画完整_____。

查看答案和解析>>
科目: 来源:重庆市2018届九年级下学期期中化学试卷 题型:实验题
欲配制50g质量分数为10%的氯化钠的溶液,操作过程如图所示,看图回答下列问题:

(1)称量时,应称取_____g 食盐。
(2)把水的密度近似地看作1g/mL,则须量取_____ mL水。如果有10mL、50mL和100mL的量筒,最好选取_____ mL的量筒。
(3)实验中使用玻璃棒的目的是_____。
(4)如果所配得的溶液溶质的质量分数比大于10%,你认为可能的原因有_____。
A.量取水时俯视读数
B.所用氯化钠中含有杂质
C.称量时左托盘放砝码,右托盘放氯化钠(1g以下用游码)
D.未溶解充分就转移到试剂瓶中
54550搅拌,加速溶解A 【解析】 根据“溶质的质量=溶液的质量×溶质的质量分数”计算配制溶液所需食盐的量;根据“溶剂的质量=溶液的质量﹣溶质的质量”计算出水的量并换算成体积,并根据“量程稍大于所量液体体积”的原则选择量筒;明白溶解时玻璃棒的作用,为加快溶解需要使用玻璃棒;根据导致溶液中氯化钠的质量分数大于10%的原因可能是:称量溶质称多了,量取水时量少了(量水时俯视读数)进行解答。...查看答案和解析>>
科目: 来源:重庆市2018届九年级下学期期中化学试卷 题型:计算题
为测定某黄铜样品中锌的含量,某同学称取20g黄铜(含铜和锌)样品于烧杯中,向其中加入19.6%的稀硫酸,直到不再产生气泡为止,共消耗稀硫酸100g,求:
(1)该黄铜样品中铜的质量_______。
(2)将反应的混合物过滤,向滤液中加入87.4g水,则所得溶液中溶质的质量分数_______。
13g16.1% 【解析】 铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气,根据反应的化学方程式和提供的数据可以进行相关方面的计算。 (1)设:锌的质量为x,生成硫酸锌的质量为y,生成氢气质量为z, Zn +H2SO4 ═ZnSO4+ H2↑ 65 98 161 2 x 100g×19.6% y z x=13g,y=32.2g,z=0.4g 答:...查看答案和解析>>
科目: 来源:黑龙江省2018届九年级下学期期中化学试卷 题型:单选题
在化学反应前后可能发生改变的是( )
A. 元素种类 B. 原子数目
C. 分子数目 D. 各物质的总质量
C 【解析】 根据质量守恒定律的内容及其质量守恒的实质可以知道:反应前后物质的质量之和、原子的种类、原子的个数不变,所以可以据此解答该题。 质量守恒定律的内容及实质可以知道,在反应前后反应物的质量总和等于生成物的质量总和,其实质是原子的个数不变;原子的种类不变,元素的种类也不变,所以本题中选项A、B和D选项在反应前后是不变的,反应前后物质的分子个数是可以发生改变的,但是不是一定改...查看答案和解析>>
科目: 来源:黑龙江省2018届九年级下学期期中化学试卷 题型:单选题
下列示意图形象地表示了A(  )与B(
)与B( )反应生成C(
)反应生成C( )其反应前后分子及数目的变化,则该反应的化学方程式中, A、B、C的化学计量数之比为( )
)其反应前后分子及数目的变化,则该反应的化学方程式中, A、B、C的化学计量数之比为( )

A. 1:1:1 B. 2:2:1 C. 2:1:2 D. 1:2:3
C 【解析】 对比反应前后反应物与生成物分子及其数目的变化的微观示意图可知,反应后仍含有1个B分子,说明反应前的2个B分子中有1个分子未参加反应而只有1个B分子参加了该反应,反应前的2个A分子参加了该反应,反应后生成了2个C分子;因此,该反应的化学方程式中A,B,C前的化学计量数之比为2:1:2;故选C.查看答案和解析>>
科目: 来源:黑龙江省2018届九年级下学期期中化学试卷 题型:单选题
科学家用计算机模拟后确认,60个N原子可结合成N60分子。下列关于N60的叙述中正确的是 ( )
A. N60是一种新型的化合物 B. 一个N60分子中含有30个N2分子
C. N60的相对分子质量为840 D. N60和N2混合后形成的是纯净物
C 【解析】 A、化合物是指由不同种元素组成的纯净物,N60是由一种元素组成的纯净物,属于单质,故A说法错误; B、分子是由原子构成的,一个N60分子中含有60个氮原子,故B说法错误; C、N60的相对分子质量为14×60=840,故C说法正确; D、根据纯净物是由一种物质组成的物质,N60和N2是两种物质,混合后形成的是混合物,故D说法错误; 故选C ...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com