
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:单选题
下列关系曲线不能正确反映其对应变化关系的是( )

A. A B. B C. C D. D
D 【解析】 根据催化剂的特点,氢氧化钙、碳酸钙的性质,氢氧化钠碱性,金属与酸反应规律进行分析解答。 A、催化剂能改变化学反应的速率,而本身的质量和化学性质不变。二氧化锰是氯酸钾分解的催化剂,反应后前后质量不变,与图像相符;B、向Ca(OH)2溶液中通入CO2至过量先发生的是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,氢氧化钙完全反应后,二氧化碳、水、碳酸钙三种物质反应生成易溶于水...查看答案和解析>>
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:单选题
图是某同学鉴别NH4HCO3、NH4C1、KCl三种化肥的过程,其中试剂甲和乙分别可能是
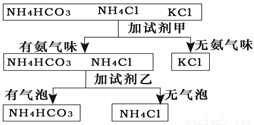
A. 甲:熟石灰;乙:稀盐酸
B. 甲:水;乙:氢氧化钠溶液
C. 甲:氢氧化钠溶液;乙:水
D. 甲:稀盐酸;乙:氯化钠溶液
A 【解析】 在第一步鉴别过程中,加入试剂甲,两种铵态氮肥有氨味,可推断试剂甲显碱性;在第二步鉴别过程中,加入试剂乙,NH4HCO3中有气泡产生,可推断试剂乙是一种酸,对照各选项,符合题意的答案应选A、C。查看答案和解析>>
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:填空题
我们的家乡大庆市有“绿色油化之都”、“天然百湖之城”的美誉,它因石油而起,因石油而兴,在合理开发利用石油资源的同时也要保护好自然环境。
(1)原油是一种黏稠状液体,属于_________资源(选填“可再生”、“不可再生”),它主要含有______两种元素(填元素符号)。
(2)石油经炼制得到的汽油、柴油等产品可作为机动车燃料。燃烧的三个条件:可燃物、________、温度达到着火点。
(3)以石油产品为原料可进一步生产___________、合成纤维、合成橡胶等合成有机高分子材料,人类从此摆脱了依赖天然材料的历史。
(4)我市淡水资源丰富,保护好水资源是每个人的责任。保护水资源一方面要节约用水,另一方面要防治水体_________。实验室用的蒸馏水是净化程度较高的水,可以用自来水通过_______制取。
不可再生C, H和氧气(空气)接触塑料污染蒸馏 【解析】 (1)煤、石油,天然气都是不可再生能源;他们的主要成分是碳、氢元素的化合物;(2)燃烧需要同时具备的三个条件:物质有可燃性、温度达可燃物的着火点、与氧气充分接触;(3)有机高分子合成材料包括:塑料 、合成纤维、合成橡胶;保护水资源一方面要节约用水,另一方面要防治水体污染;蒸馏是加热到水的沸点使水从混合物中蒸发出来,然后再被冷凝成...查看答案和解析>>
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:填空题
金属活动性顺序在工农业生产和科学研究中都有重要作用。现有A、B、C三种金属,A、B可溶于盐酸,C不溶于盐酸,将A投入BCl2溶液中可发生反应:A+BCl2=ACl2+B。
(1)A、B、C三者金属活动性由强到弱的顺序为____________。与金属置换反应规律相同,非金属单质之间的置换反应也有类似的规律,根据下列反应:①Cl2+2NaBr=Br2+2NaCl ②Br2+2NaI=I2+2NaBr
(2)Cl2、Br2和I2单质的活泼性由强到弱的顺序为____________。
(3)根据以上规律,下列反应可以发生的是_____________。
a.Cl2+2KI=2KCl+I2 b.2NaCl+I2=2NaI+Cl2↑
(4)经查阅资料,硫单质的活泼性比Cl2、Br2和I2都弱,请任写一个化学方程式证明该结论_________。
A>B>CCl2>Br2>I2aI2+Na2S=S+2NaI 【解析】 (1)A、B可溶于盐酸,说明A、B在氢前;C不溶于盐酸,说明C在氢后;将A投入BCl2溶液中可发生反应:A+BCl2=ACl2+B,说明A的活动性比B强;A、B、C三者金属活动性由强到弱的顺序为A>B>C;(2)活动性强的能把活动性弱的置换出来,①Cl2+2NaBr=Br2+2NaCl ,氯的活动性比溴的强, ②B...查看答案和解析>>
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:流程题
钛和钛合金被认为是21世纪重要的金属材料。钛合金与人体具有很好的“相容性”,可用于制造人造骨骼。工业上以钛铁矿(主要成分为钛酸亚铁,FeTiO3)为原料生产钛,其工业流程示意图如下:

请回答:(1)钛合金属于_______(选填“混合物”、“纯净物”)。
(2)钛酸亚铁FeTiO4中钛的化合价为______价。
(3)以CO和H2在合成塔中生产甲醇(CH3OH)属于化合反应,其化学方程式为________________。
(4)经高温冶炼得到金属钛,则参加反应的镁与生成钛的质量比为_________。
(5)氯化过程中主要发生的反应为2FeTiO3+6C+7Cl2 2TiCl4+2X+6CO,则X的化学式为______。
2TiCl4+2X+6CO,则X的化学式为______。
查看答案和解析>>
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:推断题
A~J均为初中常见化学物质:它们之间的转化关系如图所示,部分产物已省略。已知A是人体胃酸的主要成分,B是由四种元素组成的盐类,C是一切生命生存所必须的物质,E是厨房重要的调味品。请回答下列问题:
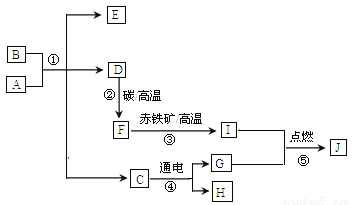
(1)物质F____________,H_________(用化学式表示)。
(2)A和B反应的化学方程式为_____________。
(3)①~⑤属于分解反应的是________________。
(4)A和J反应可生成两种不同盐类,两者所含元素种类相同,但其比例不同,则A何J反应的化学方程式为_______________。
COH2HCl+NaHCO3=NaCl+H2O+CO2↑④Fe3O4+8HCl=FeCl2+2FeCl3+4H2O 【解析】 (1)A是人体胃酸的主要成分,所以A是盐酸,B是由四种元素组成的盐类,B是碳酸氢钠,C是一切生命生存所必须的物质,C水;E是厨房重要的调味品E是氯化钠,由此可推知,D是二氧化碳,F是一氧化碳,G是氧气,H是氢气,I是铁;(2)碳酸氢钠和盐酸反应生成氯化钠、二氧化...查看答案和解析>>
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:填空题
已知A、B、C三种物质的溶解度曲线如图所示。

(1)在阴影区域部分,处于不饱和状态的是__________(选填“A、B盐酸反应生成、C”)。
(2)若饱和A溶液中含有少量的C,提纯A的方法为______结晶,过滤。
(3)P点表示的含义为_________。
(4)在t1℃下,B、C的饱和溶液升温至t2℃,所得溶液溶质的质量分数大小关系为_______。
(5)向试管中滴入2mL水后,若X中有固体析出,则X为______(选填“A、B、C”)。
B降温t1℃时B,C物质溶解度相同B>CC 【解析】 (1)在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。在阴影区域部分,处于不饱和状态的是B;(2)A的溶解度受温度影响较大,且随温度降低而减小,降温时会结晶析出,而C的溶解度受随温度降低而增大,降温时不析出,而是变成不饱和溶液,若A物质中含有少量的C物质,提纯A物质的...查看答案和解析>>
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:综合题
大庆市某中学化学兴趣小组利用以下装置制备氢气,并验证氢气的性质,按要求回答以下问题:

(1)化学实验室现有质量分数为98%的浓硫酸,需配制245g质量分数10%的稀硫酸,配制步骤如下:
①计算:所需质量分数98%的浓硫酸______g;②量取;③稀释量取和稀释浓硫酸所用的玻璃仪器有____。简要描述浓硫酸的稀释方法___________。
(2)该兴趣小组制备氢气的原理为___________(化学方程式)。
(3)装置B的作用__________________。
(4)下列有关实验操作或现象描述不正确的是____
A.实验开始时,应先通入氢气,然后再点燃C处酒精灯
B.点燃C处酒精灯后,D处硫酸铜固体由白色逐渐变为蓝色
C.E处酒精灯的作用是点燃未反应的氢气
D.实验结束时,应先停止通入氢气,然后熄灭C处酒精灯
(5)实验结束后,发现部分氧化铜未被还原,已知反应前氧化铜质量为a克,反应结束后混合固体质量为b克,则被氢气还原的氧化铜的质量为___________g。
25量筒、烧杯、玻璃棒将浓硫酸沿烧杯壁缓慢地注入水中,用玻璃棒不断搅动Zn+H2SO4=ZnSO4+H2↑吸收气体中的水蒸气D5(a-b) 【解析】 (1)①需配制245g质量分数10%的稀硫酸,需要质量分数为98%的浓硫酸,的质量为x;则245g×10%= 98%×x;x=25g;量取液体时应先倾倒至接近刻度线,然后用胶头滴管滴加至刻度线,所以用到的仪器有量筒和胶头滴管;稀释浓硫酸,...查看答案和解析>>
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:科学探究题
化学反应速率是衡量化学反应进行快慢的物理量。为了探究影响化学反应速率的隐私,以过氧化氢分解为研究对象进行实验。三个小组均采用如图装置进行实验,记录收集10mL氧气的时间。实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末。
A组:探究催化剂对化学反应速率的影响
取5mL10%H2O2溶液,三次实验分别加入0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
试剂 | MnO2 | 红砖粉末 | CuO |
t/s | 10 | 60 | 20 |
由此得出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用。某同学对该结论提出疑问。补充对比实验,操作为________________。
结果:长时间(大于100s),收集到很少量气体。
更正结论:红砖粉末______(选填“有”、“无”)催化作用,三者中______催化效率最高。
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,进行实验,记录时间t1。
乙同学:取10mL2.5%H2O2溶液,加入0.5gCuO为催化剂,进行实验,记录时间t2。
实验结果:__________________。
结论:浓度越大,反应速率越快。
丙同学:对实验设计提出疑问,并补充实验_______________。
记录时间t3,且t1<t3<t2。
更正结论为:当________时,反应物浓度越大,反应速率越快。
C组:探究_________对化学反应速率的影响。
取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴记录时间t4、t5,且t4>t5。
结论:当反应物浓度和催化剂相同时,________________。
综上所述:①为了研究某一因素对化学反应速率的影响,必须_______________。
②探究发现影响化学反应速率的因素有:_________________。
取50mL10%H2O2溶液不放入任何催化剂记录产生10mL氧气时间无二氧化锰t1查看答案和解析>>
科目: 来源:黑龙江省大庆市2018届九年级中考化学试卷 题型:计算题
铝合金是目前广泛使用的合金材料,已知某铝合金由Al、Fe、Cu三种金属构成,为了测定各种金属含量,取12.5g合金样品与盐酸反应,消耗浓盐酸(质量分数36.5%)100g。另取12.5g合金样品与氢氧化钠溶液反应,消耗含氢氧化钠12g的溶液40mL。已知:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,Fe,Cu均不与氢氧化钠溶液反应。请问:(1)12.5g样品中含铝多少克_________?(2)铜在合金中所占的质量分数是多少_________?
含铝8.1g铜占12.8% 【解析】 (1)设12.5g样品中含铝的质量为x, 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 54 80 x 12g x=8.1g 与合金反应的氯化氢的质量:36.5%×100g=36.5g; (2)设铝消耗氯化氢的质量为y, 2Al+6HCl=2AlCl3+3H2↑ 54 219 8.1g...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com