
科目: 来源:仁爱版化学九年级上册5.2质量守恒定律练习题 题型:填空题
为了探究“水的净化”过程,某实验小组从河中取了水样,观察到:水样浑浊有异味;有固体小颗粒。现对水样进行如下处理:
⑴将水样静置一段时间后进行 ________(填操作名称),除去固体小颗粒。再向滤液加入活性炭,除去水样中的颜色和异味,该过程属于________变化(填“物理”或“化学”)。
⑵为了判断⑴中得到的是硬水或软水,可加入________进行检验。
⑶饮用水需通过消毒,X是一种新型的自来水消毒剂,工业上制取X 的化学方程式为:Cl2 + 2 NaClO2 = 2 NaCl + 2 X,则X的化学式为________ 。
过滤物理肥皂水ClO2 【解析】 (1)由于过滤是除去液体中不溶性固体的操作,所以,将水样静置一段时间后进行过滤,除去固体小颗粒;活性炭有吸附性,能除去水样中的颜色和异味,该过程没有新物质生成,属于物理变化; (2)为了判断(1)中得到的是硬水或软水,可加入肥皂水进行检验。泡沫多的是软水,泡沫少、有浮渣的是硬水; (3)根据质量守恒定律,反应的化学方程式为:Cl2+2NaC...查看答案和解析>>
科目: 来源:仁爱版化学九年级上册5.2质量守恒定律练习题 题型:填空题
实验室一瓶新购进的浓硫酸,其标签的部分内容如图所示.

(1)若该瓶硫酸还没有开封使用,瓶内溶液的质量为________ g.
(2)若要配制9.8%的稀硫酸400g,则需用该浓硫酸________mL(计算结果保留至0.1).
(3)配制稀硫酸的过程中,除了用到量筒、胶头滴管、烧杯外,还需要用到的仪器可能有________ .
(4)若量取浓硫酸时采用仰视的方法,则配制的溶液溶质质量分数________9.8%(填“>”、“=”或“<”).
(5)若取该9.8%的稀硫酸100g与足量的镁充分反应后,所得溶液的质量为________g.
92021.7玻璃棒>102.2 【解析】 (1)若该瓶硫酸还没有开封使用,则浓硫酸不会吸收空气中的水分,故瓶内溶液的质量为500mL×1.84g/mL=920g; (2)溶液稀释过程中溶质质量不变,设需要98%的浓硫酸的质量为x,则有98%×x=400g×9.8%,解得x=40g,需要浓硫酸的体积=≈21.7mL; (3)将浓硫酸沿着烧杯壁慢慢注入水中,会放出大量的热,为...查看答案和解析>>
科目: 来源:仁爱版化学九年级上册5.2质量守恒定律练习题 题型:填空题
镁在空气中燃烧生成氧化镁,此反应中Mg、O2、MgO的质量比为________.
3:2:5 【解析】 镁和氧气反应的化学方程式为: 2Mg+O22MgO 48 32 80 在此反应中镁、氧气和氧化镁的质量比为48:32:80=3:2:5,故答案为3:2:5。查看答案和解析>>
科目: 来源:仁爱版化学九年级上册5.2质量守恒定律练习题 题型:填空题
常温下,氯酸钾的溶解度较小,在工业上可通过如下转化制得.
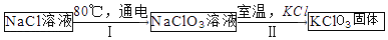
(1)实验室用KClO3制取氧气的化学方程式为________.
(2)反应Ⅰ中,通电时发生的反应方程式为NaCl+3X  NaClO3+3H2↑,则X的化学式为________.
NaClO3+3H2↑,则X的化学式为________.
(3)反应Ⅱ的基本反应类型为________.
(4)该转化中可以循环利用的物质是________(填名称).
2KClO3 2KCl+3O2↑H2O复分解反应氯化钠 【解析】 (l)实验室用KClO3制取氧气的化学方程式为2KClO32KCl + 3O2 ↑;(2)反应I中,通电时发生的反应方程式为NaCl+3X===NaClO3+3H2↑,根据质量守恒定律反应前后原子的种类和个数不变,则X的化学式为H2O;(3)反应Ⅱ中氯酸钠溶液常温下与氯化钾反应生成氯酸钾和和氯化钠,故反应类型为复分解反应...查看答案和解析>>
科目: 来源:仁爱版化学九年级上册5.2质量守恒定律练习题 题型:填空题
对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀。
①致密氧化膜能有效阻止铁锈蚀的原因是________。
②“发蓝”过程的化学方程式如下,式中X的化学式为________。
36Fe + 4NaNO2 + 9NaNO3 + 26H2O = 12X + 13NaOH + 13NH3↑
③为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质。由此可知该零件“发蓝”处理效果不好,因为________(用化学方程式示)。
致密的氧化膜使铁与氧气(或空气)和水隔绝Fe3O4Fe+CuSO4=Cu+FeSO4 【解析】 ①经“发蓝”处理后的铁表面上的蓝黑色氧化膜能够使铁与水和氧气(空气)隔绝,从而有效阻止铁锈蚀; ②根据质量守恒定律,反应前后原子的种类和数目不变,反应前:Fe原子数目为36,Na原子的数目为13,N原子的数目为13,O原子的数目为57,H原子的数目为52;反应后:Fe原子数目为0,Na...查看答案和解析>>
科目: 来源:仁爱版化学九年级上册5.2质量守恒定律练习题 题型:填空题
如图是燃料在使用过程做的碳循环示意图:

(1)化石燃料除了煤、石油外,还有________,煤燃烧会产生造成酸雨的污染气体是________(写化学式);
(2)利用海水进行碳储存,可以缓解温室效应,除了CO2外,温室气体还有________(写出一种物质的化学式);工业上也可用石灰乳(主要成分氢氧化钙)吸收CO2, 其反应方程式为________;
(3)科学家采取“组合转化”技术,将CO2转化为化工原料,其反应的化学方程式:2CO2+6H2  X+4H2O,则X的化学式为________;
X+4H2O,则X的化学式为________;
(4)生物燃料(如酒精)可来源于植物体,写出酒精燃烧的化学方程式:________;结合如图信息,从碳循环角度说出生物燃料的优点有________;
(5)相较以上燃料,目前最理想的清洁燃料是________(写化学式).
天然气 SO2O3Ca(OH)2+CO2=CaCO3↓+H2OC2H4C2H5OH+3O2 2CO2+3H2O节约石油,减少空气污染H2 【解析】 (1)三大化石燃料是煤、石油、天然气;煤燃烧后产生造成酸雨的气体是二氧化硫,化学式为:SO2; (2)造成温室效应的气体有二氧化碳(CO2)、臭氧(O3)、甲烷(CH4)等;反应物是氢氧化钙和二氧化碳,生成物是碳酸钙和水,所以方程式是...查看答案和解析>>
科目: 来源:仁爱版化学九年级上册5.2质量守恒定律练习题 题型:计算题
某兴趣小组为测定一包石灰石样品中碳酸钙的质量分数,进行实验:往12克的固体样品中不断加入稀盐酸,直到没有气泡产生,共用去稀盐酸100克。测得相关数据如图所示:

注:①该反应中,样品中的杂质不参加反应,碳酸钙完全反应。②计算结果保留一位小数。
(1)根据质量守恒定律,反应生成二氧化碳的质量为________g.
(2)计算该样品中碳酸钙的质量分数________.(写出计算过程)
4.4g83.3% 【解析】 试题根据质量守恒定律,反应前后物质的总质量不变,生成二氧化碳的质量为100g+12.0g107.6g=4.4g;设样品中碳酸钙的质量为x, 则CaCO3+ 2HCl ==CaCl2 + H2O + CO2↑ 100 44 x 4.4g 100/x=44/4.4g x=10g 样品中碳酸钙的含量为10g÷12.0g×100%≈8...查看答案和解析>>
科目: 来源:仁爱版九年级上册化学 3.1构成物质的微粒单元检测题 题型:单选题
类推是学习中常用的思维方法.现有以下类推结果,其中错误的是( ) ①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应:②氯化钠的水溶液显中性,所以盐溶液一定显中性;③分子可以构成物质,物质一定是由分子构成的;④碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的一定是碳酸盐.
A. ①②③④ B. 只有①②③ C. 只有②③④ D. 只有①
A 【解析】 试题氢氧化钠和二氧化碳反应生成盐和水,但不属中和反应,①错误;碳酸钠溶液呈碱性,②错误;构成物质的粒子有分子、原子和离子,③错误;活泼的金属也能与稀盐酸反应产生气泡,④错误。故选A。查看答案和解析>>
科目: 来源:仁爱版九年级上册化学 3.1构成物质的微粒单元检测题 题型:单选题
两种物质发生反应的微观示意图如图所示,下列说法正确的是( )

A. 反应前后元素的化合价一定改变 B. 该反应属于分解反应
C. 反应前后原子的数目发生改变 D. 该图可示意CO与O2的反应
A 【解析】 A、该反应中有单质参加反应,生成了化合物,故中元素的化合价一定发生改变,故正确; B、该反应是由两种物质反应生成一种物质,符合化合反应的特点,故不是分解反应,故错误; C、原子是化学变化中的最小微粒,反应前后原子的数目、种类都不变,故错误; D、可能表示氧气,但是不可能表示一氧化碳,故错误。故选A。查看答案和解析>>
科目: 来源:仁爱版九年级上册化学 3.1构成物质的微粒单元检测题 题型:单选题
如图是初中化学中几个重要实验,有关该几个实验的说法错误的是( )
A.  实验中热水的作用是隔绝氧气和提供热量
实验中热水的作用是隔绝氧气和提供热量
B.  实验中左边试管中铁钉生锈而右边试管中铁钉不生锈,可证明铁生锈的条件之一是与氧气接触
实验中左边试管中铁钉生锈而右边试管中铁钉不生锈,可证明铁生锈的条件之一是与氧气接触
C.  实验可证明分子是不断运动的
实验可证明分子是不断运动的
D.  实验中下层蜡烛先熄灭,上层蜡烛后熄灭,能证明二氧化碳的密度比空气大且不能燃烧,也不能支持燃烧
实验中下层蜡烛先熄灭,上层蜡烛后熄灭,能证明二氧化碳的密度比空气大且不能燃烧,也不能支持燃烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com