
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:单选题
潍坊有丰富的海洋资源,氯化钠占整个海洋盐类的80%以上。下列有关氯化钠的说法正确的是( )
A. 室温下的氯化钠饱和溶液不能再溶解氯化钾
B. 取出部分上层溶液,可将接近饱和的氯化钠溶液变为饱和
C. 可用水鉴别氯化钠和氢氧化钠
D. 将100 g质量分数为20%的氯化钠溶液稀释为10%,所用的仪器只有烧杯、量筒、玻璃棒
C 【解析】 A、一定温度下,一种物质的饱和溶液还能继续溶解其它物质,室温下的氯化钠饱和溶液还能再溶解氯化钾,故选项说法错误;B、溶液具有均一性,取出部分上层溶液,接近饱和的氯化钠溶液仍为不饱和溶液,故选项说法错误;C、氯化钠溶于水温度几乎不变,氢氧化钠溶于水温度升高,可以用水鉴别,故选项说法正确;D、利用浓溶液配制稀溶液,采用的加水稀释的方法,其操作步骤是计算、量取、溶解,所用的仪器...查看答案和解析>>
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:单选题
有100 g 10%的盐酸溶液,要使其溶质质量分数增大一倍,应采取的方法是(提示:盐酸易挥发)( )
A. 把溶液的量倒掉一半 B. 与200 g 25%的盐酸混合
C. 溶质的质量增大一倍 D. 蒸发掉溶剂的质量是原溶液质量的一半
B 【解析】 A、溶液具有均一性,把溶液的量倒掉一半,溶质质量分数不变,该选项说法不正确;B、将100g10%的盐酸与200g25%的盐酸混合时,溶质质量分数= ×100%=20%,该选项说法正确;C、设加入溶质质量为x,×100%=20%,x=12.5g,该选项说法不正确;D、由于盐酸具有挥发性,蒸发掉溶剂的同时,溶质也会挥发,故选项采用的方法不正确。故选B。查看答案和解析>>
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:单选题
下列实验能用下图表示的是( )
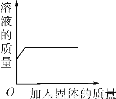
A. 向硝酸铜溶液中加入铁粉
B. 向过氧化氢溶液中加入二氧化锰
C. 向一杯接近饱和的石灰水中加入氧化钙
D. 向不饱和的硝酸钾溶液中加入硝酸钾
D 【解析】 A、铁和硫酸铜溶液反应生成铜和硫酸亚铁,溶液的质量不断减少,当反应完毕后质量不变为一定值,故A错误;B、向过氧化氢溶液中加入二氧化锰,生成水和氧气,生成的氧气逸出,且二氧化锰难溶于水,所以溶液的质量不断减少,当反应完毕后质量不变为一定值,故B错误;C、氧化钙和水反应生成氢氧化钙,水的质量减少,且反应放出热量,当恢复到反应前的温度之后,溶液中的溶质有可能增加,也又可能减小,...查看答案和解析>>
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:单选题
电解氢氧化钠稀溶液与电解水的原理均可表示为:2H2O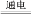 2H2↑+O2↑。电解一定质量氢氧化钠稀溶液的过程中,下列说法正确的是( )
2H2↑+O2↑。电解一定质量氢氧化钠稀溶液的过程中,下列说法正确的是( )
A. 溶液氢氧化钠的质量分数减小 B. 溶液中氢元素质量分数减少
C. 溶液中钠元素质量变大 D. 溶液中氢、氧元素质量比不变
B 【解析】 A、电解氢氧化钠稀溶液,水电解为氢气和氧气,溶液质量减少,氢氧化钠的质量分数增大,故A错误;B、水电解为氢气和氧气,溶液中氢元素质量减少,溶液中氢元素质量分数减少,故B正确;C、根据质量守恒定律,钠元素质量不变,故C错误;D、氢氧化钠中氢氧元素质量比1:16,水中氢氧元素质量比为1:8,因此水电解后溶液中氢、氧元素质量比改变,故D错误。故选B。查看答案和解析>>
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:填空题
写出下列溶液中溶质的化学式。
(1)澄清石灰水:_________;(2)硫酸铜溶液:_________;(3)碘酒_________; (4)医用消毒酒精:_________。
Ca(OH)2 CuSO4I2CH3CH2OH 【解析】 澄清石灰水中的溶质是氢氧化钙,其化学式为Ca(OH)2; 硫酸铜溶液中溶质是硫酸铜,化学式为CuSO4; 碘酒溶液中溶质是碘,化学式为:I2; 医用消毒酒精中溶质是酒精,化学式为CH3CH2OH。查看答案和解析>>
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:填空题
用“饱和”和“不饱和”填空。
(1)把硝酸钾晶体放到硝酸钾溶液里,晶体减少,则原硝酸钾溶液为_________溶液。
(2)将常温下配制的硝酸钾饱和溶液升温到80 ℃,则变成_________溶液。
(3)在10 ℃时,硝酸钾溶液中含有少量硝酸钾晶体,则该溶液为硝酸钾的_________溶液。
(4)将50 ℃时接近饱和的硝酸钾溶液降温到10 ℃,则溶液变为硝酸钾的_________溶液。
(5)在20 ℃时硝酸钾的饱和溶液中加入5 g水,则溶液变为硝酸钾的_________溶液。
不饱和不饱和饱和饱和不饱和 【解析】 (1)把硝酸钾晶体放到硝酸钾溶液里,晶体减少,说明原溶液还能继续溶解硝酸钾,则原硝酸钾溶液为不饱和溶液; (2)硝酸钾的溶解度随温度的升高而增大,所以将常温下配制的硝酸钾饱和溶液升温至80℃,则变为不饱和溶液; (3)在10℃时的硝酸钾溶液中含有少量硝酸钾晶体,则该溶液为硝酸钾的饱和溶液; (4)硝酸钾的溶解度随温度的降低而减小,...查看答案和解析>>
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:填空题
下表为氯化钠和氯化铵在不同温度时的溶解度,回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)由表中数据可知,溶解度随温度变化较大的物质是______。
(2)20 ℃时,100 g水最多只能溶解NaCl______g,氯化钠与氯化铵溶解度相等的温度在______之间。
(3)向烧杯中加100 g水和50.0 g氯化铵配成50 ℃的溶液,再冷却到20 ℃,烧杯中析出固体______ g。
NH4Cl36g10~20℃12.8g 【解析】 试题(1)据表格数据分析,溶解度随温度差距较大的是氯化铵;(2)溶解度是指在一定温度下,100g水所能溶解溶质的质量,据表格可知20℃时只能溶解氯化钠36.0g;10℃至20℃之间,氯化钠与氯化铵溶解度有可能相等;(3)据表格数据,50℃时,溶解度为50.4,g说明此事50.0g氯化铵完全溶解,20℃溶解度为37.2g说明此时100g水...查看答案和解析>>
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:填空题
实验室需要配制50 g溶质质量分数为4%的氢氧化钠溶液,所需固体氢氧化钠的质量为2g,主要操作步骤是:_____、_____、_____、_____。在溶解过程中用玻璃棒搅拌,其作用是_____。在量取水的过程中,某同学仰视读数,会使所配制的溶液中溶质质量分数_____ (填“偏大”“偏小”或“不变”)。
计算称量量取溶解加速溶解偏小 【解析】 配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解;在溶解操作中,玻璃棒起到搅拌以加快氢氧化钠溶解速率的作用;用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使所配制的溶液中溶质质量分数偏小。查看答案和解析>>
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:填空题
如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
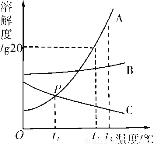
(1)P点含义是_________。
(2)t2 ℃时,将15 g A物质放入50 g水中,充分溶解后,形成溶液的质量为_________。
(3)若A物质中含有少量的B物质,提纯A物质的方法是_________ (填“降温结晶”或“蒸发结晶”)。
(4)t3℃时,将A、B、C三种物质的饱和溶液降温到t1℃,三种溶液中溶质的质量分数由大到小的顺序为_________。
t1 ℃时,A、C两物质的溶解度相等60g降温结晶B>A>C 【解析】 ⑴在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。P点含义t1℃时,A、C两物质的溶解度相等;⑵溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。t2℃时,将15g A物质放入50g水中,充分溶解后,溶质是10g,形成溶液的质量为60g;⑶A的溶解度受温度影响较大,且随温度降低而减小,降温时会结晶析...查看答案和解析>>
科目: 来源:广东省2019届九年级化学:第九单元测试卷 题型:简答题
根据物质的溶解度和溶解过程的有关知识回答下列问题:
(1)20 ℃时,34 g KCl溶解在100 g水中恰好达到饱和,则该温度下,KCl的溶解度为_____。
(2)相同条件下,碘难溶于水,高锰酸钾易溶于水,说明固体物质的溶解能力与_____有关;碘难溶于水而易溶于汽油,说明固体物质的溶解能力与_____有关。此外,你认为固体物质的溶解能力还与_____条件有关。
(3)在试管中加入NaOH固体,加入少量蒸馏水溶解,用手触摸试管外壁,你会感觉到试管外壁_____;用X固体代替NaOH重复上述操作,若试管外壁变冷,则加入的X固体可能是_____ (填化学式)。
34g溶质的性质溶剂的性质外界的温度发热NH4NO3 【解析】 (1)20°C时,34 g KCl溶解在100 g水中恰好达到饱和,则该温度下,KCl的溶解度为34g; (2)相同条件下,碘难溶于水,高锰酸钾易溶于水,说明固体物质的溶解能力与溶质的性质有关;碘难溶于水而易溶于汽油,说明固体物质的溶解能力与溶剂的性质有关;此外固体物质的溶解能力还与外界的温度有关; (3)固体...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com