
科目: 来源:江苏省扬州市2019届九年级上学期期中考试化学试卷 题型:单选题
下列关于空气的说法中错误的是
A. 空气是人类宝贵的自然资源 B. 空气中的氮气常用作保护气
C. 空气中的稀有气体常用作灭火剂 D. 空气中的氧气的主要来自植物的光合作用
查看答案和解析>>
科目: 来源:江苏省扬州市2019届九年级上学期期中考试化学试卷 题型:单选题
原子序数为92的铀(U)是一种核原料,该元素一种原子的质子数和中子数之和为238,下列关于该原子的说法不正确的是
A. 该元素为金属元素 B. 核外电子数为92
C. 相对原子质量为238 D. 核电荷数为238
查看答案和解析>>
科目: 来源:江苏省扬州市2019届九年级上学期期中考试化学试卷 题型:多选题
一种新型火箭推进剂在火箭发射过程中,发生反应的微观过程如图所示。下列说法错误的是
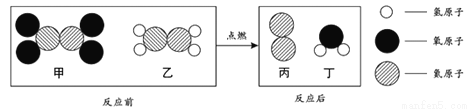
A. 反应前后分子个数没有改变 B. 反应前后原子种类不变
C. 反应后氧元素质量减小 D. 丁是氧化物
查看答案和解析>>
科目: 来源:江苏省扬州市2019届九年级上学期期中考试化学试卷 题型:多选题
取4份等质量的KClO3,向其中3份中分别加入少量等质量的KMnO4、MnO2和Mn,分别在某温度下加热至质量不再改变,测定收集到的氧气质量。然后将剩余固体溶于足量水中,添加过物质的组别中均有相同组成的不溶物。测定结果如下:
组别 | ① | ② | ③ | ④ |
加入物质 | 无 | KMnO4 | MnO2 | Mn |
收集到的氧气质量 /g | 0 | m1 | m2 | m3 |
不溶物的质量 /g | 0 | w1 | w2 | w3 |
(提示:Mn在加热条件下会与氧气反应生成二氧化锰,本题中各反应前后所涉及的含钾元素的化合物均可溶于水,已知m1>m2>m3。)下列说法一定正确的是
A. 不加入其他物质时,KClO3不能发生分解反应
B. KMnO4是KClO3分解制氧气效果最好的催化剂
C. 3种物质的加入都有利于KClO3分解制氧气
D. 残留不溶物的质量关系为w1<w2<w3
查看答案和解析>>
科目: 来源:江苏省扬州市2019届九年级上学期期中考试化学试卷 题型:填空题
“见著知微,见微知著”是化学的思维方法。
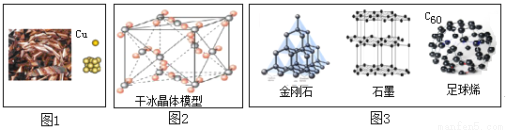
(1)化学上“Cu”能表示铜元素,表示一个铜原子,还能表示_____。化合物中,铜元素常呈现+1价或+2价,写出铜的对应价态氧化物的化学式为_____、_____。
(2)干冰是二氧化碳的固体形式。熔点是-57℃,沸点是-78.5℃,干冰在室温环境中由于温差太大,吸收大量的热使分子间的距离迅速增大,从固态不经过液态直接变成气态。
①干冰由_____构成。
②干冰是优良的制冷剂,可用来保藏易腐烂的食品,其原因是_____。
A.干冰是固体 B.干冰升华时吸热 C.干冰升华后无残留 D.干冰比空气重
③ 镁条在二氧化碳中燃烧生成氧化镁和黑色粉末,写出反应的化学方程式____。
(3)足球烯是近些年科学家们发现的一类物质,因形状像足球而得名,其中一种化学式是C60(如图3)。
①物质的性质决定用途,用途反映物质的性质。金刚石是天然存在最硬的物质,因此金刚石可以用作____。石墨很软,有滑腻感、优良的导电性,因此石墨可以用于____。
②金刚石、石墨等物质物理性质有较大差异的原因______。
③下列关于C60的说法正确的是_____。
A.它的一个分子中含有60个碳原子 B.相对分子质量是720 C.它是一种单质
查看答案和解析>>
科目: 来源:江苏省扬州市2019届九年级上学期期中考试化学试卷 题型:简答题
以下是某小朋友血液中某些元素检测结果的报告单(部分),回答以下问题:
序号 | 检测项目 | 结果 | 参考值 |
1 | 锌 | 7.7 | 11~22 μmol•L-1 |
3 | 铁 | 17.8 | 9.0~21.5 μmol•L-1 |
4 | 钙 | 2.5 | 2.2~2.7 μmol•L-1 |
6 | 铅 | 0.28 | 0~0.48 μmol•L-1 |
(1)该小朋友血液中缺乏的微量元素是__ (填元素符号);缺乏此元素会____;检测项目中属于有害元素的是___(填元素名称)。
(2)根据检测结果,医生建议她每天补充6.5mg的锌,小朋友的爸爸买了补锌剂(如图):

葡萄糖酸锌中含有___种元素,其中碳元素和氢元素的质量比是__。试通过计算说明该小朋友每天一共应该口服__支葡萄糖酸锌口服液。
查看答案和解析>>
科目: 来源:江苏省扬州市2019届九年级上学期期中考试化学试卷 题型:简答题
水是人们日常生活中非常熟悉的物质之一,我们应该多角度进行研究。
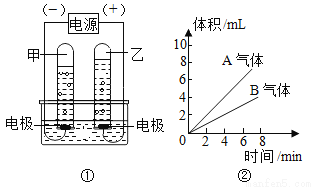
(一)水的组成——电解水
(1)电解一段时间后,将两极产生的气体的体积与时间的关系绘制成图②所示的平面直角坐标系,回答:
①由图①、②看出,A气体是__(填化学式),B气体在电源的___极。
②0~8min A、B气体的体积比为________。
(2)微观该反应中发生分解的微粒是____。
(3)电解水的化学方程式为__________。
(二)水的净化
小刚收集到一瓶浑浊的长江水,他要模拟自来水厂的净水过程,最终制成自来水。其实验过程如图所示。请回答以下问题。
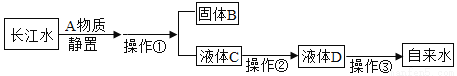
(4)操作①的名称是_________;该操作中用到的玻璃仪器有烧杯、玻璃棒和_______。
(5)操作②主要是除去水中的异味和色素,应选用的物质是_____。
(6)小刚发现经净化后的D是硬水,日常生活中常用___ 的方法使硬水软化。
(三)水的性质、变化和用途
(7)下列是有关水的性质、变化和用途的描述:
a.通常为无色、无味的液体
b.没有水,人和动物就无法生存
c.水是常用的灭火剂
d.氢气在氧气中能燃烧生成水
e.水可与氧化钙(CaO)反应生成氢氧化钙。
①其中属于水的物理性质的有________(填序号,下同);属于水的化学性质的有________;属于水的用途的有__________。
②写出上文描述中体现水的化学性质的化学方程式____。
查看答案和解析>>
科目: 来源:江苏省扬州市2019届九年级上学期期中考试化学试卷 题型:实验题
磷(包括红磷和白磷)是初中化学实验中经常使用的物质,化学小组的同学以“磷的燃烧”为主题设计并整理了以下三组实验,请你参与完成:
(1)探究空气中氧气的含量:
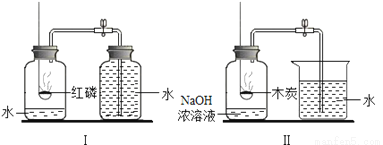

实验Ⅰ和Ⅱ装置中,能完成测定空气中氧气体积分数的是_______(填序号)。红磷燃烧的化学反应方程式为_______________。
(2)探究物质燃烧的条件:

①通过实验Ⅰ得到:可燃物燃烧的必备条件是____________。
②改进后的装置Ⅱ中可看到的现象是_________。
③将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如装置Ⅲ所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是________。

(3)利用图IV所示装置探究化学反应过程中物质总质量的变化。实验过程气球的作用是_________。
查看答案和解析>>
科目: 来源:江苏省扬州市2019届九年级上学期期中考试化学试卷 题型:科学探究题
潜水艇里要配备氧气的再生装置,以保证长时间潜航。有以下几种制取氧气的方法:
①加热高锰酸钾 ②用二氧化锰分解过氧化氢 ③常温下过氧化钠固体(化学式为Na2O2)与二氧化碳反应生成碳酸钠和氧气。
(1)写出方法①和②的化学方程式___,______。
(2)事实证明最适合在潜水艇里制氧气的是方法是③,与其它两种方法相比,这种方法的优点是____(填序号)。
A. 无需加热,常温下就可自动完成,使用方便
B. 能将人呼吸产生的二氧化碳转变为呼吸所需的氧气
C. 生成等质量的氧气,药品用量少
D. 生成物没有毒,不污染环境
探究一:某同学设计了下图所示的实验装置来探究过氧化钠和二氧化碳反应产生氧气。
(查阅资料)已知过氧化钠是一种浅黄色固体粉末,过氧化钠还能与水反应生成氢氧化钠和氧气,方程式为:2Na2O2 + 2H2O == 4NaOH + O2↑。
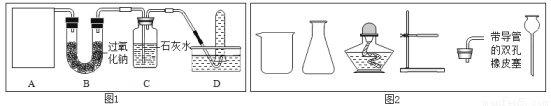
(3)A是二氧化碳气体的发生装置,装配该装置时,应选用的仪器除带导管的双孔橡皮塞外,还需要的仪器有(填名称,从图2中选择)_____、_____。实验室制取二氧化碳的化学方程式______。
(4)用图1中装置D所示的方法收集氧气,其依据是_______;检验D装置试管内收集到的气体是否是氧气的方法是_________。
(5)B中反应方程式是___________。
石灰水的作用是①观察气体的流速,②判断过氧化钠与二氧化碳何时完全反应, ③_____________。
(6)你认为该方案_______(填“能”或“不能”)证明过氧化钠与二氧化碳反应生成氧气,理由是_______。
探究二:小红同学利用过氧化钠能和水反应的原理来测定Na2O2的纯度并用所得的氧气来确定某物质的组成
(实验步骤):
①称取20g样品置于装置中(整个装置的质量为45g)。
②一次性加入20mL蒸馏水后将装置放置在电子天平上,观察显示数字的变化,并记录(数据见下表)。
③进行计算。
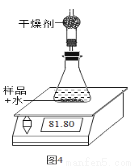
时间/s | 60 | 120 | 180 | 240 | 300 |
天平示数/g | 83.82 | 82.43 | 82.15 | 81.80 | 81.80 |
(7)装置中干燥剂的作用是______;如果没有干燥剂,测定结果会_____(选填“偏大”、“ 偏小”、“ 不变”)。
(8)取一定质量的某物质在上述所得的氧气中完全燃烧测得生成二氧化碳4.4克和水1.8克,通过计算确定该物质中各元素的原子的个数比_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com