
科目: 来源:不详 题型:单选题
| A.Al>Mg>Zn | B.Al>Zn>Mg | C.Mg>Al>Fe | D.Mg=Al=Zn |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.8:17 | B.11:14 | C.14:11 | D.14:111 |
查看答案和解析>>
科目: 来源:文昌一模 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 数据记录时间 | t1 | t2 | t3 | t4 |
| 剩余物质质量/g | 46.50 | 46.40 | 46.38 | 46.38 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀盐酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 实验序号 | 1 | 11 | 111 |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
查看答案和解析>>
科目: 来源:山东省期末题 题型:单选题
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:模拟题 题型:计算题
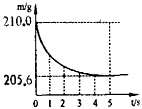
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com