
科目: 来源:不详 题型:单选题
| 物 质 | CaCO3 | Ca(OH)2 | NH3 | NaOH |
| 市场参考价(元/公斤) | 1.8 | 2.0 | 6.5 | 11.5 |
| A.CaCO3 | B.Ca(OH)2 | C.NH3 | D.NaOH |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.Na2S | B.NaHS | C.Na2S和NaHS | D.Na2S和NaOH |
查看答案和解析>>
科目: 来源:门头沟区一模 题型:问答题
查看答案和解析>>
科目: 来源:道里区一模 题型:单选题
| A.只含CaC03 | B.可能含CaC03、MgC03 |
| C.只含K2C03 | D.可能含K2C03、MgC03 |
查看答案和解析>>
科目: 来源:安丘市 题型:问答题
| 浓度限值(mg/m3) |
| 一级标准 二级标准 三级标准 0.15 0.50 0.70 |
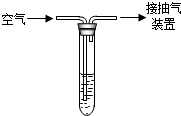
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:定西 题型:问答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com