
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:单选题
下列操作,现象和结论都正确的是( )
序号 | 操作 | 现象 | 结论 |
A | 向某固体滴加稀盐酸 | 有气泡产生 | 该固体是碳酸盐 |
B | 在空气中加热除去碳粉中的杂质铜粉 | 粉末完全变黑 | 碳粉中杂质已除尽 |
C | 向氢氧化钠溶液中滴加稀盐酸溶液 | 没有明显现象 | 氢氧化钠与稀盐酸不发生反应 |
D | 用氯化钾溶液进行导电性试验,观察小灯泡是否变亮 | 小灯泡变亮 | 氯化钾溶液中存在自由移动的离子 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:单选题
下列实验设计不能达到其对应实验目的的是( )
选项 | 实验 | 现象 | 结论 |
A |
| 铁片表面有少量气泡,锌丝表面有较多气泡 | 说明铁与锌的活泼性 Fe<Zn |
B |
| 硫磺在空气中燃烧发出微弱的淡蓝色火焰,在氧气中发出明亮的蓝紫色火焰 | 说明硫磺在氧气中燃烧更旺盛 |
C |
| ①试管中没有明显现象 ②试管中铁钉生锈 | 说明铁生锈需要水 |
D |
| 试管中白磷燃烧,热水中白磷不燃烧 | 说明燃烧需要氧气 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:填空题
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等,亚氯酸钠受热易分解。
(1)亚氯酸钠(NaClO2)在酸性溶液中生成HClO2而发生分解,分解的化学方程式:5HClO2═4X↑+HCl+2H2O。HClO2读作____,其中氯元素的化合价为___;X的化学式___。
(2)以氯酸钠(NaClO3)等为原料可以制备亚氯酸钠。氯酸钠受热会分解,其生成物与氯酸钾分解的生成物相似。除此以外,氯酸钠与氯酸钾还具有一些其它相似的化学性质。
①试写出氯酸钠受热分解的化学方程式___。
②试分析氯酸钠与氯酸钾具有相似化学性质的原因___。(填字母)
A 都含氯元素 B 都含氧元素 C 都含ClO3- D 以上都是
查看答案和解析>>
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:科普阅读题
可燃冰是在低温和高压条件下形成。可燃冰外观像冰,主要含有甲烷水合物,其组成可表示为CH4·nH2O,还含少量二氧化碳等气体。可燃冰具有能量高、燃烧值大等优点。2017年5月,中国首次海域天然气水合物(可燃冰)试采成功,成为全球第一个稳定开采可燃冰的国家。可燃冰开采困难重重,原因之一是可然冰极不稳定易爆炸,当甲烷气体涌入大气层,会产生比二氧化碳更为严重的温室效应。置换法是开采方法之一,将CO2液化后进入1500米以下的洋面,就会生成二氧化碳水合物沉入海底,因CO2较甲烷易于形成水合物,因而就可能将甲烷水合物中的甲烷分子置换出来。
(1)一个甲烷分子中含有____个原子。32g甲烷完全燃烧后可以生成___g二氧化碳。
(2)下列有关说法正确的是__。
A 可燃冰的开采不存在任何困难
B 可燃冰是一种前景广阔的燃料
C 能产生温室效应的气体除二氧化碳外,还有甲烷等气体
(3)某种可燃冰的组成为CH4·nH2O,其中CH4与H2O的质量比是1:9,则该可燃冰中n=__。
(4)一定条件下,甲烷与二氧化碳反应是回收处理二氧化碳的一种方法,其产物是一种单质和一种氧化物,都有可燃性,请写出该反应的化学方程式____。
查看答案和解析>>
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:实验题
某兴趣小组在常温和其它相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口放置于空气中,烧杯中物质质量随时间变化如下表,请回答下列问题。
时间 | 质量/g | |||||
水 | 饱和石灰水 | 稀盐酸 | 浓硫酸 | 氯化钠浓溶液 | 氯化钙浓溶液 | |
1天 | 8.16 | 8.37 | 8.64 | 11.18 | 9.38 | 10.25 |
2天 | 5.76 | 5.94 | 6.69 | 12.25 | 8.47 | 10.33 |
(1)下列图示能反映水在空气中放置时发生变化的微观示意图是______(填字母编号)。图中 表示氧原子,
表示氧原子,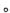 表示氢原子
表示氢原子
(2)为研制一种安全、环保的除湿剂,可选择上表中的(填溶质的化学式)____。
(3)现配置100g 20%的稀硫酸,则需要质量分数为98%(密度为1.84g/cm3)的浓硫酸____ml。(结果保留整数)
(4)为进一步研究稀盐酸敞口久置后浓度变化,其中甲同学猜想稀盐酸浓度可能会变大,理由是_____。
查看答案和解析>>
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:科学探究题
分析、归纳、推理是学习化学的重要方法,请同学们根据下面微观粒子反应(在水溶液中进行反应,水分子已省略)示意图,分析解决下列问题。

(1)图1所用到的稀硫酸是把10ml的浓硫酸和90ml的水混合而成的,但在混合后发现其体积少于100ml,试从微观角度分析其原因:__。
(2)图2发生反应的微观实质是Ca(OH)2溶液中的__(填化学用语)与K2CO3溶液中的(填化学用语)发生反应__;
(3)从图1、图2、图3可以发现,碱溶液中都含___(填化学用语),因此它们具有相似化学性质。试分析图1、图2、图3的反应中,属于碱的共同性质的是__。(填图序号)
(4)写出一种既能与氢氧化钙溶液又能与硝酸钙溶液反应的物质:____(填化学式)。
查看答案和解析>>
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:实验题
硼及其化合物在工业上有很多用途。
(1)硼氢化钠(NaBH4)具有优良的还原性,在化学领域有着广泛的应用。利用硼精矿(主要成分为B2O3,含有少量Al2O3、SiO2、FeCl3等)制取NaBH4的流程如下图。

已知:①B2O3+2NaOH=2NaBO2+H2O;
②偏硼酸钠(NaBO2)易溶于水,不溶于醇,在碱性条件下稳定存在;
③Al2O3、SiO2均可与NaOH溶液反应生成可溶性钠盐。
回答下列问题:
(1)①操作1是____,滤渣主要成分为______(填化学式)。
②写出加快硼精矿溶解速率的措施(写一种)_______。
③除硅铝步骤加入CaO而不加入氯化钙的原因有:_____
I.能将硅、铝以沉淀除去;II.。
(2)单质硼可用于生成具有优良抗冲击性能硼钢,以硼酸(H3BO3)和金属镁为原料可以制备单质硼(B)。其制备过程先后通过两个化学反应,写出相关化学方程式:

①分解反应____
②置换反应____
查看答案和解析>>
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:实验题
具备基本的化学实验技能是学习化学和进行探究活动的基础和保证。下图为粗盐提纯实验中的三个主要操作,请回答:

(1)三个操作均需要用到的一种仪器的名称是____。
(2)粗盐提纯过程中正确的实验步骤顺序是____。(填字母序号)
(3)当A中出现时,停止加热_____。
(4)已知20℃时氯化钠的溶解度为36g,现要溶解7.2g粗盐,至少需要量取_____ml水。(水的密度为1g/cm3)
查看答案和解析>>
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:实验题
下图为实验室中常用装置。
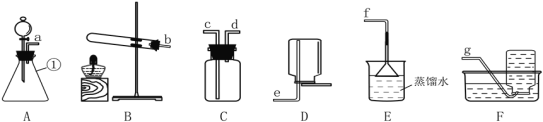
请回答下列问题:
(1)实验室用高锰酸钾制取并收集较纯净的氧气所选用的装置是_____(填装置字母),该反应的化学方程式为__。二氧化锰直接排放会造成环境污染。从充分加热后的上述剩余固体中回收二氧化锰的方法是______、过滤、洗涤和烘干(注:锰酸钾可溶于水)。
(2)夏天温度高,检查装置B的气密性,方法是:连接好仪器,把导管一端放入水中,然后___,观察到有气泡冒出,说明装置气密性良好。
(3)实验室常用锌粒和稀硫酸制取氢气,其反应的化学方程式:______。
(4)实验室制取二氧化碳的化学方程式是______,发生装置选取A的优点_____,若实验室需要制取88g的二氧化碳,则最少需要含80%CaCO3的大理石____g。
(5)通常状况下,氨气是一种无色、有强烈刺激性气味的污染性气体,极易溶解于水形成氨水,相同条件下密度比空气小。常温下实验室可以用浓氨水与生石灰制取氨气。请从上图中选出合适的仪器连接成一套制备并收集氨气的装置,则装置的接口连接顺序是a→____→f,上述实验中,E装置的作用是_____。
查看答案和解析>>
科目: 来源:广东省广州市南沙区2019届九年级下学期学业水平综合测试化学试卷 题型:科学探究题
金属钴(Co)在国防工业中有重要应用。
(1)钴的化学性质与铁相似,与酸反应生成+2价的钴盐,CoCl2溶液为红色。
①请写出金属钴粉与稀盐酸反应的化学方程式:_____。
②预测上述反应发生的现象: _____。
③上述反应后新增的离子为: _____(填化学用语)。
(2)通过废锂电池(主要成份为LiCoO2、炭粉和铝箔)回收可得到草酸钴晶体。在实验室中研究不同条件下Co2+的浸出率(样品质量、加入盐酸体积均相同),结果如下表。从实验结果看,在仅考虑提高Co2+的浸出率的情况下,回答下列问题:
编号 | 温度/℃ | 时间/min | 盐酸浓度/% | 钴浸出率/% |
① | 80 | 120 | 10.5 | 90.82 |
② | 80 | 150 | 8.5 | 100.0 |
③ | 80 | 180 | 10.5 | 100.0 |
④ | 80 | 150 | 5.4 | 80.26 |
⑤ | 70 | 150 | 8.5 | 86.85 |
⑥ | 90 | 150 | 8.5 | 100.0 |
I.本实验研究了哪些因素对钴元素浸出率的影响:____。
II.实验⑤⑥的目的是______。
III.实验为最优反应条件______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com