
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:单选题
在硝酸铜、硝酸银、硝酸镁的混合溶液中加入过量的铁粉,充分反应后再过滤,滤纸上得到的物质是( )
A.铁、铜、银、镁 B.银、铜、铁 C.铜、银 D.镁、银、铜
查看答案和解析>>
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:单选题
下列有关说法错误的是( )
A.根据质量守恒定律18g镁和18g氧气充分反应,一定生成36g氧化镁
B.金(即铜)柔锡柔,合两柔则为刚﹣﹣说明合金的硬度比组成它的纯金属大
C.百炼成钢原理:使生铁中碳等杂质的含量降低,达到钢的标准
D.单质仅含一种元素,但只含有一种元素的物质不一定是单质
查看答案和解析>>
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:单选题
甲、乙、丙、丁4种物质在密闭容器中充分反应,测得反应前后各物质的质量如下表所示。下列说法不正确的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 30 | 3 | 6 | 8 |
反应后质量/g | 16 | m | 4 | 24 |
A.该反应是化合反应 B.丁可能是单质
C.参加反应的甲、丙的质量比是7:1 D.乙可能是反应的催化剂
查看答案和解析>>
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:单选题
下列图像一定能正确反映其对应关系的是
|
|
|
|
A红磷在装有空气的密闭集气瓶中燃烧 | B一定里的炭在密闭容器中与足量的氧气充分反应 | C向两份完全相同的稀盐酸中分别加入过量的锌粉、镁粉 | D加热一定质里的氯酸钾与二氧化锰的混合物 |
A.A B.B C.C D.D
查看答案和解析>>
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:单选题
气体M(含CO、CO2中的一种或两种)。为探究M的成分,设计如图所示实验。下列说法不正确的是( )
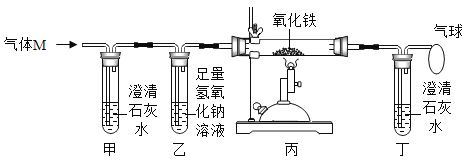
A.若甲中溶液变浑浊,则M中一定含有CO2
B.若撤走丁装置,则无法判断M中是否含有CO
C.必须通入气体一段时间后才能点燃酒精喷灯
D.气球用于收集未完全反应的CO,防止空气污染
查看答案和解析>>
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:填空题
化学用语是一种信息丰富、国际通用且比较简明的化学用语,请用化学用语填空:
①2个铁离子_____;
②4个氯分子_____;
③3个磷原子_____;
④2个硫酸根离子_____;
⑤地壳中含量最高的金属元素_____;
⑥氯化铜中铜显+2 价_____;
⑦缺_____能导致侏儒症。
查看答案和解析>>
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:填空题
如图中A、B、C、D、E是四种粒子的结构示意图,请回答下列问题:
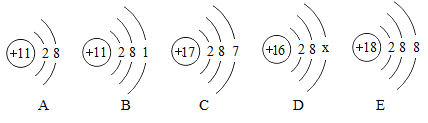
(1)图中A、B、C、D、E共包含_______种元素的粒子;
(2)A、B两种微粒的化学性质是_________(填“相似”、“不同”或“相同”);
(3)若D为硫元素的原子结构示意图,则x=________,该粒子在化学变化中得电子而变成 ________ (用离子符号表示)。
(4)以上微粒中属于稳定结构的原子是___________(填字母)
(5)根据原子结构分析氯元素的最高正价是________.
查看答案和解析>>
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:填空题
如图是CO燃烧的的微观示意图。请回答。
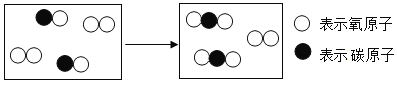
(1)写出该反应的化学方程式_______________________。
(2)结合该变化说明遵循质量守恒定律的原因是在化学反应前后__________________________。
(3)在该反应中参加反应的CO和氧气的质量比为____________。
查看答案和解析>>
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:实验题
小组同学为探究化学变化中质量的变化关系,进行了如图实验,完成下列填空。
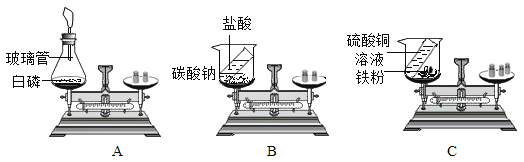
(1)已知碳酸钠与碳酸钙化学性质相似,则B图反应的化学方程式为_____________________;
(2)化学小组同学用如图实验探究质量的变化。充分反应后,天平一定不能平衡的是___(填字母)。
(3)在实验A中,气球的作用是___________________________;
(4) 铁和硫酸铜反应的现象为_____________________,该反应的化学方程式为___________________。
查看答案和解析>>
科目: 来源:福建省泉州市2019-2020学年九年级上学期月考化学试卷 题型:流程题
某品牌电器的废旧电路板中还有Fe、Cu、Ag、Ni(镍,银白色金属)等金属,如下图是某车间回收Cu、Ag、Ni的工艺流程,已知,2Cu+O2 +2H2SO4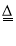 2CuSO4+2H2O。
2CuSO4+2H2O。
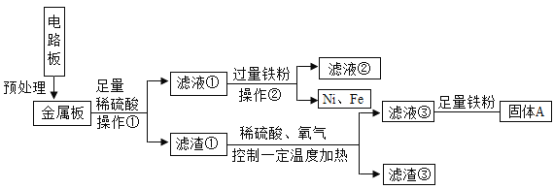
(1)操作①中使用的玻璃仪器除烧杯、玻璃棒外,还需__________;
(2)滤渣③中回收的主要金属是__________;
(3)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱顺序是Ni______Fe(填“>”或“<”)。
(4)滤液③中加入足量铁粉的主要目的是____________,固体A除主要含有铜外,还含有一定量的铁,为了进一步提纯铜,可以向固体A中加入适量的稀硫酸,发生反应的化学方程式为__________________;
(5)滤液①存在的物质除了水和硫酸,还有________________(写名称)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com