
科目: 来源:2018年四川省成都市自主招生化学试卷(二) 题型:单选题
已知:在同温同压下,相同体积的任何气体所含的分子数目都相同:常温下二氧化硫气体和硫化氢气体混合,发生反应生成硫和水。现将常温常压下m个二氧化硫分子和n个硫化氢分子混合,若充分反应后气体的体积是反应前的一半,则m与n的比值是( )
A.1:5 B.1:3 C.1:2 D.1:1
查看答案和解析>>
科目: 来源:2018年四川省成都市自主招生化学试卷(二) 题型:单选题
某黑色固体粉末可能是Fe 、FeO、CuO、C中的一种或几种。为了探究其成分,小明同学按照下图所示流程进行了实验。
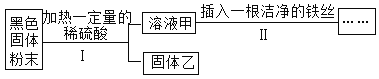
关于该实验有以下说法:
①若溶液甲呈浅绿色,则原黑色固体粉末中一定含有Fe;
②若步骤II中无明显现象,则固体乙中最多只能有四种物质;
③若步骤Ⅱ中有气泡产生,则原固体可能是纯净物也可能是混合物;
④若步骤Ⅱ中有红色固体析出,则固体乙中一定无CuO;
⑤若固体乙呈红色.则原固体中一定含有Fe和CuO。
以上说法中正确的个数是( )
A.1个 B.2个 C.3个 D.4个
查看答案和解析>>
科目: 来源:2018年四川省成都市自主招生化学试卷(二) 题型:单选题
往100gFeCl3和CuCl2的混合溶液中加入铁粉。已知FeCl3会先与铁粉发生反应:2FeCl3+Fe=3FeCl2。下图为加入铁粉的质量与反应后剩余固体的质量关系。下列说法不正确的是( )

A.D点对应纵坐标为6.4
B.B点后溶液的颜色为蓝色
C.该100g溶液中的CuCl2的质量分数为13.5%
D.取DE两点间(不含D)的剩余固体加入盐酸,均有气泡产生
查看答案和解析>>
科目: 来源:2018年四川省成都市自主招生化学试卷(二) 题型:填空题
熟石灰在生产和生活中有广泛的用途。请回答:
(1)熟石灰中金属元素的原子结构示意图是______;
(2)区分熟石灰溶液、氯化钠溶液、稀硫酸的操作及现象是_____________;
(3)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是_________;
(4)某地区土壤呈酸性(含硫酸),可选用熟石灰来改良.则反应的化学方程式是:___________;
(5)用熟石灰粉与草木灰按一定的比例混合可制得高效环保农药“黑白粉”。使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体。
①“黑白粉”比熟石灰更高效,是由于生成了比碱性更强的物质,该反应的化学方程式是______;
②“黑白粉”中可提供植物生长和抗倒伏的营养元素是_________(填元素符号)。
查看答案和解析>>
科目: 来源:2018年四川省成都市自主招生化学试卷(二) 题型:科学探究题
一定条件下,CO与MgSO4反应会生成三种氧化物。某兴趣小组用如下装置探究该反应。已知:SO2与CO2通入澄清石灰水现象相同;SO2能使KMnO4溶液褪色。

(1)仪器a的名称是_________;CaC2O4中C的化合价是_________;
(2)连接好装置,开始实验前需要对上述装置进行的操作是________;
(3)装置A中充分反应后残留的固体是一种常见补钙剂的有效成分, 则该化学方程式是_________;
(4)实验时观察到装置C中紫红色褪去,装置E中溶液变浑浊,则装置B中反应的化学方程式是_______;装置D的作用是__________;
(5)该装置的不足之处是________。
查看答案和解析>>
科目: 来源:2018年四川省成都市自主招生化学试卷(二) 题型:填空题
煤是重要的能源,也是生产化工产品的重要原料。随着人类社会的飞速发展,化石能源大量消耗,人类已经面临较严重的能源危机。为此,提高能源的利用率和开发更多的新能源显得相当重要。下图是煤化工产业链的一部分。
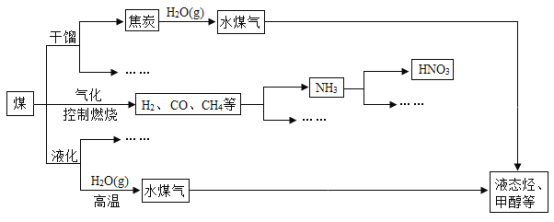
请回答:
(1)任意列举两种新能源______;
(2)上述处理煤的过程属于______(选填“物理”或“化学”)变化。
(3)煤和石油等化石燃料燃烧排放的大量二氧化碳会引起全球气候变暖。一种新的处理方法是将二氧化碳气体通人含有长石(地壳中最常见的矿石,含量高达60)成分的水溶液里,其中一种反应的化学方程式是:KAlSi3O8+CO2+2H2O=KHCO3+X↓+3SiO2↓,则X的名称是______;
(4)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
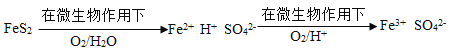
这种脱硫技术称为微生物脱硫技术。该技术的两步反应的化学方程式依次是:______。
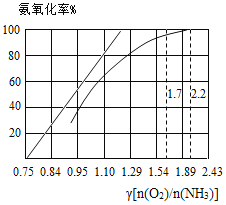
(5)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨—空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上γ[n(O2)/n(NH3)]=1.25,实际生产要将γ值维护在1.7 ~2.2之间,原因是________。
[温馨提示:n(O2)可以认为是表示氧气分子堆积数目的一种物理量,即n(O2)值越大,说明氧分子数目越多]
查看答案和解析>>
科目: 来源:2018年四川省成都市自主招生化学试卷(二) 题型:流程题
过氧化钙晶体(CaO2?8H2O)较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒,也在食品、牙膏、化妆品等制造中用作添加剂,还可以作为鱼池增氧剂。现以贝壳为原料制备CaO2的流程如下:
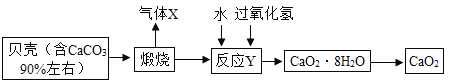
(1)将过氧化钙晶体与溶液分离的方法是_________;
(2)我国制碱工业的先驱侯德榜先生为纯碱和氮肥工业技术的发展作出了杰出的贡献。其制备原料有气体X、氨气、精制饱和食盐水,过程主要是先制得小苏打,再过滤并加热分解小苏打制得纯碱。
①实验过程中应该先向精制饱和食盐水中通入__________;其原因是_________;
②请写出制备纯碱第一步发生的化学反应方程式:________;
(3)反应Y不能在较高温度下进行的原因是_________;已知该反应是化合反应,则反应Y的化学方程式是________;获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是_______;
(4)现设计如下实验测定制得的过氧化钙晶体[CaO2?8H2O]中CaO2的质量分数:称取晶体样品25g.加热到220°C充分分解,其产物含有参与反应Y的固体物质和能使带火星木条复燃的气体等(此时所得气体混合物的总质量为1.6g,已知杂质不发生变化),则该晶.体样品中CaO2的质量分数是________。
查看答案和解析>>
科目: 来源:广东省广州市2019-2020学年九年级上学期第一次月考化学试卷 题型:单选题
下列过程中,发生了化学变化的是( )
A.干冰升华 B.从含二氧化硅的沙子中提炼高纯硅
C.海水晒盐 D.从潮湿空气中分离出水蒸气
查看答案和解析>>
科目: 来源:广东省广州市2019-2020学年九年级上学期第一次月考化学试卷 题型:单选题
空气是一种宝贵的资源,下列生产生活中用到的气体不是来自空气的是
A. 作为燃料电池燃料的H2 B. 手于生产氮肥的N2
C. 用于医疗急救的O2 D. 用于飞艇的He
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com