
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:填空题
常见的酸和碱,在现实生活中有广泛的用途。根据所学知识回答:
(1)将氢氧化钠和氢氧化钙暴露在空气中都会变质生成某一类盐,该类盐的阴离子符号是_______。
(2)工业上常用熟石灰和碳酸钠溶液制烧碱的化学反应方程式是_________。
(3)长期不合理使用化肥(例如使用硫酸铵)会使土壤酸化(含有硫酸),熟石灰常用来改良酸性土壤,化学反应方程式是_________。熟石灰可由生石灰与水制得,化学反应方程式是________。该反应的基本类型是______。
(4)浓硫酸常用来干燥某些气体,如:干燥_________等气体,其干燥原理是______。
查看答案和解析>>
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:填空题
某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程见下图:
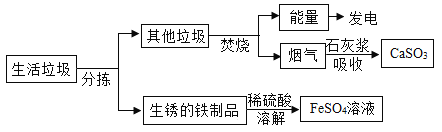
资料1: 垃级焚烧产生的烟气中含有SO2等有害气体。
资料2:FeSO4容易被空气中的O2氧化。
回答下列问题:
(1)石灰浆吸收SO2(性质与CO2相似)的化学反应方程式为____________。
(2)溶解步骤中同时发生的三个化学反应方程式为:Fe+Fe2(SO4)3=3FeSO4、____________、____________。
(3)将所得FeSO4溶液在氮气环境中蒸发浓缩、_______、过滤,得到FeSO4晶体,其中氮气的作用是________。
(4)政府倡导垃圾分类,其好处是(写一点):________________。
查看答案和解析>>
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:填空题
海洋是人类千万年来取之不尽、用之不竭的巨大资源宝库,开发前景广阔。
(1)目前海水淡化的方法很多,在世界范围之内能做到规模化和产业化的主要是膜法和______。高压反渗透膜法淡化海水是利用海水中各成份的_________不同分离出淡水。
(2)2017年5月18日,在中国南海海域实现可燃冰(CH4·nH2O)试采成功,这将使人类能源格局翻开新篇章。

①可燃冰中,水分子形成一种空间笼状结构,甲烷和少量N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于_____(选填“纯净物”或“混合物”)。
②若某种可燃冰中CH4与H2O的质量比是1:9,则该可燃冰中n=_______。
(3)海水“晒盐”
①海水提取食盐的方法主要为“盐田法”,其过程如下;图中②是_____池,下图中的“母液”是氯化钠的_________溶液。(填“饱和”或“不饱和”)
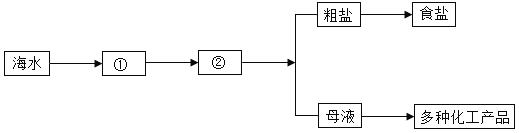
②粗盐纯化。粗盐中含有泥沙、硫酸镁、氯化钙等杂质。将粗盐溶于水,然后通过如下操作即可得到较纯的氯化钠:a过滤;b加过量的Ba(OH)2溶液;c加适量的盐酸;d加过量的Na2CO3溶液;e蒸发。正确的操作顺序是_________(填字母)。
(4)制镁。工业上一般用电解熔融状态的氯化镁制金属镁,若以卤水(含有硫酸镁、氯化钠和氯化钙)为起始原料来制取金属镁。
①从海水中提取镁过程中涉及到的分解反应的化学反应方程式为__________。
②海水本身就是含有MgCl2的溶液,它与通过转化后得到的MgCl2溶液有何不同:_________。
查看答案和解析>>
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:填空题
将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题:
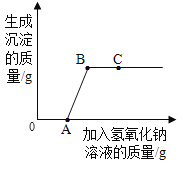
(1)A点处溶液的溶质是__________(化学式)。
(2)请写出AB段发生反应的化学方程式________。
(3)C点处溶液的pH______7(填“>”“=”、或“<”),此处溶液中的溶质为_________(化学式)。
查看答案和解析>>
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:实验题
根据粗盐中难溶性杂质的去除和溶液的配制实验图示回答相关问题:
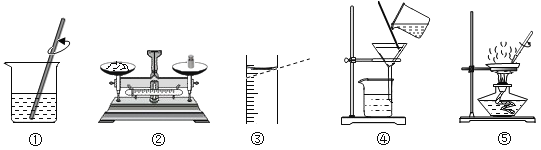
(1)操作④中玻璃棒的作用是_____________。
(2)若按照②③①步骤配制50g16%的NaC1溶液,所配制溶液的溶质质量分数________(填“偏大”、“偏小”或“无影响”)。
(3)操作⑤中停止加热的时间是________。
(4)除去粗盐中难溶性的杂质并计算精盐的产率,其正确操作步骤为________。以下操作中可能会导致精盐产率(产率=精盐质量/粗盐质量×100%)偏小的有_____(填序号)。
A 操作①中有少量溶液溅出烧杯
B 操作③中仰视读数
C 操作④中液面高于滤纸边缘
D 操作⑤中没有使用玻璃棒搅拌
查看答案和解析>>
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:科学探究题
实验设计是化学实验的重要环节。请根据下列实验要求回答相关问题:
(活动与探究)用变量控制方法探究影响物质溶解性的因素。
实验一 | 实验二 |
|
|
(1)实验一目的是探究____对硝酸钾溶解性的影响,在实验中需要保持不变的因素是______。
(2)实验二是探究_______对物质溶解性的影响,该实验中需要控制的变量是温度和________。
查看答案和解析>>
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:填空题
为研究氢氧化钠、氢氧化钙两种溶液的化学性质,进行如下实验。
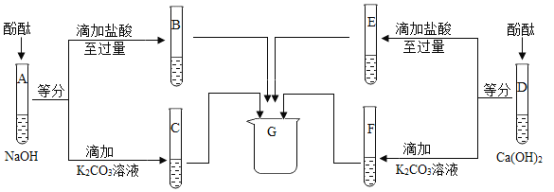
(1)A、D两种溶液的化学性质相似,因为其溶液中都含有______离子(填离子符号)。
(2)B中溶液的pH_______7(选填“>”、“<”或“=”),呈______性。
(3)F中现象是__________。
(4)四支试管内的物质在G中混合后得到无色溶液,如果其中一定含有的溶质是KC1、NaC1、CaCl2,则可能含有的溶质是_______(填写化学式)
查看答案和解析>>
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:科学探究题
兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关探究
(实验探究1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 蓝紫色 | 蓝色 | 绿色 | 黄色 |
(查阅资料)
pH值 | 7.5-9 | 10-11.9 | 12-14 |
紫甘蓝汁液显示的颜色 | 蓝色 | 绿色 | 黄色 |
(得出结论1)三种溶液的碱性由强到弱的顺序为_________。
(实验探究2)甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由_____色变为_____色。向其中加入稀盐酸,该反应的化学方程式为__________。乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图1所示。
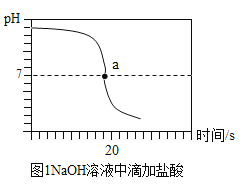
a点表示的含义是___________。
(得出结论2)从微观角度分析,该反应的实质是_________。
查看答案和解析>>
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:实验题
某探究性活动中,甲、乙同学设计并完成了如图所示的实验。(已知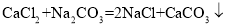 )
)
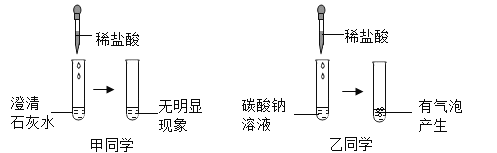
(1)写出甲同学实验中发生反应的化学方程式____________。
(2)反应结束后,甲、乙同学把废液倒入同一废液缸中,观察到废液缸中产生少量的气泡,最终有白色沉淀生成。请回答以下问题:
(Ⅰ)废液缸中最终生成的白色沉淀是_________。
(Ⅱ)甲同学实验后的废液中一定含有的物质是_________。
(3)丙同学从实验(2)的废液缸中取出废液,过滤,对滤液进行了探究。请你帮助丙同学从实验(2)的废液缸中取出废液,过滤,对滤液进行了探究。请你帮助丙同学完成以下探究方案:
探究目的 | 探究步骤 | 实验现象 |
_________ | A.取少量滤液于试管中,滴加过量的稀硝酸 | 产生气泡 |
证明滤液中一定有NaCl | B.向实验A所得溶液中滴加 _________ | 产生白色沉淀 |
(探究结论)该滤液中含有的溶质是碳酸钠和氯化钠。
查看答案和解析>>
科目: 来源:山东省烟台市2017-2018学年九年级上学期期中化学试卷 题型:计算题
甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取5.0g样品溶于一定量的水中得到25.0g溶液,再分别加入不同质量,溶质质量分数为10%的氢氧化钠溶液,反应得到沉淀的实验数据如下表
甲 | 乙 | 丙 | |
加入氢氧化钠溶液质量(g) | 35.0 | 40.0 | 45.0 |
反应得到沉淀的质量(g) | 2.5 | 2.9 | 2.9 |
试回答下列问题:
(1)上述实验中,_________同学所用的氢氧化钠溶液一定过量。
(2)求样品中氯化镁的质量分数_________(写出计算过程,结果精确到0.1%,下同)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com