
科目: 来源:江苏省扬州市高邮市、宝应县2019-2020学年九年级上学期期末化学试卷 题型:多选题
下列有关物质性质与用途对应关系正确的是
A.H2密度小于空气,可作燃料
B.N2很难与其他物质反应,可用作保护气
C.镁燃烧产生耀眼白光,可用于烟花制作
D.酒精具有可燃性,可用作溶剂
查看答案和解析>>
科目: 来源:江苏省扬州市高邮市、宝应县2019-2020学年九年级上学期期末化学试卷 题型:多选题
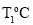 时,将等质量的
时,将等质量的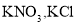 分别加入到各盛有
分别加入到各盛有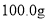 水的两个烧杯中,充分搅拌后恢复到
水的两个烧杯中,充分搅拌后恢复到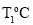 ,现象如图1、2所示。下列说法正确的是( )
,现象如图1、2所示。下列说法正确的是( )
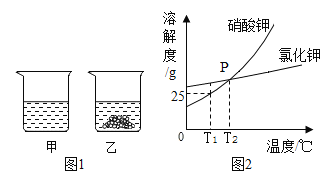
A.甲中加入的固体是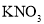
B.甲中溶液可能是该溶质的饱和溶液,乙中上层清液一定是该溶质的饱和溶液
C.将甲、乙中的物质混合,充分搅拌,一定有固体剩余
D.若将甲、乙的温度从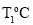 升高到
升高到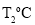 ,两溶液中的溶质质量分数相等
,两溶液中的溶质质量分数相等
查看答案和解析>>
科目: 来源:江苏省扬州市高邮市、宝应县2019-2020学年九年级上学期期末化学试卷 题型:单选题
下列实验操作能达到实验目的是
目的 | 主要操作方法 | |
A | 粗盐的提纯(仅考虑不溶性杂质) | 溶解、过滤、洗涤、干燥 |
B | 除去氮气中少量氧气 | 将混合物通过灼热的木炭 |
C | 除去铁粉中少量的铜粉 | 加入足量硫酸铜溶液,过滤 |
D | 鉴别蒸馏水和食盐水 | 用玻璃棒分别蘸取待测液在火焰上灼烧 |
A.A B.B C.C D.D
查看答案和解析>>
科目: 来源:江苏省扬州市高邮市、宝应县2019-2020学年九年级上学期期末化学试卷 题型:单选题
一定质量的某有机化合物完全燃烧,生成2.2gCO2和1.8gH2O,另取3.2g该有机化合物在O2中完全燃烧,消耗4.8gO2,该有机化合物的化学式可能是
A. C2H4 B. CH4O C. CH4 D. C2H4O
查看答案和解析>>
科目: 来源:江苏省扬州市高邮市、宝应县2019-2020学年九年级上学期期末化学试卷 题型:综合题
水是重要的自然资源,也是生命必需物质。
(1)可饮用的水
矿泉水水质主要成分(mg/L)

如图是某矿泉水的标签,请回答问题:
①镁离子_____________________;氯离子________________________;(用化学用语表示)。
②结合上表写出碳酸氢钙的化学式________________________;其中碳元素的化合价为________________________。
③矿泉水属于________________________(填“纯净物”或“混合物”);其中含量最多的分子是________________________;(用化学用语表示);该矿泉水成分中锶、钙、钠、钾等指的是_______________________(填“单质”或“元素”)。
④矿泉水中适量的钙元素有助于预防________________________。
(2)实验中的水
①洗涤仪器。容器内壁沾有下列物质,直接用水能够洗涤干净的是________________;
a 做结晶实验后的硝酸钾晶体
b 长期敞口盛放石灰水的试剂瓶内壁白色固体
c 做溶解实验后留下的植物油
d CO还原氧化铁后试管壁上的黑色固体
②做铁丝在氧气中燃烧实验时集气瓶底预留少量水的目的是____________________________;
③水也可以用作某些化学反应的反应物,请写出有水参加反应的一个化学方程式是____________________________。
(3)生活中的水
①自来水生产过程常加入活性炭,作用是____________________________;
②生活中鉴别硬水、软水的方法是:取少量水样,加入肥皂水并搅拌,出现____________________________现象的为硬水。生活中常用____________________________的方法来软化硬水;
③保护水资源是我们义不容辞的责任。下列做法不合理的是____________________________(填字母) 。
a 严格监管化肥和农药的使用
b 不间断地放水洗衣服
c 积极探索污水处理的新技术
d 抑制水中所有动、植物的生长
查看答案和解析>>
科目: 来源:江苏省扬州市高邮市、宝应县2019-2020学年九年级上学期期末化学试卷 题型:综合题
“见著知微,见微知著”是化学的思维方法。
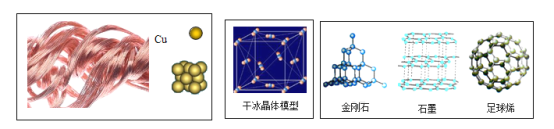
(1)铜是生活中常见的一种金属
①铜可用以制作导线,体现了金属铜的___________________性。
(2)固态的二氧化碳俗称“干冰”
①请写出干冰的一种用途__________________________;
②镁条在二氧化碳中燃烧生成氧化镁和一种黑色粉末,写出反应的化学方程式__________________________;
③通过这个反应,谈谈你对物质燃烧的新认识__________________________。
(3)物质的性质决定用途,用途反映物质的性质。
①金刚石硬度很大、石墨硬度很小,两者物理性质有较大差异的原因________________。
②下列关于足球烯(C60)的说法正确的是________________。
a 它的一个分子中含有60个碳原子
b 相对分子质量是720
c 它是一种化合物
查看答案和解析>>
科目: 来源:江苏省扬州市高邮市、宝应县2019-2020学年九年级上学期期末化学试卷 题型:实验题
请根据下列实验装置图回答有关问题:

(1)写出序号为①、②的仪器名称:①_______________________; ②_______________________;
(2)实验室制取二氧化碳的化学方程式为_______________________;若 选用F裝置收集CO2气体,应从_______________________(填“a”或“b”)端通入,使用该装置收集,检验CO2是否收集满的操作是_______________________。
(3)用双氧水和二氧化锰制取氧气的化学方程式为_______________________, 该反应的基本类型为_______________________,反应后过滤、干燥,所得到的二氧化锰_______________________ (填“能”或“不能”)继 续作为双氧水分解的催化剂。
(4)实验室常用锌粒和稀硫酸制取氢气,可选用的发生装置是_______________________(填字母), 装置C、D、E中能用来收集氢气的是_______________________(填字母)。
(5)某化学兴趣小组借助氧气传感器探究微粒的运动,数据处理软件可实时绘出氧气体积分数随时间变化的曲线。收集一塑料瓶氧气依次按以下步骤进行实验:
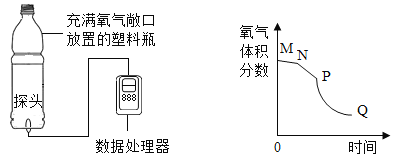
Ⅰ敞口放置; Ⅱ 双手贴在塑料瓶的外壁上:Ⅲ将塑料瓶的瓶口朝下,三步实验中测得氧气的体积分数随时间变化的曲线依次为图中的MN段、NP段和PQ段。
①以曲线MN段和_____________________作对比, 能证明温度越高氧分子运动速率越快。
a NP段
b PQ段
②曲线PQ段可证明氧气具_____________________性质 。
③随着实验的进行,最终传感器测出氧气的体积分数约为_____________________ %时,几乎不再变化。
查看答案和解析>>
科目: 来源:江苏省扬州市高邮市、宝应县2019-2020学年九年级上学期期末化学试卷 题型:流程题
“做好垃圾分类、 推动绿色发展”,下图为某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程,请回答下列问题:
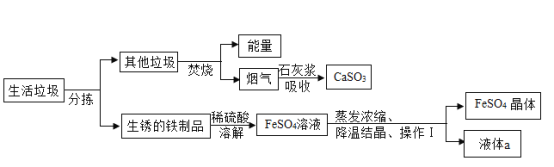
资料1:垃圾焚烧产生的烟气中含有SO2等有害气体:
资料2:石灰浆的主要成分为Ca(OH)2;
资料3: FeSO4 容易被空气中的O2氧化;
(1)垃圾分类后,对燃烧值较高的垃圾进行高温焚烧,焚烧中产生的热能转化为高温蒸气,推动涡轮机转动,使发电机工作。过程中实现了____________________能→热能→动能→____________________能的转变。
(2)石灰浆吸收SO2(化学性质与CO2相似)的化学方程式为____________________。
(3)加稀硫酸溶解环节,发生三个反应的化学方程式为:①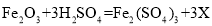 ②
②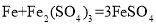 ③_______________________; 方程式①中X所代表物质的化学式是_______________________。
③_______________________; 方程式①中X所代表物质的化学式是_______________________。
(4)从FeSO4溶液到FeSO4晶体的获得环节中,操作I的名称是_______________________;实验室实现该操作需要的玻璃仪器有:烧杯、玻璃棒和_______________________;其中玻璃棒的作用是_______________________;液体a是FeSO4的_______________________溶液(填“饱和”或“不饱和”); FeSO4 晶体的成功获得需特别关注条件的控制,其方法之一是在氮气环境中进行结晶等系列操作,原因是_______________________。
(6)政府倡导垃圾分类,其意义是_______________________(写一点)。
查看答案和解析>>
科目: 来源:江苏省扬州市高邮市、宝应县2019-2020学年九年级上学期期末化学试卷 题型:科学探究题
甲烷(CH4) 与CO、H2的性质有诸多相似处:难溶于水、具有可燃性等。而CO、H2都能还原金属氧化物,那么甲烷(CH4)能否还原氧化铜?若能反应,产物有哪些?校兴趣小组针对于此,称取4. 0g氧化铜粉末,展开探究:

[查阅资料]①无水CuSO4为一种白色固体,其遇水变蓝;
②Cu和Cu2O均为红色固体,且 。
。
[进行实验]甲同学组装装置并检查其气密性良好。通入纯净、干燥的CH4后,乙同学提醒CH4有可燃性,在点燃A处酒精喷灯前,需从C装置后尖嘴导管处收集气体并______________。D处燃着酒精灯的作用主要是处理多余的CH4,请写出发生反应的化学方程式___________。
[实验现象] A中黑色粉末逐渐变红; B中白色固体变蓝; C中澄清石灰水变浑浊。
[产物分析]结合实验现象,可以判断:甲烷能够还原氧化铜。
甲同学认为:实验后,装置A中所得红色固体全部为单质铜,并结合装置B、C实验现象,书写出甲烷与氧化铜反应完全转化为单质铜的化学方程式_______________________。
乙同学认为:实验后,装置A中所得红色固体并不一定全部为单质铜,理由是_______________________。
[定量测定]
小组同学待装置冷却后,停止通CH4,测得A中红色粉末的质量为3.4g.若CH4将4.0g,氧化铜完全还原为铜单质,则理论上所得铜单质的质量应该为_______________________;故所得红色粉末中一定含有氧化亚铜。
另一小组为进一步确定该红色粉末中氧化亚铜的质量,该小组同学将上述3.4g红色粉末置于试管中加入足量稀硫酸,加热并充分振荡,静置。观察到:红色固体逐渐减少,但未完全溶解,溶液由无色变蓝色。再将实验所得物质进行过滤、洗涤、干燥,称量,最终所得红色固体的质量为2.4g。通过计算确定原3.4g红色固体中氧化亚铜的质量(请写出计算过程)_____________________。
查看答案和解析>>
科目: 来源:黑龙江省七台河市勃利县2017-2018学年九年级上学期期末化学试卷 题型:单选题
以下变化中属于化学变化的是
A.煤的干馏
B.石油的分馏
C.充有氖气的霓虹灯发出红光
D.高压锅压力过大而爆炸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com