
科目: 来源:中考题原创:鉴别食盐氯化钠与假盐亚硝酸钠 题型:综合题
某地查获一批“毒豆芽”,经检测毒豆芽中含有亚硝酸钠、尿素等违禁物,如果人食用含亚硝酸钠的食品会致癌,因此要禁止在食品中大量添加。则回答问题:
(1)下列有关NaNO2的说法正确的是(_____)
a.NaNO2是一种氧化物 b.NaNO2中氮元素的化合价为+5价
c.NaNO2由三种元素组成 d.NaNO2中Na、N、O三种元素的质量比为1∶1∶2
(2)硝酸钠使人中毒的原理与重金属离子(如铅离子、汞离子等)使人中毒的原理不同,重金属离子(如铅离子、汞离子等)使人中毒的原理是______________。
(3)亚硝酸钠是一种常用的防腐剂,我国规定肉灌肠中亚硝酸钠添加标准为每千克食品含量不超过150毫克,则200g质量分数为15%亚硝酸钠溶液至少可用于生产肉灌肠___千克。
查看答案和解析>>
科目: 来源:中考题原创:鉴别食盐氯化钠与假盐亚硝酸钠 题型:实验题
亚硝酸钠(NaNO2)外观酷似食盐,有咸味,加热会分解,放出有臭味的气体。我国曾发生过多次将这种工业用盐常被冒充食盐掺假或被误作食盐食用,导致多起中毒事故发生。请你阅读下表中的有关信息,并结合所学化学知识,回答下列问题:
项目 | 亚硝酸钠(NaNO2) | 氯化钠(NaCl) |
溶解性 | 易溶,在15 ℃时溶解度为81.5 g | 易溶,在15 ℃时溶解度为35.8g |
熔点、沸点 | 熔点:271 ℃ ,沸点:320 ℃; | 熔点:801 ℃;沸点:1413 ℃; |
溶液酸碱 | 碱性 | 中性 |
与稀盐酸作用 | 放出红棕色气体 | 无现象 |
与硝酸银溶液作用 | 生成浅黄色沉淀 | 生成白色沉淀 |
(1)根据上表写出亚硝酸钠的两条物理性质___________。
(2)亚硝酸钠跟盐酸反应会生成氯化钠、两种氮的氧化物和水,请你写出亚硝酸钠跟盐酸反应的化学方程式为______________________________。
(3)请结合上表信息,判断以下区别亚硝酸钠和氯化钠的方法错误的是____(填序号)
a. 滴加稀盐酸 b. 滴加硝酸银溶液 c.加热 d.品尝味道
(4)请你结合已学过的化学知识,用三种方法鉴别亚硝酸钠和氯化钠:
方案 | 选取的试剂和方法 | 实验现象和结论 |
方法一 | __________ | __________ |
方法二 | __________ | __________ |
方法三 | __________ | __________ |
查看答案和解析>>
科目: 来源:中考题原创:农作物秸秆大有作为 题型:单选题
果果在新华网阅读我国的《“十三五”农作物秸秆综合利用实施方案》,实现到2020年全国秸秆综合利用率达到85%以上的目标。下列关于秸秆综合利用的措施,其中不予考虑的是( )
A.推广使用微生物催腐剂,将秸秆腐熟还田
B.推广秸秆饲料和食用菌生产,发展农业循环经济
C.有序发展生物质能、秸秆建材等
D.就地焚烧,增补农田肥力
查看答案和解析>>
科目: 来源:中考题原创:农作物秸秆大有作为 题型:填空题
果果了解到农作物秸秆是一种宝贵的生物质能,综合开发利用我国产量巨大的农作物秸秆将大有作为,以秸秆为原料的生物可用于发展秸秆发电和颗粒燃料能,还可用作养殖饲料、沼气化利用、造纸、生产装饰板和有机肥等方面。则回答:
(1)果果在秋收时节观察到本地还有零星的秸杆焚烧现象,这样会造成巨大的资源浪费。尤其是焚烧秸秆可能导致的后果有(至少两点)__________________。
(2)农作物秸秆蕴含丰富的____(“可再生”或“不可再生”)生物质资源,在生产沼气的过程则主要发生了______(填“物理”或“化学”)变化。生态农业大量使用沼气作为新能源,沼气的主要成分是甲烷,可用于煮饭、照明、取暖。请写出甲烷(CH4)完全燃烧的化学方程式为______________。
(3)清洗沼气池和定期检查时,要注意避免明火,否则容易发生_______事故。请分析其原因为_______________。
(4)绿色农庄推广使用一种新型一次性可降解餐盒,以棉花秸秆为原料研制而成,废弃后在自然条件下两个月就可自然降解。请分析其中的优点之一是_________。
查看答案和解析>>
科目: 来源:中考题原创:农作物秸秆大有作为 题型:单选题
我国每年可收集秸秆总量约7亿吨,用20%秸秆生产乙醇,年产量可达到2800万吨。下列有关秸秆处理的成熟技术中不属于化学变化的是( )
A.发酵制取沼气 B.制取生物质乙醇
C.压缩制造成为成型生物质燃料 D.制糖
查看答案和解析>>
科目: 来源:中考题原创:农作物秸秆大有作为 题型:填空题
乙醇在空气中不完全燃烧时生成水、二氧化碳和一氧化碳。某实验中测得反应前后各物质的质量如下表,则根据表格中数据判断:
物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
反应前质量/g | 6.6 | 8.8 | 0 | 0 | 0 |
反应后质量/g | 2 | 0 | 6.6 | 5.4 | a |
(1)反应后一氧化碳的质量a=____。
(2)请完善该实验发生反应的化学方程式为4C2H5OH +11O2 12H2O+___CO2+___CO。
12H2O+___CO2+___CO。
查看答案和解析>>
科目: 来源:中考题原创:农作物秸秆大有作为 题型:科学探究题
中国石油化工集团公司对秸秆制乙醇生产技术获得重大突破,可为万吨级示范装置的建设提供技术支撑。某化学兴趣小组对“秸秆主要由哪些元素组成”的问题展开以下探究活动:
(查阅资料)我国现已成为世界上第三大生物燃料乙醇生产国和应用国。乙醇俗称酒精,其化学式为C2H5OH。用乙醇做燃料,在空气中充分燃烧生成二氧化碳和水。
(提出猜想)该小组根据乙醇的成分猜想秸秆中主要含有碳元素和氢元素。
(设计实验)设计并利用如图装置进行实验,观察实验现象,请完善实验记录:

实验步骤 | 实验现象 | 实验结论 |
(1)将秸秆烘干,粉碎后放在直玻璃管中 (2)通入一会儿氧气,再点燃酒精灯。 | (1)秸秆燃烧,直玻璃管内有水雾产生。 | 生成物中有____。 |
(2)还能够观察到澄清石灰水__________。 | 生成物中有CO2。 |
(结论与解释)(1)将秸秆烘干的主要目的是:①干燥,使其容易燃烧;②______________。
(2)根据以上探究,该小组得出结论:秸秆中一定含有C、H、O三种元素。你认为这种说法是否正确,并阐述你的理由:___________________________________。
(拓展应用)科学家预言未来最理想的燃料是绿色植物。植物秸杆的主要成分是纤维素,化学式为(C6H10O5)n,在适当催化剂作用下与水作用生成葡萄糖(化学式为C6H12O6);再将葡萄糖在一定条件下发酵转化为乙醇。请写出葡萄糖转化为乙醇的化学方程式为:___________________,该反应的基本类型为_________。
查看答案和解析>>
科目: 来源:中考题原创:溶解度曲线的理解与应用 题型:单选题
根据图4信息判断,下列叙述不正确的是
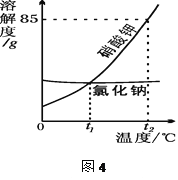
A.硝酸钾的溶解度随温度升高而增大
B.t1℃时,氯化钠和硝酸钾的溶解度相同
C.将t2℃时的硝酸钾饱和溶液降温到t1℃,有晶体析出
D.t2℃时,80g硝酸钾溶于100g水中可制得饱和溶液
查看答案和解析>>
科目: 来源:中考题原创:溶解度曲线的理解与应用 题型:单选题
如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线。下列说法错误的是

A.t1℃时,三种物质中B的溶解度最大
B.t2℃时,取三种物质各a g分别放入100g水中充分溶解,只有C物质能形成饱和溶液
C.将等质量的三种物质的饱和溶液分别由t2℃降温到t1℃,A溶液中析出的晶体质量最大
D.可用增加溶剂的方法使接近饱和的B溶液变为饱和溶液
查看答案和解析>>
科目: 来源:中考题原创:溶解度曲线的理解与应用 题型:填空题
我国北方有许多盐湖,湖水中溶有大量的碳酸钠和氯化钠,合理利用自然资源,冬天捞碱(Na2CO3),夏天晒盐(NaCl)。Na2CO3和NaCl的溶解度曲线如图所示,据图回答下列问题:
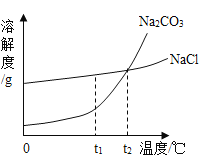
(1)在____℃时,碳酸钠和氯化钠两种物质的溶解度相同。
(2)等质量Na2CO3、NaCl饱和溶液分别从t2℃降温到t1℃,析出晶体较多的是_________。
(3)从湖水中得到的碳酸钠常含有少量的氯化钠,可以采用_____(选填“降温结晶”、“蒸发结晶”或“过滤”)的方法得到较纯净的碳酸钠。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com