
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:单选题
在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识正确的是( )
物质 | M | N | Q | P |
反应前质量(g) | 18 | 1 | 2 | 30 |
反应后质量(g) | X | 26 | 2 | 10 |
A.反应后物质M的质量为3g B.该反应的类型是分解反应
C.参加反应的M、P的质量比为1:4 D.物质Q一定是该反应的催化剂
查看答案和解析>>
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:单选题
下列对一些事实的解释中,不合理的是( )
事 实 | 解 释 | |
A | 盛夏,大明湖畔,荷香四溢 | 分子在不停运动 |
B | 将10ml酒精和10mL水混合后总体积小于20mL | 分子之间有间隔 |
C | 水在直流电作用下,可分解为H2和O2 | 化学反应中,分子和原子都可分 |
D | NaOH、Ca(OH)2溶液都能使无色酚酞试液变红 | 水溶液中都含有大量的OH- |
A.A B.B C.C D.D
查看答案和解析>>
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:单选题
下列实验方案设计可行的是( )
A.用溶解、过滤的方法分离氯化钠和硝酸钾的固体混合物
B.用酚酞鉴别氢氧化钠溶液和碳酸钠溶液
C.向氧化铜中加入适量稀硫酸恰好反应,再加入适量氢氧化钡溶液,过滤即制得氢氧化铜
D.向某无色溶液中加入足量稀盐酸无现象,再加入氯化钡溶液,若产生白色沉淀,证明原溶液中一定含有 SO42-
查看答案和解析>>
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:单选题
下列各组物质的分离、鉴别方法中,不正确的是( )
选项 | 物质 | 鉴别方法 |
A | 分离食盐和沙粒 | 溶解、过滤、蒸发 |
B | 鉴别氢氧化钠固体和硝酸铵固体 | 加水溶解后,测溶液温度变化 |
C | 鉴别蒸馏水和过氧化氢溶液 | 加入二氧化锰后,看气泡 |
D | 鉴别硬水和软水 | 过滤 |
A.A B.B C.C D.D
查看答案和解析>>
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:单选题
将a g锌粒加入一定质量的MgSO4、CuSO4和AgNO3的混合溶液中,充分反应后过滤,将滤渣洗涤、烘干后称量质量为b g,向滤液和滤渣中分别加入稀盐酸,下列不合理的是( )
A.如果滤液中产生白色沉淀,则滤液的颜色为蓝色 B.滤渣的质量可能等于所加锌粒的质量
C.如果滤渣中有气体生成,则滤渣中一定含有4种金属 D.反应后所得滤液中至少含有两种金属离子
查看答案和解析>>
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:单选题
去下列各物质中混有的少量杂质,所用试剂及操作方法均正确的是( )
选项 | 物 质 | 杂 质 | 除杂试剂或操作方法 |
A | NaNO3溶液 | AgNO3 | 加入适量NaCl溶液,过滤 |
B | NaCl溶液 | Na2CO3 | 加入过量的BaCl2溶液,过滤 |
C | O2 | H2O | 通过灼热的铜网 |
D | 氯化钙 | 盐酸 | 加入过量氧化钙,过滤 |
A.A B.B C.C D.D
查看答案和解析>>
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:单选题
为测定某化肥[(NH4)2SO4和NH4Cl组成]的含氮量,取12g于研钵中,向其中加入氢氧化钙充分反应,当加入7.4g氢氧化钙时恰好完全反应,则此化肥中氮元素的质量分数约为( )
A.21.1% B.23.3% C.25.5% D.27.7%
查看答案和解析>>
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:填空题
(1)分类是学习和研究物质性质常用的一种方法,物质的性质决定物质的用途。按要求从硫酸、氮气、盐酸、氯化银、氢氧化铜、甲烷中选择合适的物质,将其化学式填写在下列横线上。
①最简单的有机物________________;
②可作食品袋填充气体的单质____________________;
③一种难溶性的碱________________;
④一种易挥发的酸____________。
(2)全球首创的智能共享摩拜单车正式登陆泉城济南,为市民提供出行服务,倡导绿色出行,共建美好城市。
①摩拜单车从骑行安全因素考虑,车身的材料使用了铝合金。铝合金材料的车身具有不易被腐蚀,不易被损坏等优点,可以延长单车的使用寿命。铝合金属于__________________(填写“金属材料”“复合材料”“有机高分子材料”之一)。
②摩拜单车的轮胎使用无毒环保橡胶制作,采用“横向镂空”设计,具有缓冲好、不怕扎、免充气及可回收再利用等众多优点,是国家提倡的“绿色环保”产品。已知合成橡胶是由不同单体在引发剂作用下,经聚合而成的品种多样的高分子化合物。单体有丁二烯、苯乙烯、丙烯腈等多种。其中丙烯腈(CH2CHCN)中碳、氢元素的质量比为_______________(填最简整数比)。
③摩拜单车的入驻解决了济南市民出行“最后一公里”的问题,减少了私家车的使用。私家车尾气的大量排放是导致酸雨的重要原因,请简述酸雨的形成过程_______________。
(3)为减少CO2在空气中的排放量,实际生产中,经常利用NaOH溶液来“捕捉”CO2,流程如下图(部分条件及物质未标出)。
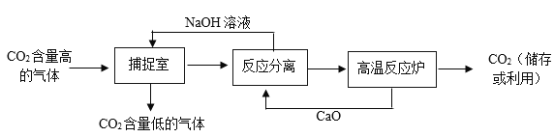
①捕捉室内发生的化学反应的化学方程式为________________;
②“高温反应炉”内发生的反应为________________反应(填“化合”“分解”“置换”“复分解”之一)。
查看答案和解析>>
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:填空题
(1)“以国为重的大国工匠”徐立平的先进事迹受到广泛关注。“大国工匠”徐立平的工作是给固体燃料发动机的推进剂药面“动刀”整形,以满足火箭及导弹飞行的各种复杂需要。
①徐立平因其精湛的技艺和敬业奉献的精神被赞誉为“雕刻火药的大国工匠”。在药面整形的过程中,有丝毫的偏差都有可能造成燃料爆炸。下列有关燃料燃烧或爆炸的说法中,不正确的是__________(填写序号A、B、C、D之一)。
A可燃物在有限的空间内燃烧可能会引起爆炸
B燃料燃烧引起的爆炸属于化学变化
C控制燃烧条件可以防止爆炸
D可燃物温度达到着火点一定能燃烧
②中国航空工业的发展需要大国工匠精神,也需要化学知识的支持。其中“国防金属”镁是制造火箭的重要材料,目前世界上大约60%的金属镁是利用化学方法从海水(或卤水)中提取的。其简要过程如下图所示:
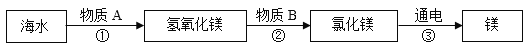
I.从海水中提取MgCl2时,通常采用化学沉淀法将海水中的镁元素予以富集,在工业上,过程①中加入的物质A一般是 _________。
Ⅱ.请写出过程②中反应的化学方程式________________。
(2)济南享有“泉城”的美誉,清冽甘美的泉水赋予济南市灵秀的气质和旺盛生命力,也形成了独特的泉水文化。
①天然水转化成饮用水需经一系列净化,Cl2是一种廉价的自来水消毒剂,与水反应生成次氯酸(HClO)有较强的杀菌作用。氯气(Cl2)和次氯酸中氯元素的化合价分别是____________。
②下列说法中,错误的是__________(填序号)。
A清澈的泉水肯定属于纯净物 B过滤可以除去泉水中的所有杂质
C水的天然循环实现了自身的净化 D水是一种常用的溶剂
(3)泉水中蕴含一定量的钾元素与钠元素。KNO3和NaCl都是易溶于水的物质,它们的溶解度曲线如图所示:
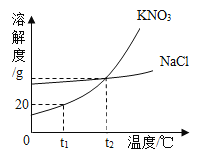
①t1℃时,KNO3溶液的溶质质量分数__________NaCl溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一)。
②t2℃时,向盛有50g水的烧杯中加入50gKNO3充分溶解后,缓慢降温至t1℃,则所得溶液中溶质与溶液的质量比是________(填最简整数比)。
③当KNO3固体中含有少量NaCl时,可采用降温结晶的方法提纯KNO3,请说明提纯的原理__________。
查看答案和解析>>
科目: 来源:2019年山东省济南市南山区中考三模化学试卷 题型:实验题
如下图所示为实验室中常见的气体制备、净化、干燥和收集实验的部分仪器。 试根据题目要求,回答下列问题:
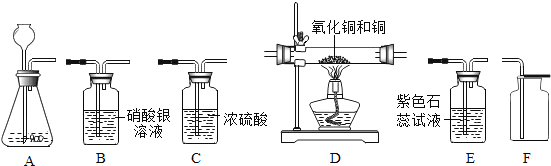
(1)用石灰石和稀盐酸为原料制取并收集干燥纯净的二氧化碳气体。(提示:挥发出的少量 HCl 气体可用硝酸银溶液吸收)。
①仪器 A 中发生的化学反应方程式是__________。
②某同学设计的仪器连接顺序为_________________。
③为证明二氧化碳能和水反应,可将二氧化碳气体通入装置中__________填装置字母)
(2)小明同学欲利用锌粒和稀硫酸制备的氢气来测定某氧化铜和铜的混合物样品中铜单质的质量分数,仪器连接顺序为:A→C1→D→C2→C3(已知:CuO+H2 Cu+H2O,其中C1、C2、C3为浓硫酸洗气瓶),并检验装置的气密性,所设计的实验装置中气体流向是从左向右。
Cu+H2O,其中C1、C2、C3为浓硫酸洗气瓶),并检验装置的气密性,所设计的实验装置中气体流向是从左向右。
①D 处大玻璃管内可以观察到的现象是_______________。
②根据完全反应后C2装置的质量变化测定样品中铜单质的质量分数,若装置中不连接C1,则样品中铜单质的质量分数将________________(填“偏大”“偏小”“不受影响”之一)。
③取混合物样品 10g,若测得充分反应后,D 处大玻璃管内的物质总质量减少 1.6g,则原混合物样品中铜单质的质量分数为______________。
④经测定,仪器 A 中稀硫酸和锌粒反应后溶液 pH 变大了,试叙述其中的化学原理____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com