
科目: 来源: 题型:
【题目】海底世界动物园中,表演者常常携带氧气瓶在水中与鱼“共舞”。氧气能被压缩在氧气瓶中说明( )
A.氧分子的大小发生改变 B.氧分子可以再分
C.氧分子总是在不断运动 D.氧分子之间有间隔
查看答案和解析>>
科目: 来源: 题型:
【题目】【2014年黑龙江省绥化市】某氢氧化钠样品中含有少量的碳酸钠杂质.现取21.3g样品于烧杯中,加入173.4g水使其完全溶解,再向其中逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示,请计算:
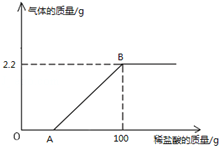
(1)样品中氢氧化钠的质量.
(2)B点时,烧杯内溶液的溶质质量分数.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学反应方程式书写正确的是
A.铜加入稀盐酸中:Cu+2HCl═CuCl2+H2↑
B.二氧化碳通入足量的澄清石灰水中:CO2+Ca(OH)2═CaCO3↓+H2O
C.铁加入稀硫酸中:2Fe+3H2SO4═Fe2(SO4)3+3H2↑
D.碳酸钠固体加入稀盐酸中:Na2CO3+HCl═NaCl+H2O+CO2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】(2分)维生素C(化学式为C6H806)对人体皮肤和牙龈的健康有重要作用,缺乏维生素C会引起坏血病。经研究表明,青少年每天都需要摄入60mg的维生素C,若其中的12mg由水果补充。请计算回答:
(1)维生素C中碳、氢、氧三种元素的质量比是 ;
(2)若食用的水果以苹果计,已知每100g苹果中含维生素C的质量为4mg,那么每天需吃苹果的质量
是 g。
查看答案和解析>>
科目: 来源: 题型:
【题目】【2014年湖南省娄底市】硅钢是变压器、充电器中的核心材料,其主要成份是Fe和Si。某学生用硅钢样品做了如下实验:取4.2g硅钢样品,将60g稀硫酸分6次加入样品中(其中稀硫酸与硅及其它杂质不反应),充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
稀硫酸的用量 | 剩余固体的质量 |
第一次加入10g | mg |
第二次加入10g | 2.8g |
第三次加入10g | 2.1g |
第四次加入10g | 1.4g |
第五次加入10g | 0.7g |
第六次加入10g | 0.7g |
(1)从以上数据可知,稀硫酸加入第 70 次充分反应后,铁恰好完全反应。
(2)表格中m= 71 。
(3)计算所用稀硫酸中溶质的质量分数。72
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学为了测定NaCl和MgCl2固体混合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如下实验数据:
实验次数 | 一 | 二 | 三 | 四 |
固体混合物的质量(g) | 20 | 20 | 20 | 20 |
加入NaOH溶液的质量(g) | 20 | 40 | 60 | 80 |
生成沉淀的质量(g) | 2.9 | m | 8.7 | 8.7 |
问:
(1)表中m的值为 ;(2分)
(2)原固体混合物中MgCl2的质量分数是多少?(要求写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】“黄铜”是铜、锌合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下:(烧杯质量均为56g)
甲 | 乙 | 丙 | |
烧杯+稀盐酸质量 | 139g | 129g | 129g |
加入黄铜样品质量 | 20g | 24g | 20g |
充分反应后,烧杯+剩余物质质量 | 158.8g | 152.8g | 148.8g |
请回答下列问题:
(1) 同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量是 .
(2)计算黄铜样品中锌的质量分数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com