
科目: 来源: 题型:
【题目】(4分)A图为实验示意图,在室温情况下,烧杯中盛装的是甲物质的溶液,试管①中盛装的是乙物质的溶液,试管②中盛装的是丙物质的溶液。当它们由室温升到80℃时,发现烧杯中甲物质没有明显变化,而试管①中盛装的是乙物质全部溶解,试管②中有丙物质析出。B图表示三种物质的溶解度曲线。请你据此现象回答下列有关问题:

(1)室温时, (选填“烧杯”、“试管①”或“试管②”)中溶液可能是不饱和溶液;
(2)上图能表示甲物质的溶解度曲线的是 (选填a、b或c);
(3)若乙物质溶液中混有少量的甲物质,提纯乙物质可采取的方法是
(4)对于甲、乙两物质饱和溶液,在温度 时,乙物质的溶质质量分数一定比甲物大.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验现象描述不正确的是
A.白磷在空气中燃烧产生大量白烟
B.氢气在氧气中燃烧发出淡蓝色火焰
C.电解水时负极产生的气体体积是正极产生的气体体积的2倍
D.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
查看答案和解析>>
科目: 来源: 题型:
【题目】(7分)实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示).
![]()
小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是( )
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
ⅡNa2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ室温(20℃)时,测定四种物质的溶解度数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度g | 36 | 109 | 215 | 9.6 |
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验.
实验步骤 | 实验现象 | 结论及化学方程式 |
①取少量溶液于试管中,②滴加 | 产生大量气泡 | 反应的化学方程式: |
③把产生的气体通入澄清的石灰水中. | 澄清的石灰水变浑浊 | 猜想②正确. 反应的化学方程式: |
查看答案和解析>>
科目: 来源: 题型:
【题目】(5分)鸡蛋壳的主要成分是碳酸钙.小明同学为了测定鸡蛋壳中碳酸钙的质量分数,分别设计了如下实验并进行计算.将鸡蛋壳洗净、干燥并捣碎后放入锥形瓶里,加入足量的稀盐酸充分反应(假设其他杂质不与盐酸反应).
测得相关数据如图所示:

【数据处理】
(1)反应生成二氧化碳的质量为 g.
(2)请帮小明计算鸡蛋壳中碳酸钙的质量分数,并写出计算过程:
(3)实验过程如果有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比会
(填“偏大”、“偏小”或“不变”)
查看答案和解析>>
科目: 来源: 题型:
【题目】(5分)下图是KNO3和NaCl的溶解度曲线。试回答下列问题:
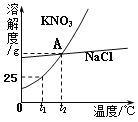
(1)交点A表示的一条意义是_____________________________。
(2)在t1℃时,将足量KNO3溶解在100g水中恰好形成饱和溶液,该溶液的溶质质量分数为_____,再将该溶液升温至t2℃(溶剂不蒸发),升温后溶液浓度__________(填“变大”“变小”“不变”之一)。
(3)当KNO3中含有少量NaCl时,可采用降温结晶的方法提纯KNO3,请说明提纯的原理_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A. 二氧化锰对过氧化氢的分解具有催化作用
B. 空气中含量最多气体是氮气
C. 在空气中加热铁丝,铁丝只能红热不能燃烧
D. 硫与氧气反应,发出淡蓝色火焰
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质的鉴别方案错误的是
A. 用燃着的木条鉴别氮气和二氧化碳气体
B. 用肥皂水鉴别硬水和软水
C. 用闻气味的方法鉴别白酒和白醋
D. 用二氧化锰鉴别水和5%过氧化氢溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】(7分)如下图所示为实验室中常见气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:

(1)高锰酸钾(KMnO4)固体在加热条件下,能较快地分解为锰酸钾(K2MnO4,可溶固体)、二氧化锰(难溶固体)和氧气。若以高锰酸钾为原料在实验室中制备并收集干燥的氧气:
①所选仪器的连接顺序为________________(填写仪器序号字母)。
②用高锰酸钾制备氧气所发生反应的化学方程式为____________________________________________。
③从高锰酸钾完全分解后的固体剩余物中提纯锰酸钾的方法是__________________
(2)若用锌和稀硫酸反应制取氢气,并用来测定某不纯氧化铜样品的纯度(杂质为少量单质铜),仪器的连接顺序为:A→D1→C→D2→D3(已知:CuO+H2 △ Cu+H2O ;D1、D2、D3为3个浓硫酸洗气瓶)。
①仪器C的大玻璃管中可以观察到的现象是 。
②仪器D1的作用是__________,通过测量反应前、后D2浓硫酸洗气瓶的质量变化,来计算氧化铜样品的纯度。若不连接D1,则计算出样品纯度的结果将 (填“偏小”“偏大”“不受影响”之一)。
③按照正确的仪器连接顺序进行实验,充分反应后测量,仪器D2的质量增加了1.8g,则仪器C大玻璃管内的固体质量应该减少__________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com