
科目: 来源: 题型:
【题目】保护环境人人有责,下列措施中与保护环境无关的是
A.提倡乘坐公共交通,骑自行车或步行的方式出行
B.推广使用太阳能、风能等清洁能源
C.减少户外运动时间,避免呼吸道疾病
D.废旧电池回收集中处理
查看答案和解析>>
科目: 来源: 题型:
【题目】(4分)化学小组探究镁、铁、铜三种金属的活动性顺序,设计了下图所示实验方案。
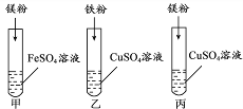
(1)试管乙中观察到的现象是 ,反应的化学方程式为 。
(2)同学们经讨论后认为该方案可以优化, 试管的实验是多余的。
(3)去掉多余的实验,同学们将另两只试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,向滤渣中加入稀硫酸,有气泡产生,则滤渣的成分可能是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(3分)工业废水中含有硫酸亚铁、硫酸铜和污泥。某同学设计了利用废水制备硫酸亚铁晶体(FeSO4·7H2O)并回收铜的实验方案,流程如下:
已知:硫酸亚铁晶体受热易分解。
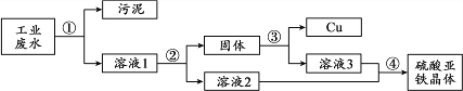
回答下列问题:
(1)步骤②中需加入的物质及目的是 。
(2)步骤③中发生反应的化学方程式为 。
(3)步骤④的操作是蒸发浓缩、降温结晶、 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(5分)A~F为初中化学常见物质,它们由H、C、O、Cl、Na、Ca中的元素组成。
(1)A为氧化物,可用于制备改良酸性土壤的碱,写出用A制备碱的化学方程式 。
(2)B、C均为液体,且组成元素相同,C在一定条件下可生成B,B的化学式为 。
(3)D用于玻璃、造纸、纺织、洗涤剂的生产。取D溶液进行实验,操作及部分现象如图所示。D与F反应的化学方程式为 。
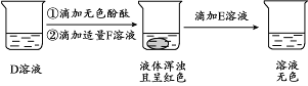
(4)从上述物质中任选2种为一组,按下图装置进行实验,将液体滴入瓶中,关闭活塞。请根据表中现象,写出符合要求的物质。
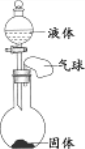
现象 物质 | 气球变鼓,一段时间后恢复原状 | 气球变鼓,一段时间后不恢复原状 |
液体 | ||
固体 |
查看答案和解析>>
科目: 来源: 题型:
【题目】(5分)下图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
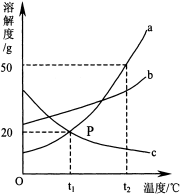
① P点的含义是 。
② t2℃时a、b、c三种物质的溶解度由大到小的排列顺序是 。
③ t2℃时将30g a物质加入到50g水中充分溶解,所得溶液是 (填“饱和”或“不饱和”),溶液质量是 g。
④ 将t1℃时a、b、c三种物质的饱和溶液分别升温到t2℃,三种溶液的溶质质量分数大小关系是 。
Ⅰ.b>a=c Ⅱ.a=b>c Ⅲ.a>b>c Ⅳ.b>a>c
查看答案和解析>>
科目: 来源: 题型:
【题目】依据国家相关法律规定,机动车驾驶员醉驾将受到刑事处罚。检测驾驶员是否酒后驾车,可用一种装有重铬酸钾(K2Cr2O7)的仪器。在K2Cr2O7中Cr元素的化合价是
A.+2 B.+3 C.+6 D.+7
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能说明分子之间有间隔的是
A.1g酒精和1g水混合质量为2g
B.1体积酒精和1体积水混合小于2体积
C.氧气加压降温形成液氧
D.空气受热体积膨胀
查看答案和解析>>
科目: 来源: 题型:
【题目】(10分)我国著名化学家侯德榜发明的“联合制碱法”主要原理是:I.向浓氨水中通入足量的CO2,使氨气、水和CO2发生化合反应而生成NH4HCO3溶液;II.向所得溶液中加入食盐细粒,充分搅拌,会析出溶解度较小的小苏打固体并得到化肥溶液;III.加热析出的固体制取纯碱。此法经过调整并应用于化工产业,某化工企业的工艺流程示意图如下:

请完成下列填空:
(1)“联合制碱原理II”中发生反应的化学方程式为 。
(2)在如图的流程中,先加Ca(OH)2溶液的目的是 ,再加入Na2CO3溶液的目的是 。
(3)“操作1”的名称是 ,“氨化溶液”后,溶液的pH 7(填:“大于”、“小于”或“等于”),从而有利于吸收“气体A”,气体A为 (填名称)。
(4)利用“270℃以上小苏打完全分解,纯碱受热不分解”的性质,化学兴趣小组的同学对实验室所购纯碱(假设所含杂质均为小苏打)进行了如下实验:称取20.00g干燥的固体样品放入坩埚,300℃恒温加热至质量不变,在干燥器中冷却后称量残留固体质量为19.38g。
根据题目所给信息,计算该样品中纯碱的质量分数(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com