
科目: 来源: 题型:
【题目】如图为CO还原CuO“微型”实验装置(夹持仪器等略),已知:HCOOH热浓硫酸H2O+CO↑,下列说法错误的是
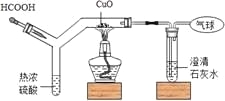
A. 实验中所需CO可现制现用
B. 此装置可节约用品,污染小,现象明显
C. 此装置内空间较小,空气易排空,实验危险系数小
D. 该实验中所涉及反应的基本类型有分解反应和置换反应
查看答案和解析>>
科目: 来源: 题型:
【题目】一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案:
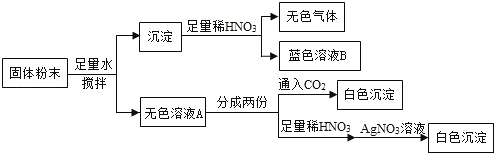
下列判断正确的是( )
A.蓝色溶液B中阳离子只有Cu2+
B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl
D.原固体粉末一定有CaCO3、NaOH、NaNO3、CuCl2和Ca(NO3)2
查看答案和解析>>
科目: 来源: 题型:
【题目】NaCl、KNO3两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
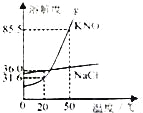
A.20°C时,NaCl的溶解度为31.6g
B.KNO3的溶解度大于NaCl的溶解度
C.使NaCl从其饱和溶液中析出,可采用蒸发溶剂的方法
D.50℃时,在100g水中加入100gKNO3,所得溶液中KNO3的质量分数为50%
查看答案和解析>>
科目: 来源: 题型:
【题目】为测定某市售碳酸钙药品中碳酸钙的质量分数(杂质为SiO2,与稀盐酸不反应),某同学的方法是:将样品与稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中碳酸钙的质量,从而计算出样品中碳酸钙的质量分数。为测定生成CO2的质量,他设计了如下实验方案(已知:无水氯化钙是常见的干燥剂):
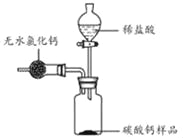
(1)按图组装好装置,检查装置气密性后,在分液漏斗中加入过量稀盐酸,并在干燥管中加入适量无水氯化钙样品,称得装置和药品的总质量为564.57g;
(2)在广口瓶中加入碳酸钙样品,称得装置和药品的总质量为574.57g;
(3)旋紧橡皮塞,打开分液漏斗旋塞,向广口瓶中滴加稀盐酸,使样品与稀盐酸完全反应;
(4)反应结束后,称得装置及装置内所有物质的总质量为570.57g。
请根据上述实验回答下列问题:
(1)该方案测得样品中碳酸钙的质量分数是多少(写出解题过程,计算结果精确到0.1%)?
(2)该实验中用稀盐酸与碳酸钙样品反应,而不用浓盐酸与碳酸钙样品反应,其原因是
。若实验中不用无水氯化钙干燥,则测得样品中碳酸钙的质量分数与上述实验计算结果相比 (选填“偏小”或“不变”或“偏大”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】图1是探究白磷在水中燃烧的实验装置。该装置的不足之处有:①通过氧气时,白磷易被冲散而较难与氧气接触;②逸散的五氧化二磷会造成空气污染。图2是探究白磷在水中燃烧的改进实验装置,由A、B、C三部分组成。请认真阅读下列内容并回答有关问题:
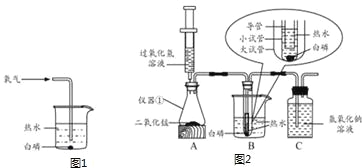
资料卡:凡能与碱反应生成盐和水的氧化物,称为酸性氧化物。常见的酸性氧化物有CO2、SO2、SiO2、P2O2等。
(1)在仪器①中加入1药匙二氧化锰,用注射器吸入约40mL5%的过氧化氢溶液,然后将注射器的针头刺入橡皮塞中。仪器①的名称为 。
(2)在广口瓶中加入氢氧化钠溶液至其中上部,旋紧双孔塞。加入氢氧化钠溶液的目的是 。
(3)取一专人绿豆大小的白磷放入小试管中,再加入少量约80℃热水(热水的高度以小试管高度![]() 为宜);将大试管必须要小,其原因是 。
为宜);将大试管必须要小,其原因是 。
(4)缓慢推动注射器。仪器①中发生反应的化学方程式为 ,装置B小试管中观察到的现象为:①有气泡产生;② 。
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列反应的化学方程式。
(1)镁条在空气中燃烧生成所化镁: ;
(2)锌和稀硫酸反应: ;
(3)氢氧化钠溶液和稀盐酸反应: ;
(4)实验室加热高锰酸钾制取氧气: ;
(5)硫化氢(H2S)气体和二氧化硫气体混合生成硫和水: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】区分下列各组物质的两种方法都正确的是
需区分物质 | 方法一 | 方法二 | |
A | 空气和氧气 | 用带火星木条检验 | 闻气味 |
B | 硬水和软水 | 观察颜色 | 加明矾搅拌 |
C | 铜丝和铁丝 | 用磁铁吸引 | 观察颜色 |
D | 二氧化碳和氮气 | 澄清石灰水 | 燃着的木条 |
查看答案和解析>>
科目: 来源: 题型:
【题目】用分子的观点解释下列现象,不合理的是
A.端午时节粽飘香——分子在不停地运动
B.干冰升华变为气体,所占体积变大——气体分子变大
C.晴天湿衣服比阴天干得快——晴天气温高,分子运动速率快
D.6000L氧气加压后可装入容积为40L的钢瓶中——分子间有间隔
查看答案和解析>>
科目: 来源: 题型:
【题目】某科研小组设计利用稀H2SO4浸取某废弃的氧化铜锌矿(主要成分为CuO和ZnO,其余成分既不与酸反应,也不溶解于水)的方案,实现废物综合利用。部分实验流程如下:

请根据上述实验流程回答下列问题:
(1)操作1的名称是 。
(2)在氧化铜锌矿中加入过量稀硫酸,主要成分发生反应的化学方程式为 , 。
(3)加过量铁粉后,发生反应的基本反应类型是 ,得到滤渣1的成分为 (填化学式)。
(4)在实验过程中,双氧水会与Fe2+反应生成Fe3+和水,以便在后续的操作中将溶液中铁元素除去。高锰酸钾溶液也能将Fe2+氧化成Fe3+,选用双氧水的优点是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500 g溶质质量分数为0.9%的生理盐水,需氯化钠固体____g。下列实验操作与目的分析均正确的一组是____(填序号)。
项目 | 实验操作 | 目的分析 |
A | 称量时,将取出的过量氯化钠放回原瓶 | 节约药品 |
B | 溶解氯化钠时用玻璃棒搅拌 | 增大氯化钠的溶解度 |
C | 称取氯化钠时,在天平两边托盘上各放一张质量相等的纸 | 整洁美观 |
D | 量取所需水时,视线与量筒内液体凹液面的最低处保持水平 | 准确读数 |
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有:烧杯、玻璃棒、量筒和____。
(3)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示。与丙烧杯中溶液溶质质量分数一定相同的是____(填序号)烧杯中的溶液。
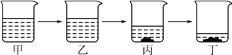
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com