
科目: 来源: 题型:
【题目】我市被评为国家级文明城市,“保持城市清洁”应作为我市的一项长效机制。因此,在日常生活中不宜提倡的是
A. 将废旧电池回收集中处理 B. 将垃圾分类投放
C. 在饭店就餐使用一次性餐具 D. 减少使用煤炭做燃料
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10.0克,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示。求:

(1)铜锌合金汇中,Zn的质量分数是 。
(2)所用稀硫酸溶液中溶质的质量分数是多少?
查看答案和解析>>
科目: 来源: 题型:
【题目】A~F是初中化学中的常见物质,如图所示是它们之间的转化关系,图中部分反应物或生成物未全部标出.已知:A是天然气的主要成分,B在常温下为液态,F是黑色粉末.
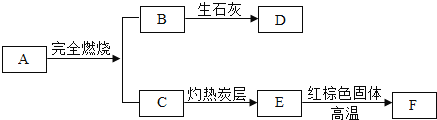
(1)B→D是 反应(填“放热”或“吸热”);
(2)C→E属于基本反应类型中的 反应;
(3)写出E→F的化学反应方程式 ;
(4)写出E物质的另一种用途 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A.SO2、CO、NO2都是造成空气污染的气体
B.合金硬度一般比组成它的纯金属大
C.洗洁精具有乳化作用,能去除餐具上的油污
D.硝酸铵固体溶解时放热
查看答案和解析>>
科目: 来源: 题型:
【题目】请结合下图回答问题:
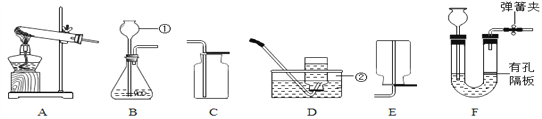
(1)写出有标号的仪器名称:①______________,②______________。
(2)用高锰酸钾制取氧气选A、D进行实验,该反应的化学方程式是______________; 发现水槽中的水变红的原因是_______;气体收集完毕时,应先______(填a或b)。
a.从水中取出导气管 b.熄灭酒精灯
(3)实验室用B、C装置制取二氧化碳的化学方程式是__________________________,若将发生装置由B改为F,其优点是_______________。
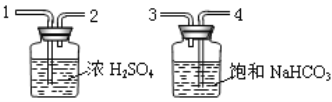
为了得到纯净、干燥的CO2,除杂装置(如下图所示)的导管按气流方向连接顺序是________(选填字母)。
a.1→2→4→3 b.2→1→3→4 c.4→3→1→2 d.3→4→2→1
(4)实验室用固体无水醋酸钠和碱石灰混合加热的方法制取甲烷(甲烷的密度比空气小,且不溶于水)。该实验可选用的发生装置和收集装置组合是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硬水中含有一定量的Ca(HCO3)2和Mg(HCO3)2,某兴趣小组的同学将一定量的硬水煮沸后出现白色固体,该小组的同学探究其成分。
查阅资料:已知可溶性的Ca(HCO3)2加热会分解,出现白色沉淀和能使澄清石灰水变浑浊的气体,分解的化学方程式为_________
【提出问题】硬水煮沸后的白色固体中还含有什么物质?
【猜想】 甲:MgCO3; 乙:Mg(OH)2; 丙:MgO
【实验】
(1)甲同学取白色固体,加入适量的稀盐酸,观察到有气泡产生,认为自己的猜想正确,其他同学否定了他的结论,理由是_______
(2)乙同学称取10.8g白色固体,设计如下实验确定固体组成:
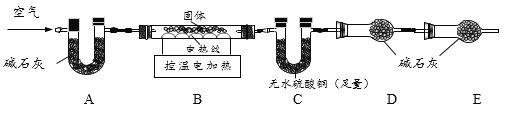
①反应前,先通一段时间的空气,目的是_____________。
②加热一段时间后,装置C中可观察到_______(填实验现象),证明乙同学的猜想成立。
③实验中E装置的作用是___________________。
④充分反应后,测得C增重1.8g,D中增重4.4g。
【结论】(1)白色固体中各成分的质量比为______。
(2)写出Mg(HCO3)2受热分解的化学方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示某些物质间转化关系。通常情况下,A是一种无色液体,D和E是组成元素相同的两种气体,且D有毒,F是一种红色金属,X用于改良性土壤(部分反应条件或某些反应产物未注明)。回答问题:
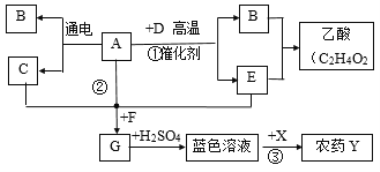
(1)写物质化学式:G_________、X______________。
(2)写出化学方程式:
①____________________。
②____________________。
(3)反应③用于配制农药Y,Y的俗称为_____________。
(4)工业上可用B和E合成乙酸,反应中B和E的质量比为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】比较推理是化学学习中常用的思维方式,下列推理正确的是( )
A. 烧碱属于碱,故纯碱也是碱
B. 生铁比铁硬,故黄铜比铜硬
C. Al(OH)3可以治疗胃酸过多,故NaOH也可治疗胃酸过多
D. 洗涤剂对油污有乳化作用,故汽油对油污也有乳化作用
查看答案和解析>>
科目: 来源: 题型:
【题目】钙及其化合物在生产、生活中具有广泛的应用。
(一)钙的广泛用途
(1)高钙奶中含钙,这里的钙是指_____。(选填序号,下同)
a.单质 b.元素 c.原子
(2人体中钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其中磷元素化合价为___________。
(3)混凝土中也含有一定量的含钙物质,钢筋与混凝土混合形成钢筋混凝土,以上叙述中不涉及的材料是____。
a.无机材料 b.合成材料 c.复合材料
(二)轻质CaCO3的制备
某实验小组利用石灰石残渣(杂质不溶于水也不溶于酸)制备轻质CaCO3,同时得到K2SO4,流程如下:
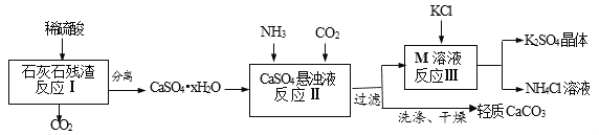
(1)反应Ⅱ中先通NH3,再通CO2的目的是_______,化学方程式为______。
(2)反应Ⅲ中相关物质的溶解度如下表。你认为反应Ⅲ在常温下能实现的原因是______。
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(3)判断CaCO3固体已洗涤干净的方法是____________________;
K2SO4晶体洗涤时,不可选用下列________洗涤剂(填字母编号)。
A.热水 B.冰水 C.饱和K2SO4溶液
(三)CaSO4xH2O成分测定
上述流程中分离所得的CaSO4xH2O中含有一定量的CaCO3。实验小组为了测定CaSO4xH2O中x的值及含量,取22.20g样品加热至900℃,将得到的气体先通过浓硫酸,再通入碱石灰,测得实验数据如下表:
名称 | 浓硫酸 | 碱石灰 |
实验前 | 100.00 | 100.00 |
实验后 | 103.60 | 102.20 |
【资料】已知CaSO4xH2O在160℃生成CaSO4, CaCO3在900℃时分解完全。
(1)CaSO4xH2O的质量为_____。
(2)x的值___________。
(四)CaSO4xH2O的性质探究
CaSO4xH2O受热会逐步失去结晶水,1350℃时 CaSO4开始分解;取纯净CaSO4xH2O固体3.44g,加热,测定固体质量随温度的变化情况如下图所示。
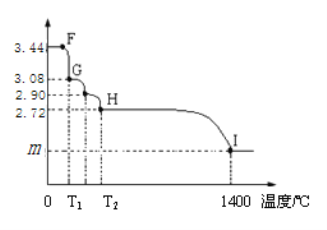
(1)0~T1固体质量没有发生变化的原因可能是_____________。
(2)G点固体的化学式是_________。
(3)将T2~1400℃温度段加热固体所产生的气体通入酸性KMnO4溶液中,溶液褪色,反应后的固体为氧化物,则则H~I段发生反应的化学方程式为__________;m=______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com