
科目: 来源: 题型:
【题目】小明同学想在实验室用NaOH溶液与CO2气体制取Na2CO3溶液。但是经过检验,发现很难得到纯净的Na2CO3溶液,在老师的帮助下查阅了相关资料,制定了计划。
【查阅资料】
①CO2通入NaOH溶液时极易因CO2过量而产生NaHCO3,且无明显现象。
②NaHCO3溶液煮沸时不会发生分解反应;NaHCO3溶液与CaCl2溶液不反应
③NaHCO3+NaOH=Na2CO3+H2O
④Na2CO3+CaCl2=CaCO3↓+2NaCl
【制取步骤】
①量取两份50 mL相同浓度的NaOH溶液备用;
②用一份50 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
③小心煮沸②溶液1-2分钟;
④在得到的③的溶液中加入另一份50 mL NaOH溶液,使其充分混合即得。
【实验探究】制得的Na2CO3溶液中可能含有的杂质是___________。
为检验制得的溶液是否为纯净的Na2CO3溶液,请你与小明同学一起完成下列实验探究:
实验步骤 | 实验现象 | 实验结论 | |
取少量制得的溶液于试管中,加入过量的显中性的CaCl2溶液 | ________。 | 溶液中含有Na2CO3 | |
将上步实验所得混合物进行过滤,将滤液分成两份 | 取其中一份加入足量的____, | 无气泡产生 | 制得的溶液中不含_____, |
取另一份加入______, |
| 制得的溶液中含NaOH | |
【结论】所制得的不是纯净的Na2CO3溶液。
【评价与反思】小芳同学认为可以用过量的Ca(OH)2溶液替代CaCl2溶液进行以上实验,你认为是否可行,并说明原因_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于“一定”的说法中,正确的是
A.含氧化合物一定是氧化物
B.由同种元素组成的物质一定是单质
C.由分子构成的纯净物一定只含一种分子
D.只生成一种物质的化学反应一定是化合反应
查看答案和解析>>
科目: 来源: 题型:
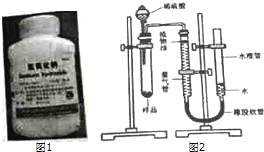
【题目】实验室有一瓶长期放置的氢氧化钠固体(如图1),某兴趣小组同学欲对该固体变质情况进行探究。
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO3
②CaCl2溶液呈中性
③CaCl2+NaHCO3═CaCO3↓+2NaCl
【提出猜想】猜想Ⅰ:固体未变质
猜想Ⅱ:固体全部变质
猜想Ⅲ:固体部分变质
【原因分析】氢氧化钠在空气中变质的原因是 (用化学方程式表示)。
【进行实验】小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是
,为了进一步得出结论,组内其他三位同学分别取小聪实验后的溶液于试管中,进行如下表所示实验:
同学 | 小红 | 小美 | 小伍 |
实验操作 | 加入适量氢氧化钙溶液 | 加入过量氢氧化钙溶液 | 加入过量稀盐酸 |
【实验结论】小红、小美的实验中都观察到有白色沉淀生成且溶液仍是红色,于是他们都出猜想Ⅲ正确。
【反思评价】(一)老师指出,仅凭小红的实验操作和现象无法确定猜想Ⅲ正确,理由是
。
(二)根据小美的结论推测小实验现象是 。
【提出问题】如何测定变质的氢氧化钠固体中碳酸钠的质量分数?
【实验原理】通过测定一定质量样品与足量稀硫酸反应生成二氧化碳的体积来计算碳酸钠的质量分数。
【实验设计】小伍称取一定质量的样品,按如图2装置进行实验(已知该装置气密性良好,水准管高度可以上下调节,量气管是带有刻度的仪器)。
【反思评价】(一)在实验中,若没有植物油,测定结果会 (填“偏大”、“偏小”或“不变”)。
(二)操作中,下列情况不影响测定结果的是 (填字母)。
A、实验前试管中有空气
B、实验中水准管口有水溢出
C、读数时量气管和水准管液面不相平
D、实验后生成的气体在试管中仍有滞留.
查看答案和解析>>
科目: 来源: 题型:
【题目】诺贝尔化学奖获得者以色列科学家丹尼尔谢赫曼在发现准晶体方面作出的突出贡献。准晶体可能具有下列性质,其中属于化学性质的是
A.密度低 B.抗氧化性强 C.耐磨损 D.导电性差
查看答案和解析>>
科目: 来源: 题型:
【题目】学校化学兴趣小组的同学们在学习了酸碱盐的性质后同老师到化学实验室中对酸碱盐进行了探究。
【实验探究一】 酸碱中和反应
实验小组在向氢氧化钠溶液中滴加稀盐酸进行中和反应操作时,忘记预先在氢氧化钠溶液中加入酚酞试液,为判断反应进行的程度,决定对反应后溶液的性质进行以下探究:
【猜想假设】猜想①盐酸不足量; 猜想②恰好完全中和; 猜想③盐酸过量
【方案设计】(并填写表中的空格)
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取适量反应后的溶液于试管中,滴加几滴无色的酚酞试液,振荡 | 溶液变红色 | 猜想①正确 |
方案二 | 用一根洁净的玻璃棒蘸取反应后的溶液滴在pH试纸上,把试纸呈现的颜色与标准比色卡对照 | pH=7 | ______ |
方案三 | 取适量锌粒于试管中,加入适量反应后的溶液 | _______ | 猜想③正确 |
【评价反思】甲同学按方案一进行实验,观察到溶液未变色,则甲同学可以得出的结论是__________(填字母序号)
A、猜想②正确 B、猜想③正确 C、猜想②或③正确
【实验探究二】 探究盐的性质
盐的代表是碳酸钠(Na2CO3),它是食用碱的主要成分(常含有少量的NaCl)。兴趣小组的同学为测定市售食用碱中Na2CO3的含量,设计了如图实验装置:
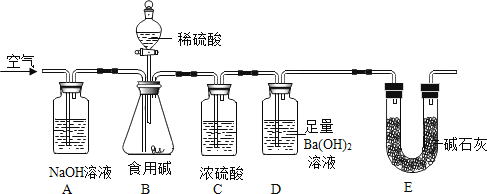
设计思路:用空气将装置B中生成的二氧化碳缓缓吹入装置D中,利用装置D的质量变化测定食用碱中Na2CO3的含量。请结合实验装置和设计思路,回答下面问题:
①装置D中发生反应的化学方程式为___________________________________;
②装置A的作用是____________,装置E的作用是_______________;
③缓缓通入空气的目的是_________________。
④若撤除装置A,直接通入空气会导致实验结果_______(填“偏大”、“偏小”或“不变”),若撤除装置C,对实验结果的影响是_______(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对实验现象的描述,正确的是
A.磷在空气中燃烧产生白雾
B.带火星的木条插入甲烷气体中复燃
C.二氧化碳通入紫色石蕊溶液,溶液变红色
D.硫在氧气中燃烧发出微弱的淡蓝色火焰
查看答案和解析>>
科目: 来源: 题型:
【题目】下列鉴别或检验物质的方法不正确的是
A.用紫色石蕊鉴别二氧化碳和一氧化碳
B.用肥皂水鉴别氢氧化钙溶液和氯化钠溶液
C.与熟石灰混合研磨鉴别氮肥和钾肥
D.用足量稀盐酸检验氢氧化钠是否变质
查看答案和解析>>
科目: 来源: 题型:
【题目】2015年中国航空业高速发展.先进无人机亮相国庆阅兵式,首架大飞机C919总装下线。
(1)用来制造无人机的碳纤维复合材料属于 (填“纯净物”或“混合物”)。已知自然界中存在碳﹣12、碳﹣13、碳﹣14三种不同的原子,这三种原子都属于同种元素的原因是 。
(2)某种无人机的动力来源于锂电池,锂电池放电时的原理是锂和二氧化锰反应生成亚锰酸锂(LiMnO2),则锂电池放电时的能量转化是 。在化合物中锂元素通常显+1价,则LiMnO2中锰元素的化合价是 。
(3)C919发动机上的压气机将高密度空气(高压压缩后的空气)压入燃烧室,能促进航空煤油的燃烧,使燃油消耗减少16%,请你从微观角度解释高密度空气能使航空煤油燃烧更充分的原因是 。该技术的使用对环境保护的意义是 (任答一点)。

查看答案和解析>>
科目: 来源: 题型:
【题目】海水晒盐得到粗盐,剩余的母液称为苦卤,粗盐和苦卤用途广泛。
(1)为了除去粗盐溶液中的Ca2+、Mg2+、SO42﹣,可按照下列实验步骤进行:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤加入适量盐酸。其中步骤③加过量Na2CO3溶液的目的是 。
(2)利用苦卤制取镁,主要流程如图:
![]()
步骤Ⅱ中的试剂a是 。步骤Ⅰ中反应的化学方程式是 。
(3)采用氨碱法生产纯碱,主要流程如图:
![]()
①上述Ⅰ、Ⅱ两个步骤总反应的化学方程式是 。
②从步骤Ⅱ过滤后的滤液中可获得铵态氮肥。检验铵态氮肥的方法是 。
查看答案和解析>>
科目: 来源: 题型:
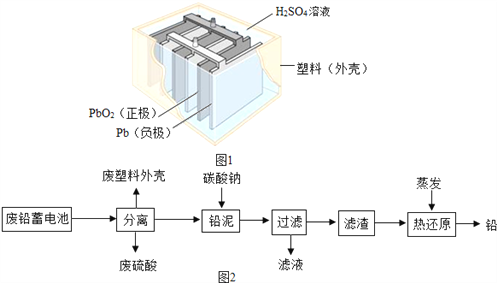
【题目】铅蓄电池在生产、生活中使用广泛。其构造示意图如图1,回答下列问题:
(1)铅蓄电池充电时是将电能转化为_________(填序号)
a、机械能 b、热能 c、化学能
(2)铅蓄电池放电过程中,反应的化学方程式为Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断_________(填“增大”、“减小”或“不变”)。
(3)如图2是回收废铅蓄电池的一种工艺流程:
①从材料分类角度看,塑料是一类_________材料;
②废硫酸可以与氟磷灰石[Ca5(PO4)3F]反应,反应的化学方程式为2Ca5(PO4)3F+7H2SO4═3CaSO4+3Ca(H2PO4)2+2HF,反应产物中可用作化肥的物质是_________
③废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
物质 | CaCO3 | Ca(OH)2 | NH3 | NaOH |
市场参考价(元/kg ) | 1.8 | 2.0 | 6.5 | 11.5 |
已知:2NH3+H2SO4═(NH4)SO4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择_________(填序号)。
a、CaCO3 b、Ca(OH)2 c、NH3 d、NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com