
科目: 来源: 题型:
【题目】为验证“加热碳酸氢铵”所发生的变化,两同学分别用甲、乙所示装置进行实验,发现两实验中碳酸氢铵固体均消失,乙实验中还观察到无水硫酸铜变蓝、浸有酚酞试液的棉球变红、澄清石灰水变浑浊。
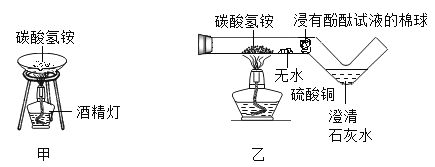
资料:无水硫酸铜呈白色,遇水后呈蓝色。
下列说法错误的是
A. 甲实验不如乙实验环保
B. 只根据甲实验“固体消失” 这一现象,可验证碳酸氢铵发生了分解
C. 乙实验有利于学生分析“固体消失” 的原因
D. 只根据乙实验的现象,可验证NH4HCO3![]() NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】根据如图所示的溶解度曲线,判断下列说法正确的是
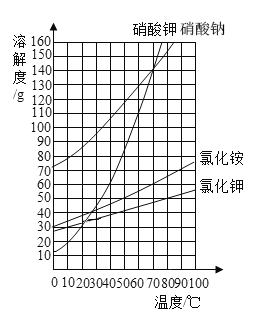
A. 50℃时,分别将等质量的硝酸钾和氯化铵溶于适量的水恰好配成饱和溶液,所得溶液的质量前者比后者大
B. 60℃时,把40g硝酸钾和40g氯化钾分别加入到50g水中,充分搅拌,降温至10℃,剩余晶体的质量氯化钾多
C. 70℃时,50g硝酸钠饱和溶液与100g硝酸钾饱和溶液中所含溶剂质量之比为1:2
D. 80℃时,向100g氯化钾饱和溶液中加入150g硝酸钠,充分搅拌后,最终得到250g溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】我国在2017年“世界环境日”(6月5日)确定的主题是“绿水青山,就是金山银山”.华雪与同学们积极参加了这一主题的活动,在老师的指导下,他们对一造纸厂排放的污水进行检测,发现其主要的污染物为NaOH.为了测定污水中NaOH的含量,他们首先把溶质质量分数为98%(密度1.84g/cm3)的浓硫酸20g,稀释为质量分数为10%的硫酸;然后取80g污水于烧杯中,逐滴加入10%的硫酸至49g时恰好完全反应(假定污水中的其它成分不与硫酸反应).请计算:
(1)把20g上述浓硫酸稀释为质量分数为10%的硫酸,需要水的质量是______g.
(2)污水中所含NaOH的质量分数是___________?(写出计算过程)
(3)取80g该污水于烧杯中放置几天后,若其中的氢氧化钠全部转化为碳酸钠.则此时应逐滴加入10%的硫酸______克才能使碳酸钠恰好完全变成硫酸钠.
查看答案和解析>>
科目: 来源: 题型:
【题目】某校九年级“我们爱化学”活动小组的同学,探究了过氧化钠(Na2O2)与二氧化硫(SO2)反应后所得固体产物的成分,过程如下:
【查阅资料】过氧化钠与二氧化硫反应的化学方程式为:2SO2+2Na2O2=2Na2SO3+O2,2Na2SO3+O2= 2Na2SO4;SO2能使品红溶液褪色.
【提出猜想】猜想1:固体成分为Na2SO3
猜想2:固体成分为Na2SO4
猜想3:固体成分为_________________
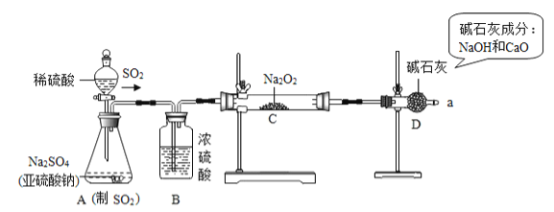
【实验探究】用如图所示的装置进行实验.打开A中分液漏斗的活塞,反应发生(产生足量的SO2)后,用带火星的木条检验从a处导出的气体,木条复燃.实验前称得Na2O2固体的质量为78g,充分反应后称得生成物固体的质量为134g.
【实验结论】
(1)A是制取SO2气体的装置,反应的化学方程式与实验室制取CO2的化学方程式类似,请写出A中发生反应的化学方程式:____________________________.
(2)由题中_________________________________________的实验现象,可推测猜想2是错误的.
(3)装置B的作用是_____________;装置D的作用是_____________________________.
(4)根据反应前后固体的质量,可计算出Na2SO3的质量为______g,Na2SO4的质量为______g.
【总结提升】
(1)若实验前称得Na2O2固体的质量为m1g,充分反应后称得生成物固体质量为m2g,则m2的取值范围是_____________________(用含m1的关系式表示).
(2)请另外设计一种实验方案,定性验证过氧化钠与二氧化硫反应后所得固体产物的成分:_________.
查看答案和解析>>
科目: 来源: 题型:
【题目】已知两种活动性不同的金属在能导电的溶液中接触可以形成原电池,从而加快化学反应速率.在实验室里,我们常用锌与稀硫酸反应来制取氢气(装置如图所示).
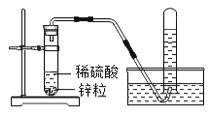
(1)实验室用锌与稀硫酸反应制取氢气的化学方程式为___________.
(2)实验室也可用锌与盐酸反应来制取氢气,但制得的氢气中往往含有HCl气体,若将制得的气体通过盛有NaOH溶液的洗气瓶,_______(填“能”或“不能”)得到纯净的氢气.
(3)点燃氢气之前,先要进行的操作是__________________.
(4)锌与稀硫酸反应时,加入某些盐溶液可使制取H2的速率加快,如__________溶液.
(5)图示装置,_____(填“能”或“不能”,药品可换)用来制取CO2气体.
查看答案和解析>>
科目: 来源: 题型:
【题目】用研磨成粉末的雄黄(化学式As4S4,化学名称为四硫化四砷)泡制的白酒或黄酒称为雄黄酒,是我国传统节日﹣端午节的饮品,也是我国古代人们在夏季除害灭病的主要消毒药剂:雄黄(化学式As4S4),可用作颜料、还原剂和药物等;砒霜(化学式As2O3)是一种剧毒物质,由于古代的生产技术落后,致使砒霜里混有少量的硫和硫化物.当银与砒霜中所含的硫接触时,就可发生化学反应,使银的表面生成一层黑色的硫化银.
(1)雄黄和雌黄两种物质中,硫元素的含量较高的是_________(填化学式).
(2)砒霜(化学式As2O3)的化学名称为_________.
(3)硫化银的化学式为________.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质与空气混合,接触到明火,有发生爆炸危险的是( )
①氢气②汽油蒸气 ③面粉尘 ④棉尘 ⑤天然气
A.①②③④⑤ B.①②③ c.①②③⑤ D.①②
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用KClO3和MnO2混合加热制氧气,并用排水法收集,有以下主要操作步骤:①装药品 ②加热 ③检查装置的气密性 ④用排水法收集氧气 ⑤停止加热 ⑥将导管从水槽中取出,正确的操作顺序是( )
A. ①②③④⑤⑥ B. ③①②④⑥⑤ C. ③①②④⑤⑥ D. ①③②④⑥⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com