
科目: 来源: 题型:
【题目】铝、铁、铜是我们生活中常见的金属。
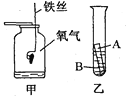
(1)甲图中发生反应后能生成_______色固体,做该实验时,在集气瓶中预先加入少量水可以防止______________。
(2)少伟同学在生活中发现,潮湿空气中的铁比铜更容易锈蚀,由此他认为铁的金属活动性比铜_______(选填“强”或“弱”)。他还想通过一个实验(如乙图)来进一步证明。若乙图中A为金属铁,你认为B是_______溶液。发生该反应的化学方程式是_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D、E、F六种物质,其中F是含铁的矿物显红色,它们之间有如下相互转化的关系。据此,回答下面问题:
①A+F![]() Fe+B ②B+H2O→C
Fe+B ②B+H2O→C
③C![]() B+H2O ④B+Ca(OH)2→D↓+H2O
B+H2O ④B+Ca(OH)2→D↓+H2O
⑤D![]() B+_______ ⑥B+A→2E
B+_______ ⑥B+A→2E
⑦F+HCl→_______+_______
(1)写出下列字母所表示物质的名称:
A_______,B_______,C_______,D_______,E_______,F_______。
(2)写出①~④反应的化学方程式,并指出①反应中的还原剂。
①___________________________, 还原剂_______;
②___________________________________。
③___________________________________。
④___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某一研究性学习小组为测定某铜锌合金的成分,取10 g该合金经粉碎后放入烧杯中,再加入93.7 g质量分数为20%的稀硫酸(反应后硫酸有剩余)。反应过程中烧杯内固体物质的质量与反应时间的关系如下图所示。请回答下列问题:
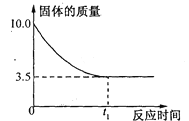
(1)将合金粉碎的目的是______________。
(2)10 g该合金中铜的质量为_______g。
(3)充分反应后产生氢气的质量是多少?
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组为了测定一批石灰石中碳酸钙的质量分数,将石灰石样品研成粉末,然后取一定量的石灰石粉末与过量稀盐酸充分反应(假设石灰石中的杂质既不和酸反应,也不溶于水)。过滤、洗涤、干燥后称量滤渣质量的数据见下表:

(1)该样品中碳酸钙的质量分数的平均值为_______(结果精确到0.1%)。
(2)引起三次实验数据差异的操作原因可能是______________。
查看答案和解析>>
科目: 来源: 题型:
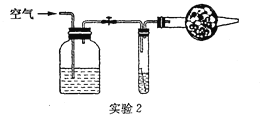
【题目】大多数金属材料在空气中都会生锈。铜锈的主要成分是铜绿[Cu2(OH)2CO3]。某同学利用下图所示的实验1进行实验,研究铜在空气中生锈的条件。一个月后该同学发现B装置中的铜丝生锈了,而A、C装置中的铜丝无明显变化。

试回答下列问题:
(1)该同学得出结论:“铜生锈的原因是铜与空气中的氧气和水相互作用。”该同学得出的结论正确吗?_______,你认为影响铜生锈的因素还可能有_______。
(2)为了验证你的判断,现给你提供实验2所示的装置,从左到右每个仪器所盛放的试剂依次为_______、_______和_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】从用石灰浆抹的墙壁上掉下一块白色固体,为探究其成分,进行如下实验:

由此得出的结论正确的是 ( )
A. 一定有CaCO3和Ca(OH)2
B. 一定有Ca(OH)2,可能有CaCO3
C. 一定没有CaCO3和Ca(OH)2
D. 一定有CaCO3,可能有Ca(OH)2
查看答案和解析>>
科目: 来源: 题型:
【题目】硅酸钠(Na2SiO3)是我国优先发展的精细化学品。用某种石英砂矿石(主要成分是SiO2,还含有少量的CuO、Na2SO4、Na2CO3)制备硅酸钠(Na2SiO3)的流程如下:
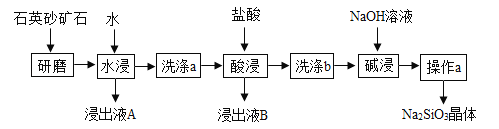
资料:SiO2既不溶于水,也不与盐酸反应。
请问答下列问题:
(1)“研磨”的目的是_______ 。
(2)检验“洗涤a”已洗净的方法是____________。
(3)“酸浸”的化学方程式为____________。
(4)“碱浸”的化学方程式为____________。
(5)“操作a”包含蒸发浓缩、_____ 、过滤、洗涤、干燥等一系列操作。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列实验装置图,回答有关问题。
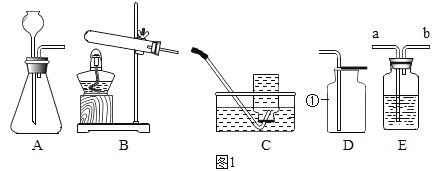
(1)图中标有①的仪器名称__________。
(2)实验室用大理石与稀盐酸反应制取二氧化碳,选用的发生装置是______(填字母),装入药品前应进行的操作是_____________。若要收集干燥的二氧化碳,需将发生装置与装置E和装置______(填字母) 相连,其中装置E内的试剂是___________,气体应从导管_____(填“a”或“b”)端通入。
(3)在2017年江苏省中学化学创新实验调演中,李彬老师设计了“氢氧焰”的实验装置如下:
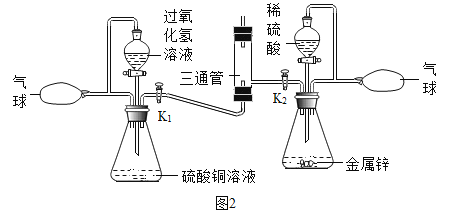
利用氢气与要求的发生装置制取并储存纯净的气体于气球中。A瓶中硫酸铜溶液的作用是______,B瓶中产生气体的化学方程式为_________________。通过玻璃活塞K1、K2分别有序控制氧气和氢气的流量,先后进行如下操作:
①关闭K2,打开K1,通入氧气,将带火星的木条置于三通管口处,观察到_____,说明氧气具有助燃性。将燃着的术条移开,.管口处无火焰。
②关闭K1,打开K2,通入氢气,将燃着的木条置于三通管口处,管口处有火焰。移去燃着的木条,氢气安静地燃烧,说明氢气具有可燃性,该反应的化学方程式为_______。把铁片放在火焰上一段时间,铁片呈红热状。打开K1,通入氧气,铁片迅速熔断被切割,由此得出的结沦是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化锰因在工业生产中应用广泛而备受关注,制备二氧化锰是一项有意义的工作,某研究性小组对此展开了系列研究。
Ⅰ.用高锰酸钾制备
资料一:(1)3K2MnO4+ 2H2SO4=2KMnO4+MnO2↓+2K2SO4+2H2O
(2)K2MnO4易溶于水
实验室加热高锰酸钾制氧气,反应的化学方程式为_____________,其反应类型是_______。将反应后的固体剩余物用稀硫酸浸取一段时间后过滤、洗涤、烘干即得MnO2。用稀硫酸而不用水浸取的原因是____________。
Ⅱ.用硫酸锰制备
电解MnSO4溶液可制得活性MnO2,同时生成氢气和硫酸,该反应的化学方程式为______,一段时间后溶液的pH将_______(填“变大”、“变小”或 “不变”)
Ⅲ.用废锂电池制备
资料二:2Al+2NaOH+2H2O=2NaAlO2+3H2↑
用废锂电池正极材料(LiMn2O4、碳粉等涂覆在铝箔上)制备纳米MnO2,并进行锂资源回收,流程如下:
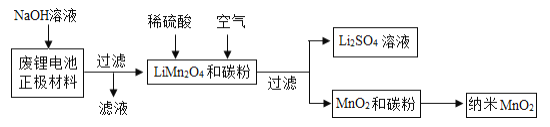
请回答下列问题:
(1)“滤液”中溶质的主要成分是________ (填化学式)。
(2)在实验室进行“过滤”操作时,需要的玻璃仪器有烧杯、漏斗和______。
(3)MnO2与碳粉经下列三步反应制得纳米MnO2:
① 2MnO2+C![]() 2MnO+CO2↑
2MnO+CO2↑
② MnO+H2SO4=MnSO4+H2O
③ 3MnSO4+2KMnO4+2H2O=5MnO2↓+K2SO4+2H2SO4
上述涉及元素化合价变化的反应有_______(填序号)。
IV.用碳酸锰制备
控制一定的温度,焙烧MnCO3制取MnO2的装置如下:
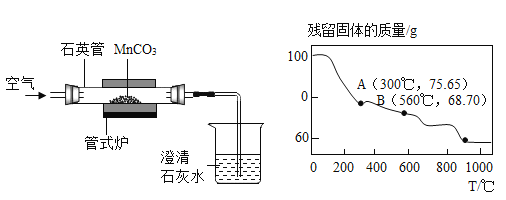
(1)实验中观察到澄清石灰水变浑浊,写出石英管中发生反应的化学方程式___________。
(2)MnCO3在空气中加热易转化为锰的不同氧化物,其残留固体质量随温度的变化如上图所示。图中B点对应固体成分的化学式为______(请写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学就在我们身边,人类的衣、食、住、行都离不开化学。
(1)在厨房里蕴藏着许多化学知识。
①下列食物中,能提供大量维生素的是________________(填字母)。
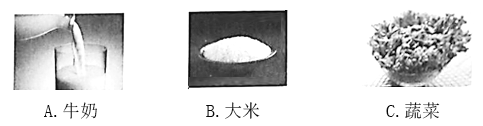
②加铁酱油中的“铁”是指______(填“元素”或“原子”), 身体缺铁会引起贫血。
③厨房中能用来除水垢的物质是____________。
④为防止菜刀生锈,可采用的一种措施是__________。
(2)汽车、高铁、飞机等已成为人们出行的常用交通工具。
①汽油是汽车常用的一种燃料。将石油加热,利用各成分的沸点不同将它们分离可得到汽油,该过程属于______变化。汽车的铅蓄电池工作时,发生如下化学反应:Pb+bO2+2H2SO4=2PbSO4+2H2O该反应涉及的物质中属于氧化物的有__________。
②高铁车头的玻璃是用无机玻璃、树脂、塑料等粘合而成,能耐受强大的撞击力,这种玻璃属于___________(填字母)。
A.复合材料 B.合成材料 C.金属材料·
③制造飞机使用了硬铝(铝铜镁硅合金),其中镁元素的某种粒子结构示意图为![]() ,镁原子的最外层电子数是___________。
,镁原子的最外层电子数是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com