
科目: 来源: 题型:
【题目】颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”。实验室制备的方法是:以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”。请回答以下问题:
(1) 写出生成“纳米铁”的化学方程式____________________________________。
(2) 反应中需要保护气的原因是__________________________________________。
(3) 某化学探究小组为了验证铁、铜、镁、汞的金属活动性顺序,设计了如下实验方案:
① 将大小一样的铁片和镁片分别加入到溶质质量分数相同的稀盐酸中;
② 将铜片加入到硝酸汞溶液中,铜片上出现银白色物质;
③ 将金属片A加入到溶液B中。
a.根据实验①判断出镁的金属活动性比铁强,依据的现象是 _____________________;
b.根据实验②的现象得出的结论是___________________________;
c.要通过实验③得出铁和铜的金属活动性顺序,那么,如果B是硫酸铜溶液,则金属A是______________,如果A是铜,则溶液B是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业明胶是用工业皮革废料,经生石灰浸渍膨胀等序制成的“蓝皮胶”,被不法商人添加到食品、药物中,变成“毒食”、“毒胶囊”。经检测,“毒食”和“毒胶囊”中铬超标数十倍,食用后对肝、肾会造成极大伤害,导致癌症。
⑴上述中的“铬”是指________(填序号)。
A.单质 B.原子 C.元素 D.分子
⑵下图是元素周期表中的一格,从图中获得的信息正确的是________。
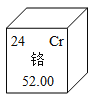
A.该元素的质子数是52 B.该元素在地壳中的含量为24%
C.该元素属于非金属元素 D.该元素的一个原子核中含有28个中子
⑶ 交警常用装有重铬酸钾的仪器检测司机是否酒后驾车,因为酒精可以使橙红色的重铬酸钾变为绿色的硫酸铬,硫酸铬[Cr2(SO4)3]中铬元素的化合价为________ 价。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某金属X有下列相关信息:① 它的主要矿物的化学成分是X2O3;② 它主要通过热还原法冶炼而成;③ 它的年产量位于金属之首。
(1) 据此推断X是_____________(填选项字母)。 A.钛 B.铁 C.铝 D.铜
(2)在高炉中用含X2O3的矿物冶炼该金属的原理是____________(用化学方程式表示)。
(3)同学们设计了如下实验方案测定该矿物中X2O3的质量分数(装置气密性良好;矿物中的杂质不参加反应;假设矿物样品中的X2O3完全反应):
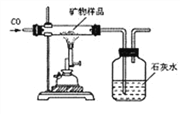
①取矿物样品并称量该样品的质量;
②测出反应前广口瓶和瓶内物质总质量;
③测出反应后广口瓶和瓶内物质总质量; ④计算得出矿物样品中x2O3的质量分数。
a. 你认为,该实验方案___________(填“一定”或“不一定”)能准确测出矿物中X2O3的质量分数,理由是____________________________ .
b. 不改变装置和药品,你还可以通过测定哪些数据,再通过计算得出矿物中X2O3的质量分数:_________________________________。
c. 从环保角度看,该装置的不足之处是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法错误的是( )
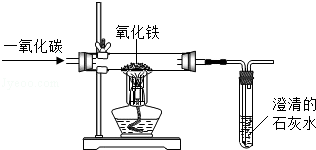
A.实验时,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成
B.实验结束时,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁
C.反应后,玻璃管中的固体物质的质量比反应前减少了,证明一定有铁生成
D.为了减少空气污染,应增加尾气处理装置
查看答案和解析>>
科目: 来源: 题型:
【题目】金属材料在生活、生产中应用十分广泛。

(1)图A是金属的一个应用实例,请说出这利用了金属的什么物理性质(答出一点即可)?______________________________
(2)图B是两块金属片相互刻划后,在纯铜片上有明显的划痕。该实验探究的目的是什么?________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】小明和小英要验证一块石头是否含碳酸钙。
(1)小明说:“只要取一小块石头放在烧杯中,再在石块上倒入盐酸,发现有大量气泡产生,就能证明石块含有碳酸钙。”小英说:“在石块上倒盐酸,产生的大量气泡是盐酸挥发而成的。”小英的说法对吗?_______(填“对”或“不对”)。
(2)小明和小英带着问题请教王老师,在王老师的指导下,进行了下列实验探究,其实验过程如下:①取一小块石块置于烧杯中,滴加盐酸后,发现产生了无色无味气体;②在老师的指导下,取①中的溶液检验,石块中含有钙元素;③他们又设计了如图所示的实验装置,在实验中观察到广口瓶中有浑浊现象产生。
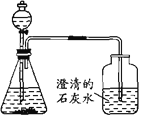
在上述实验中,他们进行的是_______实验研究(填“定性”或“定量”)。
(3)假若称取10.0 g石块与足量的稀盐酸反应(杂质不与盐酸反应),并用饱和石灰水吸收,得到的沉淀经适当处理后得干燥固体7.5 g。计算:
①石块中含碳酸钙的质量分数_______________;
②已知CO2在标准状况下的密度为1.98 g/L,则生成标准状况下CO2气体的体积为______________毫升?
查看答案和解析>>
科目: 来源: 题型:
【题目】李红在查阅资料时发现木炭也能夺取含氧化合物中的氧,表现出还原性。如:CO2+C![]() 2CO,于是她对过量木炭和氧化铁在高温条件下反应,最终产生的气体是什么产生兴趣,决定进行探究。请回答下列有关问题(提示:铁、氧化铁均能与稀盐酸发生化学反应)。
2CO,于是她对过量木炭和氧化铁在高温条件下反应,最终产生的气体是什么产生兴趣,决定进行探究。请回答下列有关问题(提示:铁、氧化铁均能与稀盐酸发生化学反应)。
【提出问题】过量木炭和氧化铁反应产生的气体是什么呢?
【猜想和假设】猜想①:可能是CO2;猜想②:可能是CO;猜想③:_______。
【实验方案与现象】将产生的气体通入澄清石灰水,澄清石灰水变浑浊。
【结论】猜想①正确。
【反思与评价】小雨不同意李红的观点,理由是_______________________________。
于是小雨进行如下的实验以验证猜想:
①称取3.2 g的氧化铁与2g木炭均匀混合,放进18.48 g的试管中,加热。
②完全反应后,冷却至室温,称得试管和固体的总质量为22.24 g。
③往试管中加入足量稀盐酸,然后过滤、洗涤、烘干、称量,得到1.52 g黑色粉末。
【数据处理】参加反应的碳元素的质量为_______,氧元素的质量为_______。
【得到结论】根据数据处理结果,得到原猜想③成立,理由是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表提供了在一定条件下,水与一些金属发生反应的信息。
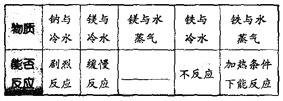
(1)请根据表中已有的知识,将表格填写完整。___________________
(2)已知铁与水蒸气在加热条件下反应生成四氧化三铁和氢气,该反应的化学方程式为_______。
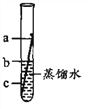
(3)铁虽然常温下不与水反应,但铁制品在潮湿环境中易生锈。某同学进行了如图所示的实验。一周以后发现铁钉表面生锈。图中a、b、e三处锈蚀情况最严重的是_______(填字母),产生该现象的原因是____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】人类的生产和生活都离不开金属。
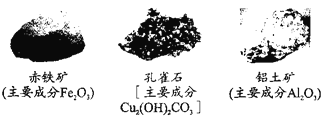
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是_______。金属以矿物形式存在,下列矿石的主要成分属于氧化物的是_______(填化学式)。
(2)铁是应用最广泛的金属。
①工业上常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为________。
②使用过的菜刀、铁锅等铁制品,清洗后需及时擦干放置,可以减少_______对铁锈蚀的影响。
(3)将一定量的锌加入稀硫酸、硫酸亚铁和硫酸铜的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。滤渣和滤液中一定含有的物质是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钛因为有神奇的性能越来越引起人们的关注。常温下钛不与非金属及强酸反应,加热时却可以和常见的非金属单质反应。钛是航空、军工、电力等工业领域的重要原材料。地壳中的钛矿石之一是金红石(主要成分是TiO2),目前大规模生产钛的方法是:
(1)使金红石与炭粉混合,在高温条件下反应,再通入氯气,制得TiCl4和一种可燃性气体。该反应的化学方程式是_____________________。
(2)在氩气的气流中,高温下用过量的镁和TiCl4反应可制得金属钛。写出该反应的化学方程式:___________________________________。
(3)从上述反应的混合物中分离出金属钛。写出简单的分离步骤和有关的化学方程式。_____________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com