
科目: 来源: 题型:
【题目】同学们在实验室用5%的过氧化氢溶液制取氧气并进行氧气部分性质实验,具体操作如下:
(1)溶液配制:用50mL 30%的过氧化氢溶液配制5%的过氧化氢溶液.溶液配制过程中,除用到玻璃棒外,还需用到下列仪器中的
A、托盘天平 B、烧杯 C、漏斗 D、量筒 E、胶头滴管
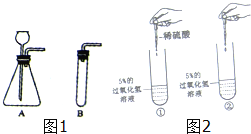
(2)气体制备:用配制好的5%的过氧化氢溶液和二氧化锰制取氧气.请你在如图1A、B两套装置中选择其中一套,并说明选择的理由: (合理即可).
(3)性质实验:小明用收集好的氧气,进行了铁丝燃烧的实验.实验前,它在集气瓶底部 ,然后把光亮的细铁丝盘成螺旋状,在铁丝下端系一根火柴,将火柴点燃,待火柴快燃尽时,缓慢插入集气瓶中,观察到的现象是 .
(4)拓展延伸:小亮同学在上述制取氧气的实验过程中,不小心把硫酸铜溶液滴加到了盛有5%的过氧化氢溶液中,立即产生大量气泡,于是引起了小亮同学的探究兴趣.
【提出问题】是哪种粒子能使过氧化氢分解的速率加快呢?
【查阅资料】硫酸铜溶液中含有三种粒子:H2O、SO42﹣、Cu2+
【猜想与假设】Ⅰ、不可能是H2O,理由是 ;
Ⅱ、可能是SO42﹣;
Ⅲ、可能是Cu2+.
【实验验证】如图2所示:
在实验①中加入稀硫酸后,无明显变化,说明 不能使过氧化氢的分解速率加快;
在实验②中加入 后,观察到有大量气泡产生,进一步证明能使过氧化氢分解速率加快的是 .
【结论】实验证明,硫酸铜在该反应前后的质量和化学性质都没有发生变化,硫酸铜是过氧化氢分解的催化剂.
【反思与交流】Ⅰ、检验实验②中产生气体的方法是 ;
Ⅱ、写出过氧化氢在硫酸铜催化作用下发生反应的化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】硬水中含较多的Ca2+、Mg2+,常用 区分硬水和软水;“84”消毒液的有效成分NaClO中氯元素的化合价为 ;Cl2常作自来水消毒剂,其实验室制法为:MnO2+4HCl(浓) △ X+Cl2↑+2H2O,X的化学式为
查看答案和解析>>
科目: 来源: 题型:
【题目】探究金属性质时,将锌粒放入硫酸铜溶液中,锌粒表面有紫红色物质析出,还有无色无味气体产生的“异常”现象。推测该气体可能是
A.氢气 B.二氧化硫 C.二氧化碳 D.一氧化碳
查看答案和解析>>
科目: 来源: 题型:
【题目】某种药品说明书里标有:本品每克含碘150毫克,镁65毫克,锌1.5毫克,锰1毫克,这里的碘、镁、锌、锰指的是
A. 原子 B. 分子 C. 单质 D. 元素
查看答案和解析>>
科目: 来源: 题型:
【题目】根据图示信息,用化学用语填空:

(1)写出溶质中金属元素的元素符号 ;
(2)写出溶液中大量存在的阴离子的符号 ﹣ ;
(3)标出溶剂中氧元素的化合价 ;
(4)写出该溶液中溶质的化学式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是初中化学中的一些重要实验,请回答:
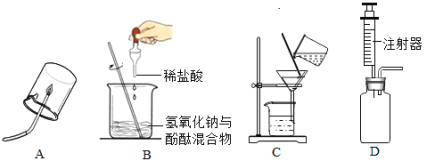
(1)A是氢气或甲烷的燃烧实验,点燃前必须 ;
(2)B实验中能够说明盐酸与氢氧化钠发生了反应的现象是 ;
(3)C是除去粗盐中难溶性杂质实验中的过滤操作,其中玻璃棒的作用是 ;
(4)D是用碳酸钠粉末与稀盐酸反应制取二氧化碳的简易装置,此装置的最大优点是 .
查看答案和解析>>
科目: 来源: 题型:
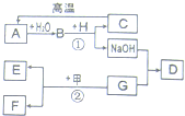
【题目】A﹣H是初中化学中常见物质,已知A为金属氧化物,C为石灰石的主要成分,D为蓝色沉淀,G和H均为只含一种溶质的溶液,甲为镁粉和锌粉的混合物.“→”表示物质间存在相应的转化关系(部分生成物未标出),他们之间的关系如图所示,请回答下列问题:
(1)A的化学式 ;D的化学式 ;
(2)写出B与H反应的化学方程式 ;
(3)将溶液G和甲充分反应后过滤,向滤渣中加入稀盐酸,有无色气体放出,则滤渣中一定含有 .
(4)举出B物质在农业生产中的一种用途 .
查看答案和解析>>
科目: 来源: 题型:
【题目】分子和原子的主要区别是 ( )
A.分子质量大,原子质量小 B.在化学反应中分子可分,原子不可分
C.分子间有空隙,原子间无空隙 D.分子体积大,原子体积小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com