
科目: 来源: 题型:
【题目】(5分)自来水生产中通常用适量的氯气杀菌消毒,以食盐(NaCl)为原料制取氯气的流程如下图所示,根据题意填写下列空白:
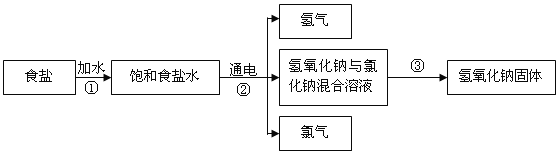
(1)上述过程中的涉及的物质属于碱的是__________(写化学式)。
(2)过程②发生反应的化学方程式为2NaCl+2X 通电 2NaOH+H2↑+Cl2↑,其中X的化学式为_________,
在反应前后Cl元素的化合价分别为_______________。
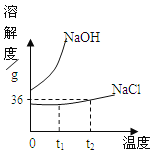
(3)氯化钠和氢氧化钠溶解度曲线如图所示,温度为t2时,过程①要将36g氯化钠配制成饱和溶液,需要水的质量为_____g;过程③要得到氢氧化钠固体所采取的结晶方法为 ____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D表示4种物质,其微观示意图见下表,A和B在一定条件下反应生成C和D,下列叙述不正确的是
物质 | A | B | C | D |
|
微观示意图 |
|
|
|
|
A.该反应类型为置换反应 B.氧元素的化合价反应前后发生了改变
C.反应前后原子的种类和个数不变 D.参加反应的A、B物质的分子个数比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】对下列事实解释不正确的是
选项 | 事实 | 解释 |
A | 氧气可以压缩于钢瓶中 | 分子间有间隔 |
B | 不同的花儿有不同的香味 | 不同的分子性质不同 |
C | 变瘪的乒乓球放入热水中能鼓起来 | 球内气体分子受热膨胀变大 |
D | 炎热的夏天自行车车胎容易爆裂 | 夏天温度高,分子间间隔变大 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)A铁丝在氧气中燃烧的试验中,集气瓶中预先装少量水的目的是_________________.
(2)用量筒测定液体的体积,俯视液面时测量结果比实际值______。(填偏大,偏小,不变)
查看答案和解析>>
科目: 来源: 题型:
【题目】(12分)油条是人们喜欢的早点,中国油条的传统加工配方是用明矾(KAl(SO4)2)作为膨松剂,明矾常引起铝残留影响人体健康问题,现在的膨松剂常用臭粉(碳酸氢铵)、小苏打。
(1)油条中的主要营养素是油脂和
(2)“铝残留影响人体健康”中的铝是指 (选填“原子”或“元素”或“单质”)
(3)已知某膨松剂含碳酸氢铵、碳酸氢钠中的一种或两种,兴趣小组对该膨松剂进行如下探究:
【查阅资料】① 2NaHCO3![]() Na2CO3+H2O+CO2↑; NH4HCO3
Na2CO3+H2O+CO2↑; NH4HCO3 ![]() NH3↑+H2O+CO2↑。
NH3↑+H2O+CO2↑。
②氨气能使湿润的红色石蕊试纸变蓝。浓硫酸可用于吸收氨气。
③ 碱石灰是固体氢氧化钠和氧化钙的混合物,能作干燥剂,和二氧化碳反应,不与氨气反应。
实验I:探究膨松剂的成分
按下图所示连接好装置。
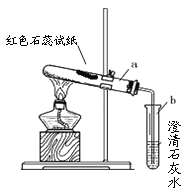
实验记录
实验操作 | 主要实验现象 | 实验结论 及解释 | |
① | 检查装置的气密性 | 装置的气密性良好 | |
② | 点燃酒精灯。 | 试管中白色固体减少,红色石蕊试纸 ,澄清石灰水变浑浊。 | 有二氧化碳和氨气生成 |
③ | 继续充分 加热 | 试管中仍有固体。 | |
得出结论:该膨松剂的成分为 (写出化学式)。
实验II:探究产生气体的量
①测定二氧化碳的质量:如下图所示装置(气密性良好,各装置中的试剂为足量)。
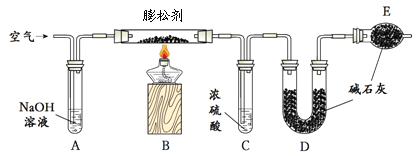
将8g膨松剂装入装置B中,加热前,先对已连接好的装置A、B和C通一段时间的空气,再连接装置D、E;加热过程中,装置C的作用是 ;停止加热后,继续通入一段时间的空气,目的是 。实验中,测定实验前后装置 (填字母序号)的质量,其质量差即为样品产生的二氧化碳气体的质量。若没有装置A,可能会造成测定结果 (填“偏大”、“不变”或“偏小”)。
②测定氨气的质量:将上图装置中 (填字母序号) 的连接顺序为对调。另取8g膨松剂装入装置B中,通过测定实验前后盛有浓硫酸的试管质量,其质量差即为样品产生的氨气的质量。若该装置的质量增加了1.36g,则同时共产生二氧化碳质量是多少? (有计算过程,结果精确到0.01)
查看答案和解析>>
科目: 来源: 题型:
【题目】(12分)盐城濒临黄海,海洋资源非常丰富。
(1)海水晒盐得到的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
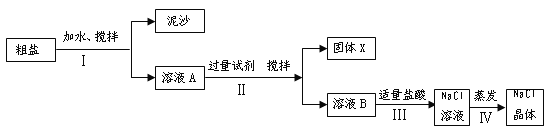
请回答下列问题
①海水是 (填“纯净物”或“混合物”) 海水晒盐得到粗盐是_____变化(填“物理”或“化学”)_
②步骤Ⅰ和步骤Ⅱ都涉及到的实验操作是 。
③步骤Ⅳ加热蒸发时,待 时停止加热。
④为了除去溶液A中的可溶性杂质,步骤Ⅱ中加入过量的试剂是Na2C03、NaOH、BaCl2 , 写出步骤Ⅲ中加入适量盐酸时发生的中和反应的化学方程式 。如果步骤Ⅱ中加入过量的试剂顺序不当,将导致得不到纯净的NaCl,下列加入试剂顺序不当的是
A Na2C03、NaOH、BaCl2 B BaCl2、NaOH 、Na2C03
C NaOH、BaCl2、Na2C03 D.Na2C03、BaCl2 、NaOH E. BaCl2、Na2C03、NaOH
(2)某实验小组利用上面提纯的氯化钠,配置100g 16%的氯化钠溶液。
①他应称取氯化钠质量是 g ,量水时选用量筒的量程最好是
A.10ml B.20ml C.50ml D.100ml
②称量氯化钠时发现天平的指针偏左,正确的处理方法是
A.增加砝码 B.减少药品 C.减少砝码 D.增加药品
③实验中实际配制的溶液中溶质质量分数小于16%,造成的可能原因有__ ; _;(不少于两点)
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是甲、乙、丙三种物质的溶解度曲线。下列说法不正确的是
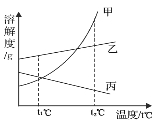
A.t2℃时,三种物质溶解度大小依次为:甲>乙>丙
B.若乙中含有少量杂质甲,可用蒸发结晶的方法进行提纯
C.等质量的甲、乙两种溶液,由t2℃降到t1℃时,析出甲的质量多
D.三种不饱和溶液都可以通过增加其溶质的方法变成饱和溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】(7分)镁与NH4Cl溶液反应,不仅有一种盐生成,还有气泡产生。为确定气体的成分,进行下列实验探究。
(一)探究:气体可能是HCl、02、NH3、H2中的一种或几种。
(二)实验:
(1)甲同为确定是否含有HCl,他将气体通入酸化的硝酸银溶液中,无明显现象,则该气体中_ HCl (填“有”或“无”)。
(2)乙同学认为只有02,则可用_ 来检验。实验证明乙同学的观点不正确。
(3)丙同学为判断是否含有H2,同时确定气体成分,通过查阅资料得知:
2NH3+3CuO == 3Cu+N2+3H20于是他设计了如下图实验装置:
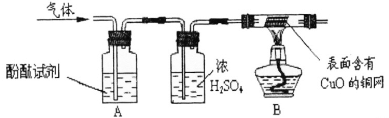
(三)实验现象与结论:A中观察到_ ,证明有NH3; B中玻璃管内观察到_ ,证明有H2。
(四)实验反思:
(4)浓硫酸的作用是_ 。
(5)大家认为丙同学在加热之前,应对气体先_ 以确保安全。
(6)写出Mg与NH4Cl溶液反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com