
科目: 来源: 题型:
【题目】在学习复分解反应发生条件时,小含同学进行如下探究:判断稀硫酸与试管中的四种溶液是否发生反应 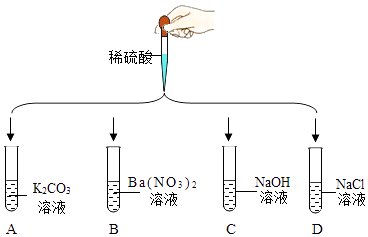 【进行实验】
【进行实验】
(1)试管A中可观察到的现象是;
(2)试管B中发生反应的化学方程式为;
(3)试管C中发生反应的微观实质是;
(4)实验结束后,向试管D中加入物质可证明溶液中仍有酸.
A.酚酞试液
B.Fe2O3
C.Cu(OH)2
D.AgNO3
(5)【反思与评价】 根据以上实验可知判断复分解反应发生的依据是 .
NaNO3、Ca(OH)2、BaCl2、Na2CO3四种物质中,任意两种物质之间,能够发生复分解反应的有个.
查看答案和解析>>
科目: 来源: 题型:
【题目】强化安全意识,提高安全素养,下列做法正确的是( )
A. 加油站内,禁止接打手机
B. 电器着火,马上用水浇灭
C. 室内失火,立即打开门窗排除浓烟
D. 被火势困在高层建筑内,乘坐楼内电梯撤离
查看答案和解析>>
科目: 来源: 题型:
【题目】乌金塘水库是葫芦岛市的重要水源之一,将水库的水净化为自来水的过程中,下列描述缺乏科学性的是
A. 加入明矾使悬浮小颗粒凝聚 B. 投药杀菌消毒
C. 通过活性炭吸附色素和异味 D. 通过过滤除去可溶性杂质
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是集中实验室制取气体常用的装置,请回答下列问题 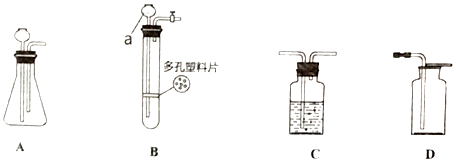
(1)仪器a的名称;
(2)指出A装置中的一处错误;
(3)装置改正错误后,A与B均为气体发生装置,其中B比A的优点为 , 利用AD装置可以制取气体的化学方程式 , 用D装置收集该气体时,验满的方法为;
(4)为获得干燥的气体,需将C装置连接在AD或BD装置中间,C装置中应装的试剂为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】实验装置设计合理,并且结论正确的是( )
A.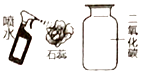 二氧化碳能使石蕊变红
二氧化碳能使石蕊变红
B.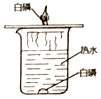 可燃物燃烧需温度达到着火点
可燃物燃烧需温度达到着火点
C.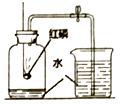 氧气约占空气体积的五分之一
氧气约占空气体积的五分之一
D.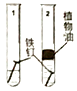 铁生锈与氧气和水有关
铁生锈与氧气和水有关
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列如图1实验装置图,回答有关问题, 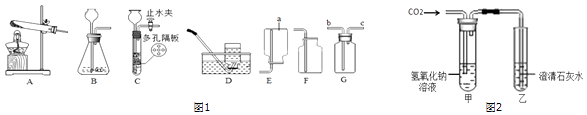
(1)装置图中仪器a的名称为 .
(2)用氯酸钾和二氧化锰混合共热制取较纯净的氧气,可选用的装置组合是 , 写出发生反应的化学方程式 . 若改用高锰酸钾制取氧气,发生装置应作的改动是 .
(3)实验室利用B装置制取二氧化碳的化学方程式为 , 如果利用G装置收集二氧化碳,气体应从端通入(填“b”或“c”),用C装置代替B装置,收集满气体后,C装置的操作是 .
(4)为研究二氧化碳会与氢氧化钠发生反应,采用图2装置进行实验,通入二氧化碳后,看到现象,说明二氧化碳与氢氧化钠发生反应;若对原装置改动继续实验,看到石灰水变浑浊,也能达到目的,改进的方法是; 若将二氧化碳通入氢氧化钠的酒精溶液,观察到溶液由澄清变浑浊,解释原因 .
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸是一种酸,草酸晶体(H2C2O42H2O)易溶于水,熔点较低,加热会熔化、气化和分解.草酸(H2C2O4)与氢氧化钙的反应:H2C2O4+Ca(OH)2═CaC2O4↓(白色)+2H2O. 【分析讨论】
(1)草酸的水溶液的pH7(填“>”、“=”、“<”)
(2)实验室可用加热草酸晶体分解的方法获得CO ①先加热草酸晶体生成CO、CO2和H2O,其化学方程式是;
②再将生成的混合气体通过NaOH溶液吸收CO2 , 其化学方程式是;
③最后用图1装置收集CO,气体应从端进入(选填“a”或“b”).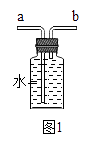
(3)【实验反思】 甲认为图2中试管口应略向下倾斜,老师、同学讨论后一致认为装置是正确的,理由是 . 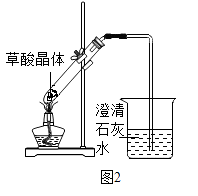
(4)实验中观察到澄清石灰水变浑浊,乙认为一定是由草酸晶体受热分解产生的CO2所导致,丙认为乙的结论不严密,理由是 .
(5)【生活链接】菠菜营养丰富,但菠菜豆腐同食,易得结石(主要成分:草酸钙晶体),小组同学对草酸钙晶体的性质及组成产生了兴趣. 【性质探究】按图3装置将草酸钙晶体(CaC2O4xH2O)样品高温加热,使其完全分解并检验产生的气体.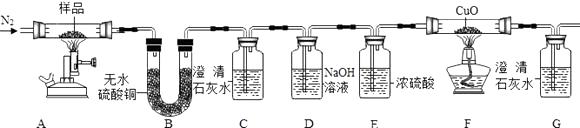
【问题讨论】
B中观察到现象,说明反应生成了水;
(6)C、G中澄清石灰水均变浑浊,说明反应还生成和气体.
(7)反应开始前通入氮气的目的是 .
(8)【组成确定】 利用热分析仪对草酸钙晶体(CaC2O4xH2O)进行热分解,获得相关数据,绘制成固体质量﹣分解温度的关系如图4.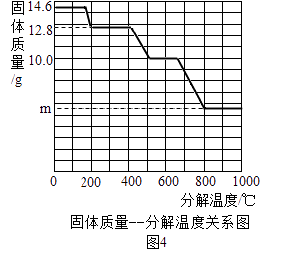
①温度为200℃左右时,晶体全部失去结晶水,晶体中结晶水的质量为g.
②计算CaC2O4xH2O中的x(CaC2O4的相对分子质量:128),x= .
③800℃以上时,经检验残留固体为氧化物,图中m的值是 .
④写出固体质量由12.8g变为10.0g时的化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室以软锰矿(主要成分为MnO2 , 还有少量FeO、Fe2O3、MgO和Al2O3杂质)为原料制备高锰酸钾的流程如图: 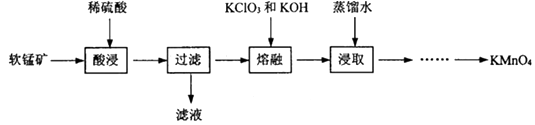
(1)“酸浸”目的是除去MnO2中的杂质,需要加热的目的是;此过程中发生的化学反应方程式是 . (任写一条)
(2)“熔融”过程中,MnO2被氧化成K2MnO4 , 同时得到KCl, ①该反应的化学方程式为 .
②加入KClO3应过量的原因除了提高MnO2利用率,还有 .
(3)浸取后为了得到较纯净的KMnO4晶体,通过蒸发浓缩、冷却结晶、过滤出KCl溶液,将晶体洗涤、低温烘干等一系列操作,其中采用低温烘干的原因是 , 写出“浸取”过程中,Cl2和K2MnO4的反应方程式 .
(4)在氧化、还原反应中,氧化剂的元素化合价降低,还原剂的元素化合价升高,以上流程中起到氧化作用的物质是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com