
科目: 来源: 题型:
【题目】早在春秋战国时期,我国就开始生产和使用铁器。工业炼铁把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
(1)一氧化碳还原氧化铁的化学方程式为:。其中,石灰石起的作用是。
(2)(一)甲组同学在学习炼铁的相关内容时,对炼铁时还原剂的选择进行了如下探究。
【提出问题】
单质碳也具有还原性,碳还原氧化铁的化学方程式为。为什么工业上不用焦炭作为还原剂直接还原铁矿石?
(3)【猜想与假设】
焦炭和铁矿石都是固体,接触面积小,反应不易完全。
【进行实验】
①称取两份相同质量的氧化铁粉末。一份与足量的碳粉均匀混合放入图1装置A的试管中;另一份放入图1装置B的玻璃管中。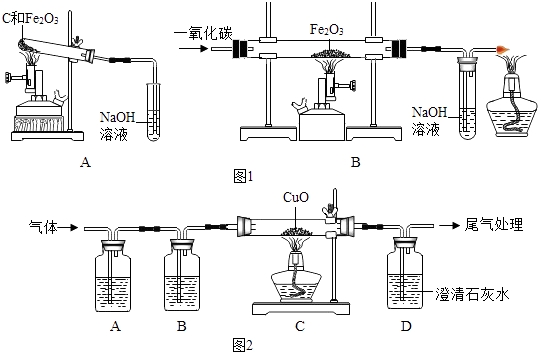
②图1装置A和B两组实验同时开始进行。在图1装置B的反应中,实验开始前应先(选填“通CO”或“加热”); 实验结束后应继续通入CO直至冷却至室温,其原因是。
(4)【实验现象】
当图1装置B的玻璃管中固体完全由时(选填“红色变为黑色”或“黑色变为红色”),图1装置A的试管中仍有。
(5)【解释与结论】
焦炭和铁矿石都是固体,接触面积小,反应确实不易完全,这可能是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因。
【完善实验】
联想到单质碳的一些化学性质,甲同学认为在碳还原氧化铁的反应中可能还会有CO产生。为了证明碳还原氧化铁所得的气体中含有CO和CO2 , 将该气体通过图2的检验装置。图2A装置中的试剂是(写名称,下同) , 图2B装置中的试剂是氢氧化钠溶液,用以吸收二氧化碳(2NaOH+CO2═Na2CO3+H2O );证明原混合气体中CO2存在的化学方程式;证明原混合气体中CO存在的实验现象是;经过检验,证实碳还原氧化铁所得的气体中确实含有CO和CO2。
(6)(二)精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】
利用绿矾制备精还原铁粉的工艺流程如下:![]()
粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为FexOy+yH2 ![]() xFe+yH2O,Fe3C+2H2
xFe+yH2O,Fe3C+2H2 ![]() 3Fe+CH4。
3Fe+CH4。
【含量测定】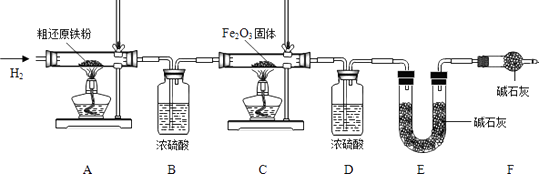
为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按图装置进行实验。
已知3CH4+4Fe2O3 ![]() 3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃酒精灯,(填“先点A处,后点C处”或“先点C处,后点A处”);
④分别熄灭A处、C处酒精灯;
⑤再缓缓通入少量H2;
⑥再次称量必要装置的质量
(7)步骤②的目的是 , 验证该步骤目的达到的实验方法是;
(8)若缺少装置D,则所测氧元素的质量分数将(填“偏大”,“偏小”或“不变”)。
(9)粗还原铁粉样品的质量为15.000g,装置B、E分别增重0.270g和0.330g,则计算样品出中碳、氧元素的质量分数分别是。(列出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】据报道,用于清洗龙虾的“洗虾粉”中含有柠檬酸钠、亚硫酸钠[Na2SO3]等,可能会对人体的健康产生危害。Na2SO3中S元素的化合价为( )
A.-2B.+2C.+4D.0
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验现象描述正确的是( )
A. 红磷在空气中燃烧产生大量白雾
B. 细铁丝在氧气中燃烧,火星四射,生成了四氧化三铁
C. 铁锈与稀盐酸反应后溶液颜色由无色变成了黄色
D. 将紫色石蕊试液滴入到稀氢氧化钠溶液中变红
查看答案和解析>>
科目: 来源: 题型:
【题目】高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
(1)试管尾部放一团湿棉花的目的是。
(2)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是。写出该反应的化学方程式。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
与盐酸反应 | FeCl2+H2O | FeCl3+H2O | FeCl2+FeCl3+H2O |
【初步验证】
试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】
猜想一:剩余固体是;猜想二:剩余固体是。
(4)【实验探究】
实验操作 | 实验现象及结论 |
(5)【实验结论】铁和水蒸气反应的化学方程式为。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上可以用FeSO4制取铁。
方案一: ![]()
(1)已知FeSO4在高温的条件下会生成Fe2O3和两种硫的氧化物,请写出相应的化学方程式。
(2)实验室中完成反应②时,固体颜色的变化是。
方案二:已知FeCO3 ![]() FeO+CO2↑;C+CO2
FeO+CO2↑;C+CO2 ![]() 2CO
2CO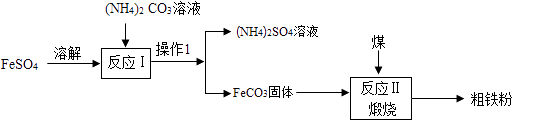
(3)方案二:已知FeCO3 ![]() FeO+CO2↑;C+CO2
FeO+CO2↑;C+CO2 ![]() 2CO
2CO
硫酸铵在农业上可以用作氮肥,其中N元素的质量分数为。
反应Ⅱ中往往还加入碳酸钙,碳酸钙能将煤燃烧生成的含硫物质除去。焙烧时间与铁金属化率的转化关系如图: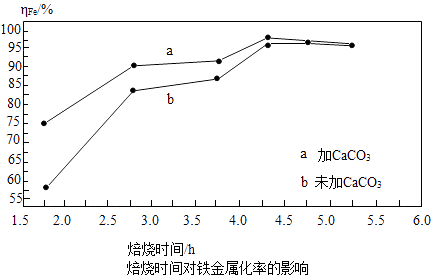
(4)曲线a、b差异的原因是。
(5)反应Ⅱ加入煤的作用是、。粗铁粉中一定含有的杂质为。
(6)【反思】工业上常采用方案二制取粗铁粉。请分析不用方案一的原因是。
查看答案和解析>>
科目: 来源: 题型:
【题目】用化学知识可以解决厨房中的许多问题,如:
(1)用洗洁精清洗碗上的油污,利用了_______________;
(2)除去冰箱中的异味,常用___________吸附;
(3)下列物质与水充分混合后,不能形成溶液的是___________.
A 食用油 B 食盐 C 面粉 D 蔗糖
查看答案和解析>>
科目: 来源: 题型:
【题目】根据你的生活经验和所学的化学知识判断,下列做法不科学的是
A. 用盐酸可区分黄金和黄铜(铜锌合金)
B. 用肥皂水区分硬水和软水
C. 用燃烧的方法除去二氧化碳中混有的一氧化碳
D. 不能用“钢丝球”打磨铝锅表面
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关金属的叙述,正确的是
A. 铝能制成铝箔是因为铝有很好的抗腐蚀性
B. 合金的硬度比其纯金属的硬度小
C. 铝、铁、铜都是银白色金属
D. 钢中含碳量低于生铁中的含碳量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com