
科目: 来源: 题型:
【题目】下列对物质的归类不正确的是
选 项 | 归 类 | 内容 |
A | 常见氮肥 | 碳铵、氨水、尿素 |
B | 同一物质 | 烧碱、火碱、苛性钠 |
C | 清洁能源 | 风能、氢能、太阳能 |
D | 常见氧化物 | 干冰、生石灰、赤铁矿 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】空气中氧气含量测定的再认识。
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1)。
(1)该实验中选择使用汞的优点有。
A.实验过程中没有污染
B.在汞槽中起到液封的作用
C.生成的化合物加热分解又能得到汞和氧气
D.能将密闭装置内空气中的氧气几乎耗尽
(2)【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的化学方程式 , 其反应类型为。
兴趣小组用该方法测出的氧气含量常常远低于21%。
(3)【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行猜想】①;② , 装置内氧气有剩余;……
(4)【实验与交流】在老师的指导下,小明分别用过量的红磷(着火点240℃)和白磷(着火点40℃)进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%。请从燃烧条件的角度回答产生上述结果的主要原因。。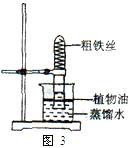
(5)【实验探究1】小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量。于是进行了实验(装置如图3)。通过7天测得的数据计算出空气中氧气的含量为19.13%。
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点。(填字母)。
A.装置内残留的氧气更少
B.反应更彻底,实验结果更准确
C.铁丝生锈比红磷燃烧反应更快
(6)【实验探究2】为了加快反应速率,小明通过查闻资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。8分钟后测得的数据如下表:
实验前的体积 |
| |
集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
131 mL | 90.0mL | 63.6mL |
请计算出空气中氧气含量(计算结果保留一位小数)。
(7)【结论与反思】通过上述实验探究,选择(填字母)进行实验,可较为快速地完成实验并减小实验误差。
A.红磷
B.白磷
C.铁粉、炭粉、氯化钠、蒸馏水
(8)【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿主要成分为Cu2(OH)2CO3]。若将图3装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由。、理由(填字母)。
A.空气中CO2含量只有约0.03%,铜不能将装置内的氧气几乎耗尽
b.铜丝反应比铁丝快
c.反应更彻底
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列装置,结合所学化学知识回答下列问题。
(1)写出标号仪器a的名称:;
(2)实验室若选择装置B用高锰酸钾制取氧气时,你认为B装置存在的问题是 , 该反应的化学方程式是;
(3)实验室里,常用亚硫酸钠固体和浓硫酸反应制取SO2;通常情况下,SO2是一种无色、有刺激性气味的有毒气体,密度比空气大,易溶于水且水溶液显酸性。实验结束后多余的SO2气体要用氢氧化钠溶液吸收,反应的化学方程式为:。为便于处理多余的有毒气体,实验室制取并收集SO2气体可以选择装置(填字母)。
查看答案和解析>>
科目: 来源: 题型:
【题目】镁是20世纪才发展起来的年轻金属,广泛应用于航空、汽车、船舶、通讯电子和国防工业等。兴趣小组同学对金属镁进行了如下探究。
(一)有关金属镁的化学性质探究
兴趣小组同学根据金属的化学性质,知道金属镁能与O2、稀盐酸和CuSO4溶液反应,并设计了如下实验进行验证(以下实验用镁条、镁条均已除去氧化膜)。
(1)兴趣小组同学把镁粉轻轻洒在酒精灯的火焰上,观察到火焰上跳动闪烁着点点银色火花,如绽放的美丽烟花。该反应的化学方程式是_______________________。
(2)兴趣小组同学探究镁与稀盐酸的反应,除观察到预期现象外,还观察到有灰白色沉淀生成的“异常”现象。于是进行了以下探究。
【实验1】向4份相同体积与浓度的稀盐酸中分别加入一定长度的某种镁带,现象如下:

【实验结论1】据表分析,________________是实验出现“异常”的因素之一。
【实验2】向4份相同体积与浓度的稀硫酸中分别加入一定长度的某种镁带,现象如下:
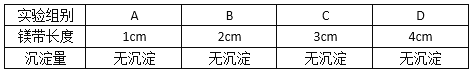
【实验结论2】对比实验1和实验2,______________是实验出现“异常”的因素之一。
(3)兴趣小组同学取一支试管,放入一根镁条,加入一定量硫酸铜溶液,观察到镁条表面有少量气泡产生,且有黑色物质生成。同学们对此实验的现象感到意外和困惑,于是查阅到了相关资料:
资料1:硫酸铜溶液在配制时加入了少量稀硫酸;
资料2:当金属粉末颗粒很小时,容易成为黑色;
资料3:生成的黑色物质可能是CuO、Cu中的一种或两种。
①镁条与硫酸铜溶液反应的实验中产生的气体可能为______________(写化学式)。
②同学们进一步设计实验确定黑色物质的成分,请在下表中补全实验方案。
实验操作 | 实验现象 | 结论 |
将黑色物质过滤、晾干后,分成两份 | / | / |
将其中一份装入硬质玻璃管中,向其中通入CO后,加热,并将生成的气体通入澄清石灰水中 | __________ | 黑色粉末中 含有CuO |
将另一份置于坩埚中,称其质量为m1,在空气中加热一段时间后冷却,称其质量为m2 | m1______m2(填“>”、“<”或“=”) | 黑色粉末中 含有Cu |
通过以上探究,兴趣小组同学确定了黑色物质为Cu和CuO两种。
(二)有关镁条表面灰黑色“外衣”组成的探究
【发现问题】镁是一种银白色有金属光泽的金属,但久置的镁条总有一层灰黑色的“外衣”,这层灰黑色的“外衣”是什么物质呢?
【查阅资料】
(1)灰黑色“外衣”的成分是碱式碳酸镁晶体,化学式为:xMgCO3yMg(OH)2zH2O;
(2)Mg(OH)2:白色固体,难溶于水,受热会分解生成两种氧化物;
(3)MgCO3:白色固体,微溶于水,受热会分解生成两种氧化物;
(4)相同条件下,Mg(OH)2受热分解的温度比MgCO3分解的温度更低。
【组成测定】为精确测量碱式碳酸镁晶体的组成,兴趣小组同学取4.66g该晶体用热重分析仪对进行加热,使得各成份在不同温度下逐个分解(加热首先失去结晶水),测定剩余固体质量与分解温度之间关系(如下图所示)。
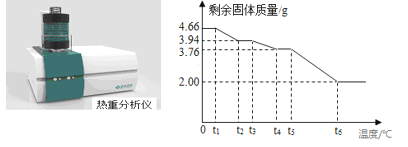
请回答下列问题:
(1)晶体中结晶水的质量为_______g。
(2)t4~t5段中,固体为_________(写化学式)。
(3)t5~t6段反应的化学方程式为________。
(4)根据图中数据计算xMgCO3yMg(OH)2zH2O中x:y:z =___________(填最简比)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com