
科目: 来源: 题型:
【题目】以甲为原料合成化工产品丁的微观过程如下图。下列说法正确的是

A. 乙、丁都是氧化物 B. 转化①中乙和丙的分子个数之比为1 : 1
C. 甲中氢元素的质量分数小于丁 D. 每个丁分子由6个原子构成
查看答案和解析>>
科目: 来源: 题型:
【题目】在实验室里称量一定质量的Na2CO3放入烧杯中,加入一定质量分数的稀硫酸100 g,恰好完全反应,共生成2.2 g的CO2气体(假设产生的气体完全逸出,水的挥发忽略不计)。已知实验中发生的化学反应:Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
(1)Na2CO3样品的质量为_________________g。
(2)100 g稀硫酸的溶质质量分数为_______________(写出计算过程)。
(3)反应后烧杯中溶液的溶质质量分数为______________(写出计算过程,结果精确到0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验是学习化学的一种重要手段。
(1)如图是实验室制备气体常用的装置。
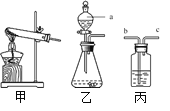
① 装置乙中仪器a的名称是_______,在该装置中它的作用主要是_______。
② 实验室用KClO3和MnO2制取O2时,应选用___________(填序号)作为发生装置,该反应的化学方程式为________。
③ 若用丙装置干燥O2,丙中盛放的试剂名称为_______,气体应从_______(填“b”或“c”)端通入。
(2)实验完全结束后,某同学要从剩余固体中提取KCl,实验流程如下:
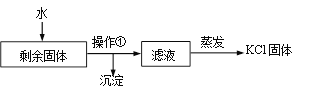
① 为了加快剩余固体在水中的溶解,可采取的一种措施是________。
② 流程中“操作①”的名称是________。
③ 玻璃棒在“蒸发”过程中搅拌的目的是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】五氧化二钒(V2O5)是一种工业催化剂,下图是生产V2O5的工业流程,下列说法正确的是
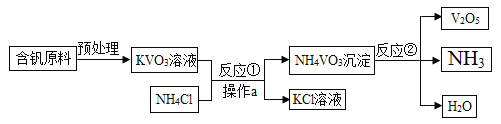
A. NH3能使干燥的红色石蕊试纸变蓝
B. 反应①中生成的副产物KCl在农业上可用作钾肥
C. 反应②的化学方程式为2NH4VO3![]() V2O5+2NH3↑+H2O
V2O5+2NH3↑+H2O
D. 操作a中需要的所有仪器为铁架台、烧杯、滤纸、玻璃棒
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线,下列说法正确的是
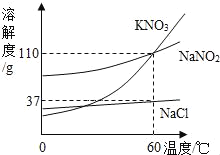
A. KNO3和NaNO2的溶解度相等
B. 60 ℃时,NaCl的饱和溶液的溶质质量分数为37%
C. 将接近饱和的NaNO2溶液变为饱和溶液,可采用降温的方法
D. 除去NaCl中少量KNO3,可在较高温度下制得浓溶液再冷却结晶、过滤、干燥
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线,下列说法正确的是
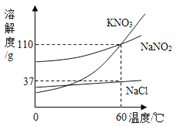
A. KNO3和NaNO2的溶解度相等
B. 60 ℃时,NaCl的饱和溶液的溶质质量分数为37%
C. 将接近饱和的NaNO2溶液变为饱和溶液,可采用降温的方法
D. 除去NaCl中少量KNO3,可在较高温度下制得浓溶液再冷却结晶、过滤、干燥
查看答案和解析>>
科目: 来源: 题型:
【题目】在实验室里称量一定质量的Na2CO3放入烧杯中,加入一定质量分数的稀硫酸100 g,恰好完全反应,共生成2.2 g的CO2气体(假设产生的气体完全逸出,水的挥发忽略不计)。已知实验中发生的化学反应:Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
(1)Na2CO3样品的质量为_________________g。
(2)100 g稀硫酸的溶质质量分数为_______________(写出计算过程)。
(3)反应后烧杯中溶液的溶质质量分数为______________(写出计算过程,结果精确到0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验是学习化学的一种重要手段。
(1)如图是实验室制备气体常用的装置。
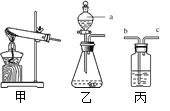
① 装置乙中仪器a的名称是_______,在该装置中它的作用主要是_______。
② 实验室用KClO3和MnO2制取O2时,应选用___________(填序号)作为发生装置,该反应的化学方程式为________。
③ 若用丙装置干燥O2,丙中盛放的试剂名称为_______,气体应从_______(填“b”或“c”)端通入。
(2)实验完全结束后,某同学要从剩余固体中提取KCl,实验流程如下:
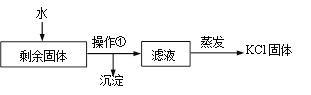
① 为了加快剩余固体在水中的溶解,可采取的一种措施是________。
② 流程中“操作①”的名称是________。
③ 玻璃棒在“蒸发”过程中搅拌的目的是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】五氧化二钒(V2O5)是一种工业催化剂,下图是生产V2O5的工业流程,下列说法正确的是
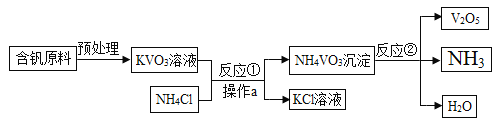
A. NH3能使干燥的红色石蕊试纸变蓝
B. 反应①中生成的副产物KCl在农业上可用作钾肥
C. 反应②的化学方程式为2NH4VO3![]() V2O5+2NH3↑+H2O
V2O5+2NH3↑+H2O
D. 操作a中需要的所有仪器为铁架台、烧杯、滤纸、玻璃棒
查看答案和解析>>
科目: 来源: 题型:
【题目】现有一家庭食用纯碱样品,其中含杂质氯化钠(不含其它杂质),为了测定样品中杂质氯化钠的质量分数,李明同学进行了三次实验。实验如下表:
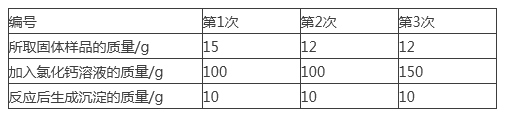
完成下列计算(计算结果精确到0.1%):
(1)样品中氯化钠的质量分数;
(2)加入氯化钙溶液的溶质质量分数;
(3)恰好完全反应时,反应后所得溶液中氯化钠的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com