
科目: 来源: 题型:
【题目】如图中A~J表示初中化学常见的物质。其中B、C、F、J为氧化物,且C能造成煤气中毒,F中两种元素的质量比是4∶1;D、H为相同类别的化合物,E、I也为相同类别的化合物,且D、I在某些情况下可用作干燥剂。“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
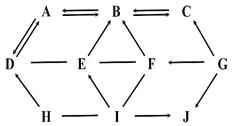
(1)写出化学式:C________________。
(2)写出化学方程式:
A转化为D的反应________________________________;
I转化为E的反应________________________________;
F转化为B的置换反应____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属材料包括纯金属以及它们的合金。
(1)铁锅、铝锅和铜火锅可以用来炒菜、做饭和涮肉,是因为铁、铝、铜能够________。
(2)为了验证铁、铝、铜的金属活动性顺序,某同学选择了打磨过的铁丝,他还需要选择的两种盐溶液是__________________。写出实验中发生反应的化学方程式:_____________________。
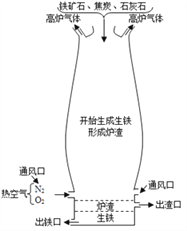
(3)炼铁的原理是利用一氧化碳与氧化铁的反应,化学方程式为______________________,该反应中氧化铁表现出______________(填“氧化性”或“还原性”)。如图是炼铁高炉示意图,写出原料焦炭的一个作用:_________________________。
(4)5g某钢样在纯氧中完全燃烧,得到0.33g二氧化碳。求此钢样中碳的质量分数______。(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】溶液与人们的生活息息相关。
(1)氯化钠、硝酸钾、氢氧化钙在不同温度时的溶解度如下表所示:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
①60℃时,氯化钠的溶解度____________硝酸钾的溶解度(填“>”、“<”或“=”)。
②氢氧化钙的饱和溶液加热后变浑浊,原因是____________________________________。
③20℃时,向氢氧化钙的饱和溶液中加入少量生石灰并恢复至20℃,溶液中溶质的质量 _________(填“增大”、“减小”或“不变”)。
④要从含有少量氯化钠的硝酸钾溶液中得到较多的硝酸钾,可以采用加热浓缩、________、过滤的方法,得到的滤液中含有_______________(填离子符号)。
(2)制作“叶脉书签”需要使用质量分数为10%的氢氧化钠溶液。用氢氧化钠固体配制50g质量分数为10%的氢氧化钠溶液,配制过程如下图所示:
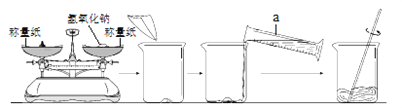
①写出图中标号仪器的名称:a______________。
②指出图中称量步骤的错误操作:_____________________________;_____________________________。
③若用质量分数为25%的氢氧化钠溶液配制50g质量分数为10%的氢氧化钠溶液,所需25%的氢氧化钠溶液和水的质量比为 ______。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列装置图,回答有关问题:
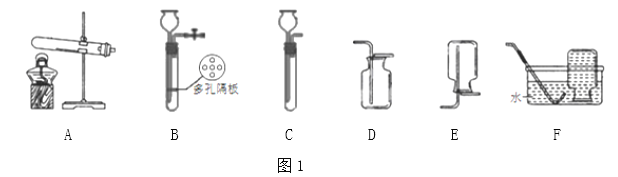
(1)实验室用过氧化氢溶液和二氧化锰制取氧气,化学方程式为___________________;选用图1中的装置D收集氧气,验满方法是_______________________________________。
(2)实验室用大理石和稀盐酸制取二氧化碳,化学方程式为______________。
(3)某同学在家尝试制取二氧化碳,发生装置如图2。
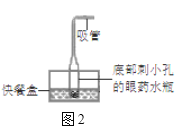
①眼药水瓶中的固体是碎鸡蛋壳,快餐盒中的液体可能是厨房中常用的___________(填字母)。
A.盐水 B.糖水 C.白酒 D.白醋
②眼药水瓶可以上下移动,该装置相当于图1中的装置________(填字母)
查看答案和解析>>
科目: 来源: 题型:
【题目】作为重要的能源,燃料对于人类社会是非常重要的。
(l)氢气被认为是理想的清洁、高能燃料,可以通过以下反应制得: 2NaCl+2H2O通电 2X+Cl2↑+H2↑,其中X的化学式是____________。
(2)乙醇可用作酒精灯、内燃机等的燃料,写出乙醇充分燃烧的化学方程式:__________。
(3)在相同的温度和压强下,相同体积的气体具有相同的分子数,反之亦然。在20℃、101kPa下,1m3一氧化碳和1m3甲烷分别充分燃烧,消耗氧气的体积比为____________。
(4)使燃料充分燃烧通常考虑两点:一是燃烧时要有足够的空气;二是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在催化剂的作用下,用O2将HCl转化为Cl2 ,可提高效益,减少污染,转化流程如图所示。下列说法正确的是
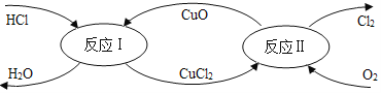
A. 反应I是置换反应,反应II是复分解反应
B. 氯、氧、铜三种元素的化合价发生了变化
C. 该转化可表示为4HCl+O2 ![]() 2Cl2+2H2O
2Cl2+2H2O
D. 需要不断补充CuO,该转化才能持续进行
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组用传感器探究稀氢氧化钠溶液与稀盐酸反应过程中温度和pH的变化,测定结果如图所示。下列说法正确的是

A. 实验中溶液的温度一直升高、pH一直增大 B. 氢氧化钠与盐酸的中和反应先放热后吸热
C. 40s时溶液中的溶质为氢氧化钠和氯化钠 D. 该实验是将稀氢氧化钠溶液滴入稀盐酸中
查看答案和解析>>
科目: 来源: 题型:
【题目】硒在元素周期表中的某些信息如图,下列说法不正确的是
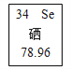
A. 硒属于金属元素 B. 硒的原子序数是34
C. 硒原子中的质子数是34 D. 硒的相对原子质量是78.96
查看答案和解析>>
科目: 来源: 题型:
【题目】定量研究是科学研究的重要方法之一,利用它能解决许多生产生活中的实际问题。
(1)将20g质量分数为4%的氢氧化钠溶液与7.3g稀盐酸混合,恰好完全反应,所得溶液的pH为7,试计算所用稀盐酸的溶质质量分数为_______________。
(2)实验室浓盐酸的溶质质量分数在36%~38%之间为合格药品。(1)题中的稀盐酸是用质量为2g的浓盐酸加水配制而成的。请通过计算判断该浓盐酸是否为合格药品。______________
查看答案和解析>>
科目: 来源: 题型:
【题目】物质的变化
我们的家乡是座美丽的滨海小城,这里三面环海,海洋蕴含着丰富的资源,以下是人们从海洋中获取某些物质的方法:
①膜法淡化海水获得淡水; ②蒸馏法从海水中提取淡水;③采用蒸发结晶的方法晒得粗盐;④开采出原油并进行分馏获得汽油、煤油等产品;⑤向粗盐的溶液中加入试剂制得精盐;⑥向海水中添加石灰乳,再向得到的沉淀中加稀盐酸,然后电解获得的氯化镁制得镁;⑦用贝壳(主要成分碳酸钙)制生石灰。
(1)请从物质变化的角度对上述方法进行分类:一类是_______________(填写序号),另一类是______________(填写序号),你的分类依据是__________________________。
(2)和①膜法淡化海水原理相同的一个实验操作是______,原理都是依据_____________不同将混合物中的各成分分离。
(3)在②蒸馏法淡化海水时水的三态变化过程首先是由______态变为____态的蒸发过程,然后是由______态变为____态的冷凝过程,这与自然界中___________循环的原理类似。请描述蒸馏法淡化海水的微观过程_______________________________。
(4)在③海水晒盐的过程中,钠离子、氯离子、水分子三种微粒的运动状态是:首先在海水中这三种微粒处于__________的运动状态(选填“自由”或“在固定位置振动”,下同),在晒盐过程中,_________(填微粒名称)不断运动到空气中去,另两种粒子结合后处于__________________的运动状态以晶体的形式析出,跟该结晶微观过程正好相反的一个物理变化是________________。
(5)在⑤粗盐精制的操作中为除去过量的碳酸钠、氢氧化钠,需要添加适量的稀盐酸,请写出稀盐酸和氢氧化钠的反应中,有效作用的粒子有______________。
(6)写出⑥中“电解氯化镁获得金属镁”的化学方程式________________,该反应的基本反应类型是___________________。
(7)贝壳制得的生石灰可用来做干燥剂,日常生活中常见的干燥剂除了生石灰干燥剂外,还有一种硅胶干燥剂,硅胶吸附性能高、化学性质稳定,其内部为毛孔网状结构,能够吸收水分,并将水分保留住。根据提供的信息分析他们的干燥原理是否相同?________,理由是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com