
科目: 来源: 题型:
【题目】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”。其标签如图所示,某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究。

【提出问题】:久置固体的成分是什么?
【查阅资料】:铁与氯化铁溶液在常温下发生反应:Fe+2FeCl3=3FeCl2
打开固体包装观察:部分固体呈黑色,部分固体呈白色,另有少量红棕色的块状固体。
【作出猜想】:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
其中可能含有Fe2O3的依据是________________________________。
【实验探究】:甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
(1)取少量久置固体于试管中,滴加足量的蒸馏水,搅拌 | 固体溶解,试管外壁发烫 | 固体中一定含有_________ |
(2)过滤,在滤液中滴加无色酚酞溶液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
(3)取滤渣放入试管中,滴加足量的______________ | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有________, 一定不含氧化铁 |
【实验质疑】:乙同学认为甲同学在实验中得出 “一定不含氧化铁”的结论是错误的,理由是____________。你认为甲同学哪一步实验操作得出的结论也不合理:____________,理由是______(用化学方程式表示)。
【继续探究】乙同学另取久置的固体进行实验探究:
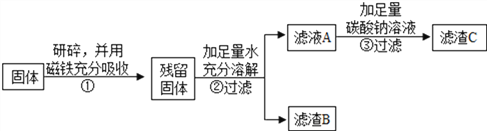
乙同学对滤渣B进行探究:
实验操作 | 实验现象 | 实验结论 |
取滤渣B于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、______、 有气泡冒出、___________ | 固体中一定含有CaCO3和Fe2O3。写出Fe2O3和稀盐酸反应的化学方程式:________________ |
【计算得出结论】:
如上述实验流程,乙同学现取5g久置固体研碎,用磁铁吸引,得残留固体3g,加足量水充分溶解过滤,得滤渣B的质量为1.8g。在滤液A中加足量碳酸钠溶液后过滤得滤渣C的质量为2g。请计算:
(1)滤液A中含氢氧化钙的质量为______________。(写出计算过程)
(2)通过计算,得出残留固体的成分:__________________。(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验设计不能达到实验目的的是( )
选项 | A | B | C | D |
实验 设计 |
|
|
|
|
实验 目的 | 探究二氧化碳能与水反应 | 探究燃烧所需要的条件 | 探究铁生锈 需要氧气 | 探究空气中氧气的体积分数 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】根据所学的知识并结合下图的仪器,回答有关问题。
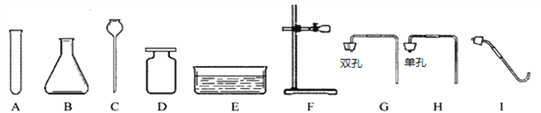
(1)写出仪器E的名称___________。
(2)实验室用高锰酸钾为原料来制取并收集氧气,除选用A、D、E、F、I外,还缺少的仪器是____________,反应的化学方程式为__________________。收集氧气时,发现水槽内的水变成紫红色,其原因是________________。
(3)实验室要制取并收集多瓶二氧化碳气体(需随时添加液体药品),其发生装置需要的仪器有______________(填字母),反应的化学方程式为________________________ 。
(4)若用下图所示的装置收集二氧化碳,气体应该从_____管通入(填“a”或“b”)。如要收集干燥的二氧化碳,在收集前需要将气体通入盛有_________(填药品名称)的下图容器中。
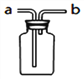
(5)氮的氧化物(NO2)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NO2还原成N2,某同学在实验室中对NH3与NO2的反应进行了探究。
(资料:NO2有毒,常温下为红棕色,实验中常用氢氧化钠溶液进行尾气处理;同温同压下,不同气体的体积之比等于分子个数之比。)
现将收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图装置进行实验。
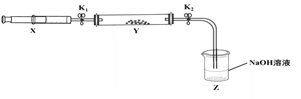
(Ⅰ)打开K1,推动注射器活塞,使X中的气体缓慢通入Y中,Y管中的现象_____________,反应方程式是_____________。
(Ⅱ)将注射器活塞退回原处并固定,待装置恢复到室温,Y中有少量水珠。
(Ⅲ)打开K2,观察到的现象____________________,原因是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在实验室里,某同学看到氢氧化钠试剂瓶的瓶口有白色粉末,他对白色粉末的成分作出了一些猜测。
猜测一:可能是氧氧化钠 猜测二:可能是碳酸钠 猜测三:可能是氧氧化钠和碳酸钠
为探究白色粉末的成分,他将该粉末溶于水,得到无色溶液,再迸行了如下实验:
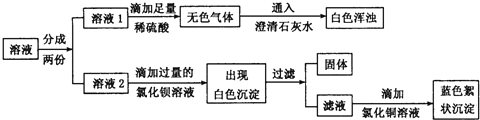
(1)根据实验现象推测,无色气体是________。
(2)在溶液2中滴加过量氯化钡溶液的目的是____________________
(3)由实验现象可知,猜测___是正确的,写出产生蓝色絮状沉淀的化学方程式__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】归纳与演绎是重要的科学方法,也是常用的化学学习方法。
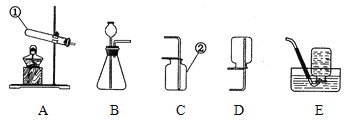
(1)写出标号仪器的名称:①_______________、②______________;
(2)我们已经学过实验室制取O2、H2、CO2三种气体的反应原理,制取与收集方法,请你归纳出实验室制取这三种气体反应的共同点___________(填序号)。
A.需要加热 B.需用催化剂 C.没有气体参加反应 D.生成的气体只有一种
(3)气体发生装置A可用来制取O2,其反应的化学方程式为________________________,可采用______装置来收集该气体。(填序号)
(4)化学上可通过多种反应得到NH3(极易溶于水,密度比空气小),例如:
a.2NH4Cl(固) + Ca(OH)2(固)△CaCl2 + 2NH3↑+ H2O
b.NH4HCO3 (固)△NH3↑+ CO2↑+ H2O c.CaO (固)+ NH3·H2O=NH3↑+ Ca(OH)2
结合以上实验装置完成下列填空: (以下所选装置均填装置序号)
我将选择反应__________(只需选填“a”、“b”或“c”中的一种)作为实验室制取NH3的反应原理,选用上图中的___________作为反应的发生装置,采用的收集装置是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列A ~ F是初中化学中的六个实验,请按要求填空:
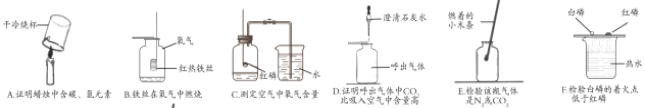
(1)B中反应的化学方程式______________________________,集气瓶中水的作用是_________________。
(2)F装置的实验现象___________________________。
(3)上述实验中不能达到实验目的的是________________(填字母),请选择其中一项说明改进措施_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂生产的烧渣(主要含有FeO、Fe2O3和SiO2),可用于制备七水合硫酸亚铁晶体(FeSO4·7H2O),其工艺流程如下:
(资料:SiO2不溶于水,也不与稀硫酸反应。)
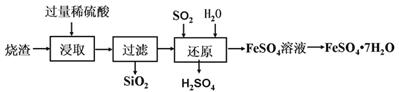
(1)“浸取”步骤中,发生反应的化学方程式有_________、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O。
(2)为提高“浸取”步骤的反应速率,可采取的具体措施有_________________(写1条,不考虑“搅拌”、“使用催化剂”)
(3)“还原”的目的是将Fe3+转化为Fe2+。写出“还原”过程中反应的化学反应方程式________________。
(4)该工艺中可循环利用的物质是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下图是某种品牌的补钙药品的部分说明书。请回答下列问题:
XX钙片
[药品规格] 每片含CaCO3 0.625g
[用法用量] 每次一片,每天2次
①CaCO3的相对分子质量是_________。 ②如果按用量服用,每天摄入钙元素的质量为___________g。
(2)为解决化石燃料日益枯竭的危机,人类正在研究利用光解的方法制取未来理想燃料——氢气,请计算2升水理论上可以制得_________克的氢气。目前氢能源还不能广泛使用的原因是(至少答一条):____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(题文)(1)请你用最合适的化学式或微粒符号填空:空气中含量最多的气体________;硫酸钠中的阴离子________;改良酸性土壤时常用的一种碱:_________;。
(2)豆浆机由于快捷方便而进入千家万户。请根据图示回答:
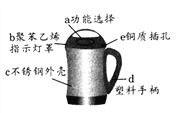
①制作材料中属于金属或合金的是_______(选填一种物质编号),属于有机合成材料的是_________(选填一种物质编号);制作手柄的塑料属于____________塑料(填“热塑性”或“热固性”);
②豆浆已成为众多家庭的早餐饮品,以下是豆浆中一些营养成分的平均质量分数。请根据下表回答:
成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素A |
质量分数/% | 96.0 | 1.8 | 0.7 | 1.1 | 0.01 | 0.03 | 0.0005 | 0.015 |
豆浆中含有的微量元素是__________;青少年缺乏______元素易患有佝偻病。在豆浆所含的营养素中能供给人体能量的营养素有______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com