
科目: 来源: 题型:
【题目】CuCl2是一种重要的化工原料。工业上常采用将Cu与稀盐酸在持续通入空气的条件下反应,FeCl3具有催化作用。反应原理如图所示。下列说法正确的是
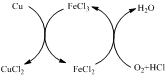
A. 反应过程中需不断添加FeCl3溶液
B. 若反应恰好完全进行,将6.4g的铜完全反应,需消耗10%的盐酸73g
C. 缓缓通入空气,能提高氧气的利用率
D. 该实验说明Cu能与稀盐酸发生置换反应
查看答案和解析>>
科目: 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示(mol·L-1是浓度的一种表示方法)。下列说法正确的是
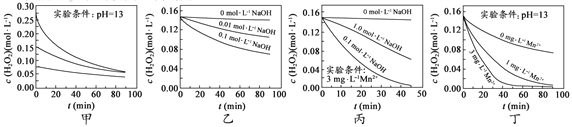
A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液pH越大,H2O2分解速率越快
C. 图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丁表明,碱性溶液中,Mn2+浓度越大,H2O2分解速率越快
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学活动小组用镁和铁探究金属的反应规律。
【查阅资料】
①镁,铁的活动性均在 H 之前并且镁比铁活泼。
②相同条件下,相同时间内金属的活动性越强,与酸反应越剧烈,产生的氢气越多。
【探究一】在室温条件下进行如图所示实验。试管内的镁带和铁片表面均被打磨洁净,且形 状、大小相同;同时加入等质量和等浓度的稀盐酸。
(1)该兴趣小组的同学认为该方案中长颈漏斗起非常重要的作用。
①通过相同条件下,相同时间内长颈漏斗中 __________
②长颈漏斗在实验中还可以起_________________ 作用。
(2)在甲、乙装置的水中滴入 2~3 滴红墨水的目的_______________。
(3)乙装置中反应方程式为______________,该反应属于基本反应类型中的_______反应。
(4)观察到甲装置中产生气泡速率比乙装置快或 __________现象时,都可以证明镁的金属活动性比铁的强。
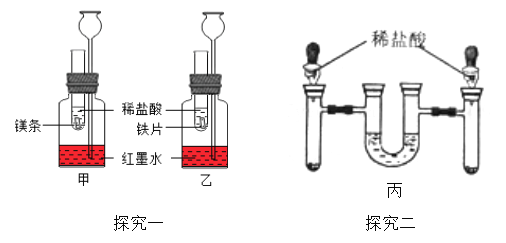
【探究二】方案二:如图丙,将等质量光亮洁净,形状厚薄相同的镁条和铁片分别放入左、 右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U 型管内为水,初始液面相平,反应过程中装置气密性良好)。
(5)实验过程中 U 型管中液面 _______(填“左高右低”,“左低右高”,“相平”); 充分反应后,冷却到室温 U 型管中液面 ___________填“左高右低”,“左低右高”,“相平”),原因是_____。
【探究三】在硫酸铜和硫酸亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出 的固体中滴加稀硫酸,没有气泡产生。下列判断正确的是 ________。写成发生反应的化学方程式 ________ 。
A.滤出的固体中一定含有铜 B.滤出的固体可能含有铁和镁
C.滤液中可能含有硫酸铜 D.滤液中一定含有硫酸镁和硫酸亚铁
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列 A~D 的四个实验,请按要求填空。

(1)A 实验中,请写出标号为①的仪器名称____。用该装置来制取二氧化碳气体的一个明显错误的地方是____,是否可以用该装置来制取氧气呢?____(填“是”或“否”),反应原理是____。
(2)B 实验中观察到的现象是____。
(3)C 实验中正极产生的气体是____(写化 学式),由此实验得出水是由_______组成的。
(4)D 实验中将镁条在空气中点燃后再放入充满 CO2的集气瓶中,发现镁条继续剧烈 燃烧,发出白光,放热,产生一种白色固体和一种黑色固体。已知该反应为置换反应,则反 应的化学方程式为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】小雨收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程 ,最终制成蒸馏水。
其实验过程如下所示。请回答以下问题
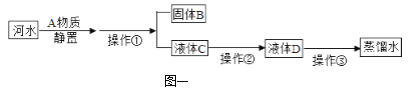
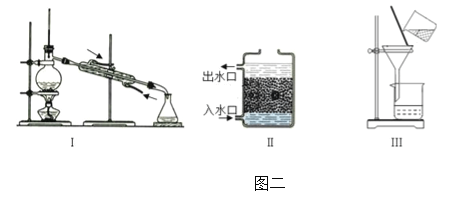
(1)如图所示:A物质的名称是____,目的是____。操作①的名称是_____,若经过操作①后,所得液体 C 中仍有浑浊,其原因可能是____(填写序号);
a.漏斗内的滤纸有破损缘 b.漏斗下端未靠在烧杯内壁 c.漏斗内液面高于滤纸的边缘
(2)操作②应选用图二中的____(填序号)装置,该过程主要是____变化( 填“物理”或“化学”)。
(3)净化程度最高的操作应选用图二中的_____(填序号)装置,加入沸石的作用 是_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】金属锈蚀是一个世界性难题。
(1)铁生锈是在空气和____共同作用的结果,铁锈中金属阳离子的化学式为____。
(2)金属铝表面常有一层致密的氧化膜,该氧化膜的化学式是_________ 。
(3)为了防止水龙头生锈,其表面常镀一层铬,其防锈的原理是____。
(4)要除去 24 g 铁锈(Fe2O3)至少需要含硫酸多少克的稀硫酸溶液_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】I、用所学化学知识填空。
(1)下列材料不属于合金的是____(填“陶瓷”或“硬铝”)。
(2)改良酸性土壤可以用____(填“烧碱”或“消石灰”);
(3)打开瓶塞,在空气中能产生“白雾”的是____(填“浓硫酸”或“浓盐酸”);
(4)用井水洗衣服时,肥皂不易起泡沫且产生浮渣,该井水是____(填“硬水”或“软水”)。
II、请完善网络图,并根据图示关系回答下列问题:
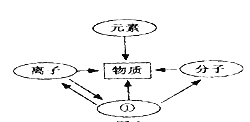
(1)物质是由 __________组成的;
(2)构成物质的微粒有分子、离子和 ______________;
(3)分子是由 ________________构成的;
(4)原子得到电子转化为________________(填“阳离子”或“阴离子”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是甲、乙两种物质(不含结晶水)的溶解度曲线.下列说法中正确的是
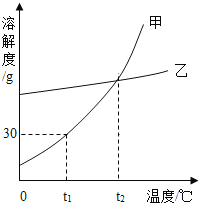
A.甲的溶解度大于乙的溶解度
B.t1℃时,50g甲的饱和溶液中有15g甲
C.t2℃时甲的饱和溶液降温至t1℃变为不饱和溶液
D.当甲中含有少量乙时,可以用降温结晶的方法提纯甲
查看答案和解析>>
科目: 来源: 题型:
【题目】近几年来,全国各地掀起苹果醋饮料风,苹果酸(C4H6O5)是苹果醋的主要成分之一,下列说法错误的是
A. 苹果酸中碳、氢、氧三种元素的质量比为 4:6:5
B. 苹果酸由碳、氢、氧三种元素组成
C. 苹果酸的相对分子质量为 134
D. 苹果酸中氧元素的质量分数为60%
查看答案和解析>>
科目: 来源: 题型:
【题目】溶质质量分数为10%的KNO3 溶液可用来配制花卉、盆栽植物的营养液。请回答:
(1)KNO3溶液能给花卉、盆栽植物提供需要量较大的营养元素是_______________。
(2)某同学用KNO3固体配制100g 10%的KNO3 溶液的过程如下(水的密度为1.0g/mL):
①计算:需要KNO3的质量是10g,水90g。
②称量:用托盘天平称量KNO3的质量。天平调零后,分别在天平左右托盘放上质量相同的纸片。先向右盘添加10g砝码 ,然后向左盘慢慢添加 KNO3直至天平平衡。
③量取:往量筒中倒入一定量的水后(见下图1),接下来的实验操作是_______________。
④溶解:将称量出的固体和量取到的水依次倒入烧杯中,用玻璃棒搅拌至固体全部溶解。
⑤装瓶贴标签:请在标签上写上内容(见下图2)。
 _______________
_______________
(3)将上述配好的100g溶液稀释成0.8%的稀溶液,需要加入_________________g水。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com