
科目: 来源: 题型:
【题目】某实验小组利用废硫酸液制备K2SO4 主要过程如下:
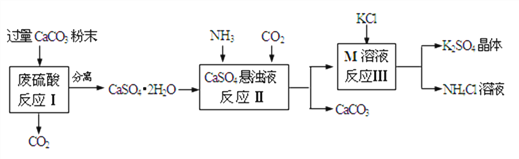
(1)反应Ⅰ过程中要不断搅拌,其目的是__________________________________。
(2)上述流程中可循环使用的物质有CO2和_______________(填写名称)。
(3)反应Ⅲ中相关物质的溶解度如下表。你认为反应Ⅲ在常温下能实现的原因是_____________。
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
请写出该反应的化学方程式 ______________________。
(4)将反应Ⅲ得到的K2SO4晶体用饱和K 2SO4溶液洗涤而不用水洗的目的是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组做了以下实验探究。向包有Na2O2的脱脂棉中吹气,发现脱脂棉剧烈燃烧起来。于是他们决定探究脱脂棉燃烧的原因。请你参与他们的探究。
【提出问题】脱脂棉为什么会燃烧?
【查阅资料】
(1)Na2O2是一种淡黄色固体,常温下能与CO2、H2O、HCl气体等物质发生反应,不能与N2发生反应。
(2)人呼出的气体的主要成分及含量:N2:74%;O2:16%;水蒸气:6%;CO2:4%
(3)CO2既不与NaHCO3反应,也不溶于饱和的NaHCO3溶液。
【猜想与假设】
(1)可能是CO2与Na2O2反应产生了O2,释放出热量。
(2)可能是H2O与Na2O2反应产生了O2,释放出热量。
(3)可能是____________与Na2O2反应产生了O2,释放出热量。
【实验验证】
实验I:验证CO2与Na2O2反应产生了O2,释放出热量。
同学们用下图所示的装置(部分夹持装置略去)进行实验验证猜想1成立。打开止水夹K,鼓入纯净、干燥的氮气一段时间后,关闭止水夹K.注入稀盐酸,观察到脱脂棉剧烈燃烧。
【解释与结论】
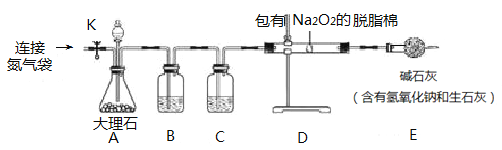
(1)从脱脂棉可燃烧的现象可知它是一种______________________。
(2)注入稀盐酸前鼓入纯净、干燥的氮气的目的是_______________。
(3)装置C中盛放的药品是_______________________。
(4)已知该反应还生成一种盐,则反应的化学方程式为_____________________。
实验II:验证H2O与Na2O2反应产生了O2,释放出热量。
(1)验证H2O与Na2O2反应产生了O2(略)
(2)验证H2O与Na2O2反应能释放出热量,请简述一个实验方案(写出实验步骤、现象及结论)_____。
【拓展与应用】保存过氧化钠时应注意______等事项.
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组在实验室制备气体的过程如下,请回答下列问题:
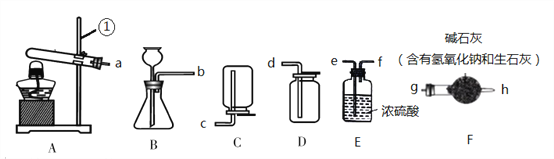
(1)二氧化碳气体制备
实验室制备CO2,其反应的化学方程式为_________________。应选择的气体收集装置为______(选填装置对应的字母)。
(2)氨气制备
实验室制备NH3的反应原理为:Ca(OH)2(固)+2NH4Cl(固)![]() CaCl2+2H2O+2NH3↑。现要制备并干燥NH3,所选装置的正确连接顺序为_____→______(选择装置对应的导管口字母)。仪器①的名称是______________。
CaCl2+2H2O+2NH3↑。现要制备并干燥NH3,所选装置的正确连接顺序为_____→______(选择装置对应的导管口字母)。仪器①的名称是______________。
(3)拓展延伸
实验室制备O2也可用上述制备NH3的发生装置,写出用该发生装置制备O2的化学方程式__________。在医院给病人输氧时,可以利用E装置在瓶中装大约半瓶蒸馏水,对该装置的作用下列说法正确的是______。
A.f导管可以连接供给氧气的钢瓶 B.该装置可以保持氧气的湿润
C.该装置不用来观察是否有氧气输出 D.该装置能用来观察输出氧气的速度
查看答案和解析>>
科目: 来源: 题型:
【题目】法国化学家尼古拉斯·勒布朗早在1791年发明的工业合成碳酸钠的方法,简称勒布朗制碱法。该方法包括以下几个反应阶段:①原料氯化钠与浓硫酸在高温下反应得到产物硫酸钠和氯化氢气体,②在1000℃条件下通过硫酸钠与木炭反应生成硫化钠和二氧化碳,③生成的硫化钠继续和碳酸钙反应来得到碳酸钠。请完成下列计算(计算过程保留3位有效数字)
(1)假设每一步反应物的量足够,反应完全,理论上每获得1kg纯度为80%的纯碱需要氯化钠的质量是_________kg。
(2)反应②中碳单质过量时也同样可以反应获得Na2S,此时所发生的反应化学方程式是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示四种液体或溶液中存在的粒子示意图。(图中粒子个数不代表实际粒子数目关系)
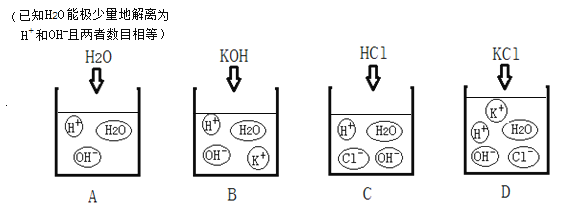
请回答。
(1)在烧杯A、B、C中分别滴入2-3滴酚酞溶液,烧杯______(填字母编号)的溶液变红。
(2)若烧杯D的溶液是另取一定量的烧杯B、C 中的溶液混合后得到的,再向其中滴入酚酞溶液不变红,小明推断是氢氧化钾与盐酸恰好完全反应了。小红则提出该推断_____(填“正确”或“不正确”),理由是_____________________。烧杯D 中水分子的数目一定______(填“大于”或“等于”或“小于”)烧杯B、C中的水分子数目之和。
(3)四个烧杯中能证明使酚酞变红的粒子不是K+的是_____________________(填字母编号)。
依据烧杯A、B、C中滴入酚酞溶液后的现象,请从微观角度解释酚酞溶液遇液体或溶液变红的原因是_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示,请结合图表数据回答下列问题:
氢氧化钠 | 碳酸钠 | |||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |
(1)下图表示________(填“氢氧化钠”或“碳酸钠”)的溶解度曲线。
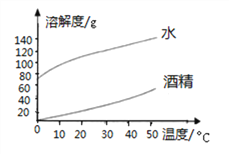
(2)温度从20℃升到40℃时,氢氧化钠在水中的溶解度变化__________(填“大于”或“小于”)碳酸钠在水中的溶解度变化。
(3)40℃ 时,若将50gNaOH分别投入到100g水和100g酒精中,能形成饱和溶液的溶剂是__,再将CO2通入所得NaOH的酒精溶液中,观察到的现象为______________。
(4)若要对比两种固体物质的溶解性,必须在_____________、______________ 、_____________的条件下进行对比。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如下图所示。
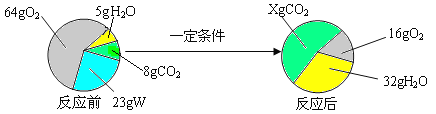
下列关于以上反应的说法中,正确的是
A. X的值为44 B. W由碳、氢两种元素组成
C. 该反应属于置换反应 D. W中碳、氢元素质量比为4∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入溶质质量分数为26.5%的碳酸钠溶液,测得溶液pH随加入碳酸钠溶液质量的变化曲线如下图所示。
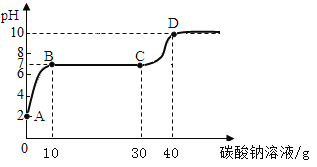
回答下列问题:
⑴A点处溶液中溶质的化学式是CaCl2和______________;
⑵计算原滤液中氯化钙的质量分数为_____________(写出计算过程,结果精确到0.1%)。
⑶根据计算所得数据在下图中画出产生沉淀的曲线。
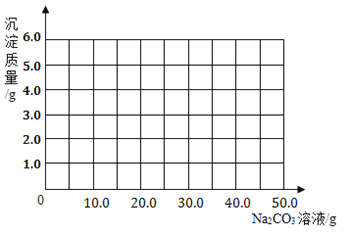 _______________
_______________
⑷CD段pH上升的原因是________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国女科学家屠呦呦获2015年诺贝尔生理学或医学奖。她最初的发现,让青蒿素(化学式:C15H22O5)成为世界卫生组织推荐的一线抗疟药,挽救了全球数百万人的生命。而下图是某厂生产的青蒿素的说明书部分内容。
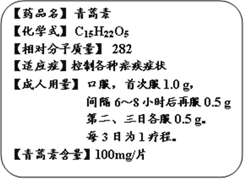
⑴青蒿素属于____________化合物(填“有机”或“无机”)
⑵青蒿素含有____________种元素;碳、氧的原子个数比为____________(填最简比)。
⑶青蒿素中氢元素的质量分数是_________(精确到0.1%)。
⑷用青蒿素控制疟疾症状一般以三天为1个疗程。根据图中说明,一个成人疟疾患者在一个疗程中共需服该药物____片。
查看答案和解析>>
科目: 来源: 题型:
【题目】兴趣小组同学为了弄清即将维修的沼气池中气体的成分,进行了有关实验。请你与他们一起完成以下探究活动:
【收集气体】将不加盖的矿泉水瓶装满水,用细绳吊入池中,再用木棍拨动使瓶中的水全部倒出(见图),然后迅速拉起矿泉水瓶,盖上瓶盖。

这种方法属于____________集气法。
【对气体猜想】猜想Ⅰ:全部是CH4; 猜想Ⅱ:全部是CO;
猜想Ⅲ:全部是CO2; 猜想Ⅳ:是CH4和CO2的混合气体。
【实验和推断】

⑴若“现象a”为石灰水变浑浊,则说明气体中含有_____气体。
⑵步骤②的目的是____________________________________;步骤③“注水装置”应选下图中的____________(填序号)。

⑶若“现象b”为杯壁有水雾出现,有同学认为“猜想Ⅰ或Ⅳ”成立,其反应方程式为:____________; 另有同学认为此现象不能证明收集到的气体中一定含有氢元素,理由是_______________;要排除这种干扰可采取的措施是______________________________。
⑷ 采取⑶中的排除干扰措施后:若“现象a、b”为无明显现象,“现象c”为石灰水变浑浊,则证明“猜想_________”成立;若“现象a、c”均为石灰水变浑浊,“现象b”为杯壁有水雾,则证明“猜想__________”成立。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com